Металлы iiA группы химического элементов включают в себя металлы щелочного земельного ряда периодической таблицы. Они являются наиболее активными металлами и обладают характерными свойствами, которые позволяют им образовывать щелочные соединения.
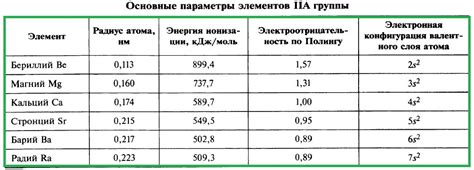
К металлам iiA группы относятся бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Эти элементы отличаются высокой электроотрицательностью и возможностью образовывать катионы с положительным зарядом.
Металлы iiA группы легко реагируют с кислородом, аммиаком, водой и другими активными неорганическими соединениями. Они образуют щелочные оксиды, гидроксиды и соли, которые широко используются в промышленности и жизнедеятельности человека.
Металлы iiA группы
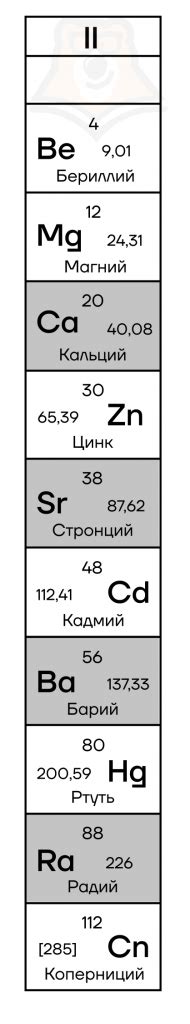
Металлы iiA группы - это группа химических элементов, которые расположены во второй группе периодической системы Менделеева. Всего в этой группе находится шесть элементов: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Металлы iiA группы отличаются высокой электропроводностью, благодаря наличию свободных электронов в своей внешней электронной оболочке. Они также обладают металлическим блеском и способностью образовывать ионы с положительным зарядом. Все элементы этой группы являются твердыми веществами при комнатной температуре, за исключением бериллия, которое имеет металлические свойства, но при этом достаточно хрупкое.
Металлы iiA группы активно участвуют в химических реакциях, особенно с кислородом и водой. Например, бериллий является амфотерным металлом и реагирует с кислотами и щелочами, а радий является самым активным из всех элементов и вступает в реакции даже с водой.
Элементы iiA группы также образуют соединения с другими элементами, такие как оксиды, гидроксиды и соли. Например, гидроксид бериллия (Be(OH)2) используется в стекольной промышленности, а оксид магния (MgO) является основным компонентом огнеупорных материалов.
Металлы как элементы периодической системы
Периодическая система элементов — это удивительная классификация химических элементов, где они упорядочены по возрастанию атомного номера и повторяющимся химическим свойствам. Металлы занимают значительную часть этой системы и представляют собой важный класс химических веществ.
Металлы обладают такими свойствами, как блеск, проводимость электричества и тепла, прочность и пластичность. Это делает их незаменимыми материалами во многих областях науки и промышленности.
Металлы могут быть разделены на несколько категорий в зависимости от своих химических свойств и особенностей структуры. Одной из наиболее известных категорий металлов являются щелочные металлы iiA группы, такие как литий (Li), натрий (Na), калий (K) и другие.
Щелочные металлы iiA группы обладают характерными свойствами, такими как низкая плотность, низкая температура плавления и реактивность с водой. Они являются одними из самых активных металлов и образуют щелочи при реагировании с кислородом. Щелочные металлы iiA группы широко используются в различных отраслях промышленности, включая производство стекла, фармацевтику и электронику.
Щелочные металлы и их особенности

Щелочные металлы, также известные как металлы iiA группы, являются элементами периодической системы, обладающими рядом уникальных особенностей. В эту группу входят литий, натрий, калий, рубидий, цезий и франций.
Первая особенность, присущая щелочным металлам, это их высокая реактивность. Эти элементы очень активно реагируют с кислородом, водой и другими веществами, что делает их полезными сырьем для производства различных химических соединений.
Еще одной особенностью щелочных металлов является их низкая плотность. Они являются одними из самых легких и наименее плотных металлов. Например, литий – самый легкий металл из всех известных и имеет плотность всего 534 килограмма на кубический метр.
Щелочные металлы также обладают высокой теплопроводностью и электропроводностью. Они являются отличными проводниками тепла и электричества, что делает их полезными в различных технологических процессах и в производстве электронных устройств.
Интересной особенностью щелочных металлов является их способность образовывать ионы со зарядом +1, что делает их положительными ионами. Это связано с тем, что внешний электрон их атомов находится в s-орбитали, что позволяет им легко отдавать свой электрон и образовывать положительные ионы.
- Литий (Li) – имеет применение в батарейках, лекарствах и пиротехнике;
- Натрий (Na) – широко используется в пищевой промышленности и для очистки воды;
- Калий (K) – важный элемент для растений и используется в удобрениях;
- Рубидий (Rb) – используется в оптике и некоторых технологических процессах;
- Цезий (Cs) – применяется при создании атомных часов и в научных исследованиях;
- Франций (Fr) – очень редкий элемент, используется только в научных исследованиях.
В заключение можно сказать, что щелочные металлы являются уникальными элементами, которые обладают рядом особенностей. Их высокая реактивность, низкая плотность, хорошая теплопроводность и электропроводность делают их полезными в различных областях науки и промышленности.
Образование щелочей и их реактивность
Щелочи - это группа веществ, которые обладают щелочной реакцией и способны образовывать гидроксиды металлов. Образование щелочей осуществляется при реакции щелочного оксида или щелочного гидроксида с водой.
Щелочные оксиды и гидроксиды имеют высокую реактивность и могут активно взаимодействовать с различными веществами. Они обладают щелочной реакцией и способны давать гидроксиды металлов при взаимодействии с водой.
Реактивность щелочей зависит от специфических свойств каждого металла. Например, натрий, калий и литий образуют наиболее активные щелочи, способные реагировать с водой даже при обычных условиях. Они образуют гидроксиды сильных оснований, которые растворяются полностью в воде и обладают щелочной реакцией.
Образование гидроксидов металлов и реактивность щелочей имеют применение в различных областях науки и техники. Щелочные вещества используются в процессе производства мыла, стекла, удобрений и других веществ. Они также широко применяются в химической промышленности и в лабораторных условиях.
Металлы iiA группы и их химические свойства
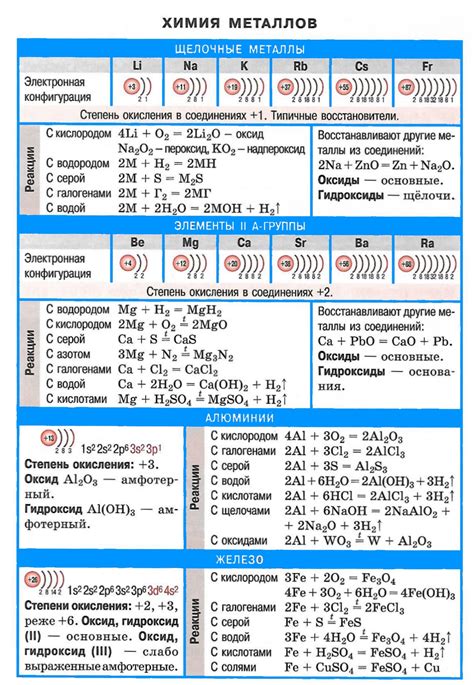
Металлы iiA группы периодической системы, такие как цинк (Zn), кадмий (Cd) и ртуть (Hg), обладают рядом уникальных химических свойств.
Во-первых, эти металлы имеют низкую температуру плавления и высокую теплопроводность. Например, цинк обладает температурой плавления всего 419 градусов по Цельсию, что позволяет использовать его в различных инженерных конструкциях. Кроме того, кадмий и ртуть обладают высокой теплопроводностью, что делает их полезными в электронике.
Во-вторых, металлы iiA группы имеют высокую реакционную способность и образуют стойкие соединения с другими элементами. Например, цинк активно реагирует с кислотами, образуя соли, такие как хлорид цинка. Кадмий и ртуть также образуют с различными элементами стойкие соединения, которые используются в медицине и промышленности.
В-третьих, эти металлы обладают специфическими физическими свойствами. Например, ртуть является единственным металлом, который находится в жидком состоянии при комнатной температуре. Это делает ртуть удобным материалом для использования в термометрах и других приборах.
В целом, металлы iiA группы обладают разнообразными и полезными химическими свойствами, которые находят применение в различных областях науки и техники.
Применение металлов iiA группы в промышленности
Металлы iiA группы, такие как магний, цинк и кадмий, широко используются в различных отраслях промышленности благодаря своим уникальным свойствам и высокой химической активности.
Магний, например, широко применяется в авиационной и автомобильной промышленности. Этот металл обладает низкой плотностью и высокой прочностью, что делает его идеальным материалом для изготовления легких и прочных конструкций. Магниевые сплавы применяются в производстве кузовов автомобилей, а также в проектировании и производстве самолетов.
Цинк имеет широкое применение в строительной и электротехнической промышленности. Цинковые покрытия используются для защиты металлических конструкций от коррозии. Кроме того, цинк широко используется в производстве батарей, металлокерамических конденсаторов и других электронных устройств.
Кадмий также находит свое применение в различных отраслях промышленности. Он используется в производстве аккумуляторов, паяльных препаратов, а также в качестве катализатора при производстве пластмасс и лакокрасочных материалов. Кадмий имеет высокую степень химической устойчивости, что позволяет использовать его в экстремальных условиях рабочей среды.
В целом, металлы iiA группы являются неотъемлемой частью промышленности и находят применение во многих отраслях, благодаря своим уникальным свойствам и химической активности.
Последствия взаимодействия металлов iiA группы с другими веществами
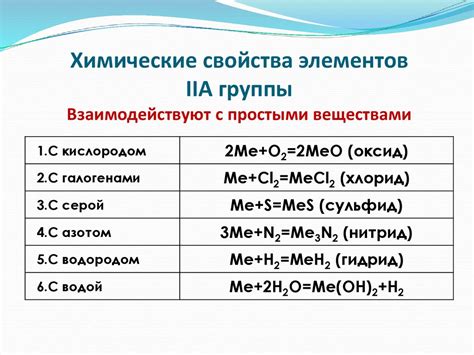
Металлы iiA группы, такие как цинк, медь и свинец, обладают способностью образовывать щелочи при взаимодействии с другими веществами. Это взаимодействие может приводить к различным последствиям, которые нельзя недооценивать.
При взаимодействии с водой металлы iiA группы образуют гидроксиды, которые являются щелочами. Гидроксиды обладают высокой щелочностью и могут вызывать ожоги на коже и слизистых. Поэтому при работе с этими металлами необходимо соблюдать правила безопасности, использовать защитные средства и избегать попадания гидроксидов на кожу.
Взаимодействие металлов iiA группы с кислотами может привести к образованию солей и выделению водорода. Это может привести к разрушению металлических поверхностей и образованию пузырьков газа. Поэтому при обработке металлов iiA группы кислотами необходимо быть осторожным и проводить работу в хорошо проветриваемом помещении.
Кроме того, металлы iiA группы могут реагировать с органическими веществами, такими как спирты или амины. Это может приводить к образованию новых соединений, которые могут быть токсичными или опасными для здоровья. Поэтому при работе с этими металлами необходимо соблюдать правила хранения и использования органических веществ, а также избегать их смешивания с металлами iiA группы.
Все эти последствия взаимодействия металлов iiA группы с другими веществами подчеркивают необходимость соблюдения мер безопасности при работе с этими металлами. Только при соблюдении правил и предосторожностей можно избежать негативных последствий и обеспечить безопасность работников и окружающей среды.
Вопрос-ответ

Какие металлы входят в iiA группу?
Металлы iiA группы включают в себя медь (Cu), серебро (Ag) и золото (Au).
Что такое iiA группа?
iiA группа – это вторая группа периодической таблицы элементов, которая включает металлы с двумя электронами в внешней энергетической оболочке.
Почему металлы iiA группы образуют щелочи?
Металлы iiA группы образуют щелочи, так как они обладают всего двумя электронами в своей внешней энергетической оболочке. Это делает их готовыми отдавать эти электроны и образовывать ионы с положительным зарядом, что приводит к образованию щелочей.
Какие свойства обуславливают способность металлов iiA группы образовывать щелочи?
Способность металлов iiA группы образовывать щелочи обуславливается их низкой электроотрицательностью и наличием всего двух электронов в внешней энергетической оболочке. Это свойства, которые делают их готовыми отдавать эти электроны и образовывать ионы с положительным зарядом.
