Гальваническая пара возникает при контакте двух различных металлов или сплавов в присутствии электролита. При этом один из металлов действует как анод, а другой как катод. Возникающий электрический потенциал между металлами может привести к коррозии одного из них. Однако существуют металлы и сплавы, которые не образуют гальваническую пару с другими материалами.
Один из примеров таких металлов - платина. Платина обладает высокой химической стойкостью и стабильностью при контакте с другими металлами и сплавами. Она не окисляется и не реагирует с большинством химических веществ. Именно поэтому платину широко используют в различных сферах: от производства ювелирных изделий до катализаторов в химической промышленности.
Еще одним примером металла, который не образует гальваническую пару, является золото. Золото также обладает высокой стойкостью к окислению и реакциям с другими материалами. Благодаря этим свойствам, золото считается одним из наиболее долговечных и престижных металлов, используемых в производстве ювелирных изделий и монет.
Еще одним интересным примером металла, который не образует гальваническую пару, является нержавеющая сталь. Этот сплав, состоящий преимущественно из железа, хрома и никеля, обладает высокой коррозионной стойкостью и не реагирует с другими металлами. Нержавеющая сталь широко применяется в различных отраслях, включая пищевую, химическую и нефтегазовую промышленность.
Избегать гальванической пары:

Гальваническая пара - это электрохимическая ячейка, образованная двумя различными металлическими материалами и электролитом, в которой происходит перенос электрона между разными металлическими материалами. При этом один металл становится анодом, выделяет электроны, а другой металл становится катодом, принимает электроны. В результате образуются различные химические соединения и происходит коррозия, что может повлиять на долговечность и надежность металлических конструкций.
Чтобы избежать гальванической пары, следует выбирать металлические материалы, которые не образуют пару друг с другом. Например, использование алюминия и нержавеющей стали вместе может привести к образованию гальванической пары, поэтому в таких случаях рекомендуется применять алюминий с пластмассой или алюминий с цинком.
Также имеет значение правильный выбор электролита. Некоторые электролиты могут способствовать образованию гальванической пары между различными металлическими материалами, поэтому для предотвращения коррозии возможно использование ингибиторов коррозии или добавление неактивных веществ в электролит.
Для точного определения, какие металлические материалы могут быть использованы вместе без образования гальванической пары, можно пользоваться специальными таблицами электрохимического ряда, которые показывают потенциалы окисления различных металлов. Такие таблицы помогут выбрать подходящую комбинацию металлических материалов для конкретного проекта и максимально уменьшить вероятность образования гальванической пары.
Металлы без реакции:
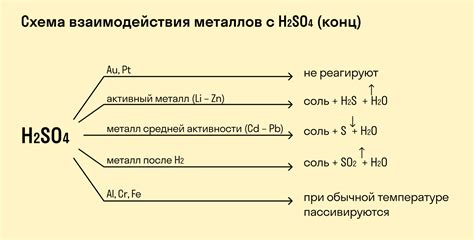
Существуют такие металлы, которые не образуют гальваническую пару с другими металлами и не проявляют реакций при контакте с другими веществами. Они обладают высокой химической стойкостью и используются в различных отраслях промышленности.
Один из примеров таких металлов - золото. Этот благородный металл не реагирует с окружающей средой и сохраняет свой блеск и цвет на протяжении долгого времени. Золото часто используется в ювелирной промышленности для изготовления украшений и монет.
Другим примером металла без реакции является платина. Этот металл обладает высокой стойкостью к коррозии и реакциям с кислотами. Платина широко применяется в химической промышленности, электронике и при производстве автомобилей.
Еще одним металлом без реакции является серебро. Оно также обладает химической стойкостью и не окисляется на воздухе. Благодаря своим свойствам, серебро используется в производстве посуды, зеркал, ювелирных изделий и в фотографии.
Таким образом, металлы без реакции являются важными материалами, которые находят широкое применение в различных отраслях промышленности, благодаря своей стойкости и химической инертности.
Пассивные металлы:

Пассивные металлы - это такие металлы, которые обладают способностью образовывать защитные пассивные пленки на своей поверхности. Эти пленки состоят из оксидов, гидроксидов или других соединений металла с кислородом или другими элементами и служат для защиты металла от коррозии. Основными представителями пассивных металлов являются алюминий, титан, хром и нержавеющие стали.
Алюминий - один из самых распространенных пассивных металлов. Он образует тонкую оксидную пленку на своей поверхности, что защищает его от окисления и коррозии. Это делает алюминий очень популярным материалом в различных отраслях, включая авиацию и строительство.
Титан - еще один пример пассивного металла. Он обладает высокой стойкостью к коррозии благодаря образованию плотной и прочной оксидной пленки на своей поверхности. Это делает титан незаменимым материалом в производстве химического оборудования и медицинских имплантатов.
Хром - также является пассивным металлом, образующим стабильную оксидную пленку на своей поверхности. Хромовые покрытия используются для защиты стали от коррозии и повышения ее эстетических качеств. Хром также входит в состав нержавеющих сталей, которые обладают высокой коррозионной стойкостью.
Нержавеющие стали - это специальные сплавы, которые содержат хром, никель и другие элементы. Они образуют плотную оксидную пленку на своей поверхности, что делает их устойчивыми к коррозии. Нержавеющие стали широко применяются в различных сферах, включая пищевую промышленность, химическую промышленность и строительство.
Использование металлов без гальванической пары:

Гальваническая пара — это комбинация двух различных металлов, находящихся в электрическом контакте в электролите. В результате этого контакта и химических реакций между металлами и электролитом, один из металлов может начать активно корродироваться. Однако, существуют металлы, которые не образуют гальваническую пару и могут использоваться без риска коррозии и ухудшения качества изделий.
Один из таких металлов — нержавеющая сталь. Она обладает высокой стойкостью к коррозии благодаря присутствию в составе специальных добавок, таких как хром или никель. Нержавеющая сталь широко используется в производстве кухонной посуды, трубопроводов, химических реакторов и других изделий, которым требуется высокая стойкость к воздействию влаги и агрессивных сред.
Еще одним металлом, не образующим гальваническую пару, является алюминий. Этот легкий и прочный металл широко применяется в авиационной, строительной и электротехнической отраслях. Алюминий обладает высокой коррозионной стойкостью, благодаря наличию защитного оксидного слоя на поверхности металла, который предотвращает дальнейшее окисление и разрушение.
Также стоит отметить титан, который считается одним из самых коррозионностойких металлов. Он применяется в медицинском оборудовании, автомобильной и авиационной промышленности, а также в производстве химических реакторов. Титан не образует гальваническую пару с другими металлами и способен выдерживать агрессивные воздействия окружающей среды.
Использование этих металлов без образования гальванической пары является эффективным способом защиты изделий от коррозии и повышения их долговечности.
Вопрос-ответ

Какие металлы не образуют гальваническую пару?
Все металлы могут образовывать гальваническую пару при взаимодействии с другими металлами, однако существуют некоторые пары металлов, которые образуют очень слабую гальваническую пару и практически не вызывают коррозии. Например, одним из таких металлов является сталь нержавеющая. Она обладает хорошей коррозионной стойкостью и может использоваться в паре с другими металлами без опасности гальванической коррозии.
Может ли золото образовывать гальваническую пару?
Да, золото может образовывать гальваническую пару при взаимодействии с другими металлами. Однако, золото является одним из наиболее инертных металлов и обладает высокой коррозионной стойкостью. Поэтому, гальваническая коррозия золота в парах с другими металлами обычно не представляет опасности.
Какие металлы образуют наиболее опасную гальваническую пару?
Некоторые металлы образуют более опасную гальваническую пару, которая может привести к интенсивной коррозии. Например, амальгама ртути и алюминия образует очень активную гальваническую пару, что может вызывать серьезные проблемы. Также, пара цинка и меди является довольно активной и вызывает интенсивную коррозию.
Может ли гальваническая коррозия привести к поломке металлических конструкций?
Да, гальваническая коррозия может привести к поломке металлических конструкций. Когда два различных металла находятся в электролите, формируется гальваническая пара, при которой один металл становится катодом, а другой – анодом. Анод, при этом, начинает корродировать. Постепенно, это может привести к разрушению и обрушению конструкции.

