Окисление щелочных металлов - это процесс, при котором эти металлы взаимодействуют с кислородом воздуха и образуют оксиды. Щелочные металлы включают в себя такие элементы, как литий, натрий, калий и другие. Степень окисления щелочных металлов зависит от реакционной способности металла и условий окружающей среды.
Окисление щелочных металлов часто происходит под воздействием кислорода, который присутствует в атмосфере. Когда металлы взаимодействуют с кислородом, происходит образование оксидов, которые являются стабильными соединениями. Окисление щелочных металлов может быть также вызвано водой или другими реагентами.
Степень окисления щелочных металлов зависит от их химических свойств. Например, литий и калий имеют наибольшую реакционную способность и легко окисляются. Натрий и рубидий обладают меньшей активностью и окисляются не так быстро. Кроме того, влияние окружающей среды также может повлиять на степень окисления щелочных металлов.
Степень окисления щелочных металлов
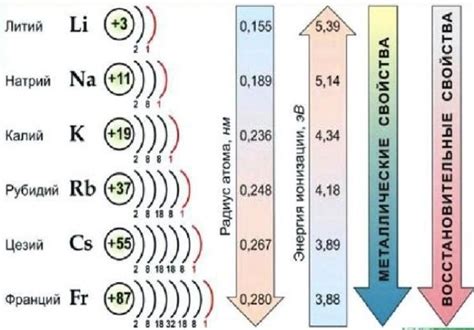
Степень окисления щелочных металлов определяет количество электронов, которые атом металла может потерять при образовании ионов. Щелочные металлы, такие как литий, натрий, калий и др., характеризуются наиболее низкой степенью окисления среди всех элементов.
Наиболее распространенная степень окисления щелочных металлов составляет +1. Это означает, что атом металла теряет один электрон и образует положительно заряженный ион. Например, натрий (Na) при окислении образует ион Na+, а калий (K) - ион K+.
Причина низкой степени окисления щелочных металлов связана с их электронной конфигурацией. У всех щелочных металлов во внешней оболочке находится один электрон, который легко отделяется при реакциях с другими веществами. Это делает их очень реакционноспособными и способными образовывать ионы с положительной зарядом.
Степень окисления щелочных металлов также может изменяться в зависимости от условий окружающей среды и типа взаимодействующего элемента. Например, в реакциях со взвешенным кислородом (как вода или пероксиды), щелочные металлы могут иметь степень окисления +2, теряя два электрона и образуя ионы с двойным положительным зарядом.
Важно отметить, что степень окисления щелочных металлов может также влиять на их свойства и способность реагировать с другими веществами. Высокая реакционность щелочных металлов делает их полезными в различных областях промышленности и химии.
Причины и особенности

Степень окисления щелочных металлов - это характеристика электронной конфигурации атома щелочного металла, и она определяет количество электронов, которые атом может потерять или приобрести при образовании химических связей.
Основной причиной высокой степени окисления щелочных металлов является их электронная конфигурация. Атомы щелочных металлов имеют один валентный электрон в s-подуровне, что делает их очень реактивными. Это значит, что они готовы легко отдавать этот электрон и образовывать положительные ионы с полным октетом валентных электронов.
Особенностью щелочных металлов также является их низкая ионизационная энергия. Это означает, что для удаления валентного электрона из атома щелочного металла требуется мало энергии. В связи с этим, щелочные металлы образуют ионы с положительными зарядами, превышающими 1, что демонстрирует высокую степень окисления.
Более того, щелочные металлы имеют низкую электроотрицательность, что позволяет им легко отдавать электрон и образовывать стабильные соединения с другими элементами. Это объясняет их способность образовывать сильные основания и обеспечивает им важное место в химии и технологии.
Режимы окисления

Режимы окисления щелочных металлов могут быть различными и зависят от условий, в которых происходит окисление. В основном можно выделить три основных режима окисления: низкотемпературное окисление, высокотемпературное окисление и электрохимическое окисление.
Низкотемпературное окисление характеризуется относительно низкой температурой окружающей среды и медленной скоростью реакции окисления. В этом режиме окисление щелочных металлов обычно происходит на поверхности материала и приводит к образованию оксидной пленки. При этом оксидные слои, образующиеся в умеренных условиях, чаще всего имеют комплексный состав.
Высокотемпературное окисление происходит при повышенных температурах и воздействии кислорода или других окислителей. В этом режиме окисления образуются более тонкие и равномерные слои оксидов на поверхности металла. Также важным фактором в этом режиме является скорость окисления, которая может быть значительно выше, чем при низкотемпературном окислении.
Электрохимическое окисление щелочных металлов происходит при взаимодействии металла с растворами или электролитами. В этом режиме окисления металл полностью или частично реагирует с ионами окислителя, что приводит к образованию соответствующих окислительных соединений. Таким образом, электрохимическое окисление может наблюдаться при проведении электролиза или при использовании электрохимических методов, например, для очистки поверхности металла от окисных пленок.
Характерные свойства
Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, обладают рядом характерных свойств, связанных со своей степенью окисления.
- Щелочные металлы имеют степень окисления +1, что делает их самыми электроотрицательными среди всех элементов блока s периодической системы.
- Эти металлы очень реактивны и способны быстро реагировать с водой, кислородом и другими веществами.
- Одной из ключевых особенностей щелочных металлов является их способность образовывать ионы с положительным зарядом. Ионы щелочных металлов могут легко перейти в раствор и взаимодействовать с другими ионами и молекулами.
- Щелочные металлы являются хорошими проводниками электричества и тепла. Это связано с наличием свободных электронов в их структуре.
- Щелочные металлы имеют низкую плотность и низкую температуру плавления и кипения. Они являются мягкими и легкими материалами.
- При сгорании щелочные металлы могут образовывать яркий пламя, что делает их полезными в фейерверках и пиротехнике.
Вопрос-ответ

Какие металлы относятся к щелочным?
К щелочным металлам относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs), франций (Fr).
Что такое степень окисления щелочных металлов?
Степень окисления щелочных металлов определяет количество электронов, которые металл отдает или принимает при образовании соединений. Она является положительным целым числом.
