Магний - это легкий химический элемент, обладающий высокой электроотрицательностью и хорошей теплопроводностью. Этот металл имеет множество применений в промышленности и технологиях, а также в медицине и пищевой промышленности.
Взаимодействие магния с кислородом - одно из наиболее значимых свойств этого металла. При контакте с воздухом магний очень быстро окисляется, покрываясь тонкой слоем оксида. Это служит защитой от дальнейшего окисления, что позволяет использовать магний в щитках от радиации, а также в аэрокосмической промышленности.
С другой стороны, магний может быть взаимодействовать с кислотами, образуя соли и водород газ. Например, магний реагирует с соляной кислотой, образуя хлорид магния и выделяя водород. Это свойство широко используется в лабораторных условиях, а также в производстве компонентов для аккумуляторов и взрывчаток.
Еще одно важное взаимодействие магния - с водой. При контакте магний с водой свободный водороду, а сам металл окисляется в оксид. Этот процесс достаточно быстрый и сопровождается выделением тепла. Именно из-за этого свойства магний часто используется в производстве специальных материалов для пищевой промышленности, приготовления растворимых витаминных добавок и средств для лечения желудочно-кишечного тракта.
В заключении, магний считается одним из наиболее активных химических элементов, которые активно взаимодействуют с другими веществами. Благодаря своим свойствам, магний нашел широкое применение в различных отраслях промышленности и науки, что делает его незаменимым материалом во многих сферах человеческой деятельности.
Свойства металла магния

Магний — лёгкий металл серебристо-белого цвета. Он обладает рядом уникальных физических и химических свойств, которые делают его важным материалом в различных отраслях промышленности и технологий.
Физические свойства:
- Магний является одним из самых лёгких металлов, его плотность составляет около 1,7 г/см³. Это делает его идеальным для применения в авиационной и автомобильной промышленности, где важен низкий вес и высокая прочность.
- При комнатной температуре магний обладает хорошей теплопроводностью и электропроводностью, что делает его востребованным материалом в производстве электрических и теплотехнических устройств.
- Магний является реактивным металлом и легко сгорает на воздухе, образуя яркую и горячую пламя. Из-за этого он находит применение в пиротехнике и производстве светящихся сплавов.
Химические свойства:
- Магний обладает высокой химической активностью и легко вступает в реакцию с водой и кислородом. Он растворяется в минеральных кислотах, образуя соли магния.
- Магний способен реагировать с многими неорганическими и органическими соединениями, что делает его важным компонентом в производстве сплавов, металлокерамики и различных химических соединений.
Применение магния:
- Магний используется в производстве лёгких сплавов, которые применяются в авиационной, автомобильной и судостроительной промышленности для создания конструкционных элементов с высокой прочностью и низким весом.
- Магниевые сплавы также используются в производстве спортивных товаров и инструментов, таких как велосипеды, гольф-клюшки и теннисные ракетки.
- Магний применяется в производстве химических соединений, таких как оксид магния, сульфат магния и карбид магния, которые находят применение в медицине, сельском хозяйстве и производстве удобрений.
Магний: лёгкий и прочный металл

Магний - металл, который отличается легкостью и прочностью. Он является одним из самых легких строительных материалов, его плотность составляет всего около 1,7 г/см³. Благодаря этому, магний активно используется в авиационной и космической промышленности, где важными критериями являются уменьшение массы и повышение прочности конструкций.
Магний имеет хорошую устойчивость к коррозии и окислению, что позволяет использовать его в производстве судов, автомобилей и спортивных инструментов. Он также обладает высокой теплоотдачей и является хорошим проводником электричества, поэтому его применяют в производстве радиаторов и электрических компонентов.
Магний является важным элементом в области медицины. Он используется для производства магниевых препаратов, которые применяются для лечения ряда заболеваний, таких как астма, сердечная недостаточность и гипертония. Магний также играет важную роль в обмене веществ и укреплении костной ткани.
В природе магний встречается в виде растворов, оксидов и солей. Он занимает второе место по распространенности среди металлов в земной коре. Магний получают из природных минералов путем их обогащения и последующей термической обработки.
Магний и вода
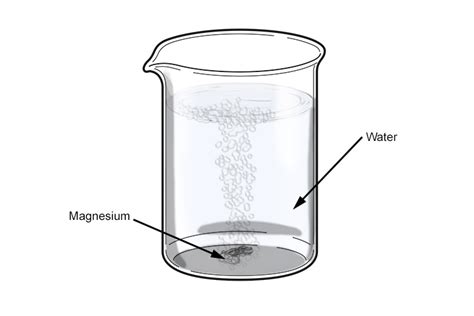
Магний является химическим элементом, который обладает высокой реакционной способностью. Взаимодействие магния с водой приводит к различным химическим реакциям.
В холодной воде магний медленно растворяется, образуя ион магния (Mg2+). При этом происходит выделение водорода (H2) в виде пузырьков. Реакция магния с водой происходит гораздо более интенсивно, если вода нагрета.
Магний активно взаимодействует с горячей водой, при этом образуется гидроксид магния (Mg(OH)2), а также выделяется водородный газ. Водородный газ может легко воспламеняться, поэтому взаимодействие магния с горячей водой является очень опасным.
В общем, взаимодействие магния с водой происходит с выделением водорода и образованием гидроксида магния. Это явление может использоваться для получения водорода в химических лабораториях или промышленности.
Магний и вода: нейтралное взаимодействие

Магний – активный химический элемент, который обладает высокой реакционной способностью. Однако, при взаимодействии с водой магний проявляет себя совершенно иначе – нейтрально.
Вода – это химическое соединение, состоящее из молекул, каждая из которых состоит из двух атомов водорода и одного атома кислорода. При контакте с магнием, вода не происходит каких-либо мгновенных реакций или образования газовых булыжников. Напротив, вода способствует защите магния от окисления и коррозии.
Молекулы воды образуют вокруг поверхности магния защитную пленку, которая препятствует дальнейшему проникновению влаги. Таким образом, вода действует как барьер для повреждения и разрушения поверхности магния.
Нейтральное взаимодействие магния с водой делает его полезным и устойчивым к воздействию окружающей среды. Магний используется в различных сферах, включая производство сплавов, производство металлических конструкций, металлообработка, производство огнеупорных материалов и другие.
Магний и кислоты
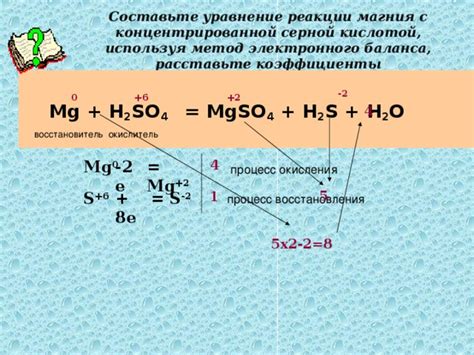
Магний, химический элемент с атомным номером 12, является активным металлом, который вступает в реакцию с различными кислотами. У него есть способность замещать другие металлы в ряду активности металлов. Это означает, что магний может образовывать соли с кислотами, такими как соляная кислота (HCl) и серная кислота (H2SO4).
Магний взаимодействует с соляной кислотой, образуя хлорид магния (MgCl2) и выделяя водород. Уравнение реакции может быть представлено следующим образом: Mg + 2HCl → MgCl2 + H2. Реакция происходит с выделением тепла.
При взаимодействии магния с серной кислотой образуется сульфат магния (MgSO4) и также выделяется водород. Уравнение реакции выглядит следующим образом: Mg + H2SO4 → MgSO4 + H2. Эта реакция также сопровождается выделением тепла.
Магний также может реагировать с другими кислотами, такими как азотная кислота (HNO3) и фосфорная кислота (H3PO4), образуя соответствующие соли и выделяя водород. Реакции в таких случаях аналогичны и дополнительные продукты образуются следующим образом: Mg + HNO3 → Mg(NO3)2 + H2 и Mg + 2H3PO4 → Mg3(PO4)2 + 3H2.
Вопрос-ответ

Какие свойства имеет металл магний?
Металл магний обладает легкостью, хорошей теплопроводностью и высокой пластичностью. Он также хорошо взаимодействует с кислородом, образуя оксид магния.
Как металл магний взаимодействует с водой?
Металл магний реагирует с водой, образуя гидроксид магния и выделяя водород. Реакция протекает быстро и с выделением тепла.
