Щелочные металлы - это группа элементов, которая включает в себя литий (Li), натрий (Na), калий (K), рубидий (Rb) и цезий (Cs). Они относятся к первой группе периодической системы и характеризуются высокой химической реактивностью. Каждый щелочный металл обладает своей химической формулой, которая отражает его состав и структуру.
Например, химическая формула лития - Li. Литий является наименее плотным металлом из всех щелочных металлов и широко используется в производстве аккумуляторов и лекарственных препаратов. Также литий является важным компонентом в реакциях синтеза органических соединений.
Натрий химической формулой обозначается Na. Он является очень реактивным металлом, который применяется в производстве металлических сплавов и стекла. Натрий также используется в пищевой промышленности в качестве добавки, а его соединения применяются в медицине для лечения различных заболеваний.
Калий имеет химическую формулу K. Он является одним из основных элементов в почве и необходим для роста растений. Калийные соединения используются в производстве удобрений и средств по защите растений от вредителей и болезней. Калий также находит применение в производстве стекла, мыла, лекарственных препаратов и многих других отраслях промышленности.
Основные свойства щелочных металлов

Щелочные металлы - группа элементов, которая включает литий, натрий, калий, рубидий, цезий и франций. У них есть несколько общих свойств, которые делают их уникальными в периодической таблице.
1. Активность: Щелочные металлы легко реагируют с кислородом воздуха и водой, что делает их очень активными элементами. Это свойство делает их отличными выбором для использования в различных химических реакциях и в промышленных процессах.
2. Электроотрицательность: Щелочные металлы обладают низкой электроотрицательностью, что означает, что они имеют большую склонность отдавать электроны. Это делает их отличными металлами для создания ионов и участия в химических реакциях.
3. Плотность и точка плавления: Щелочные металлы имеют низкую плотность и низкую точку плавления, что делает их мягкими и легкими в обработке. Это делает их идеальными для использования в различных промышленных приложениях и процессах.
4. Химическая реактивность: Щелочные металлы очень реактивны и способны вступать в химические реакции с различными веществами. Это свойство позволяет им использоваться в различных областях, включая производство батарей, стекла и мыла.
5. Электропроводность: Щелочные металлы обладают высокой электропроводностью, что делает их идеальными для использования в электронике и производстве батарей. Они также являются важными компонентами в производстве жидких кристаллов и солнечных батарей.
Щелочные металлы: определение и классификация
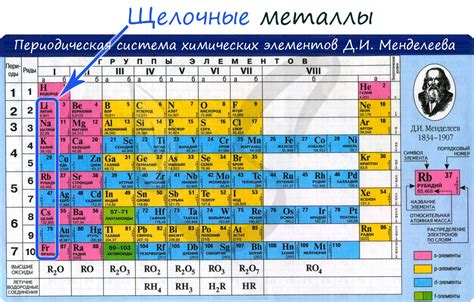
Щелочные металлы - это группа элементов периодической таблицы, которые характеризуются особыми химическими свойствами. Они включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Эти металлы называются щелочными из-за своей реактивности с водой, что проявляется в образовании щелочных растворов.
Щелочные металлы имеют низкую плотность, мягкие и легкоплавкие. Они образуют ионные соединения, обладающие высокой солевой растворимостью. Щелочные металлы также обладают высокой электроотрицательностью, что делает их хорошими веществами для образования ионов и переноса заряда в химических реакциях.
Щелочные металлы имеют широкое применение в различных отраслях промышленности и научных исследованиях. Например, литий используется в производстве аккумуляторов и лекарственных препаратах, натрий - в производстве стекла и мыла, калий - в сельском хозяйстве в качестве удобрений и регулятора pH, рубидий - в научных исследованиях и производстве специальных стекол и лазеров, цезий - в атомных часах и радиоактивных исследованиях.
В целом, щелочные металлы являются важными элементами химии, которые играют важную роль в различных отраслях науки и промышленности благодаря своей уникальной химической активности и физическим свойствам.
Применение щелочных металлов в различных отраслях

Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, нашли широкое применение в различных отраслях нашей жизни.
Литий, благодаря своим уникальным свойствам, используется в производстве аккумуляторов для электромобилей, компьютеров и мобильных устройств. Он также применяется в фармацевтической промышленности, в процессе производства лекарств для лечения психических и нервных расстройств.
Натрий является неотъемлемым компонентом пищевой промышленности. Соли натрия, такие как поваренная соль, используются в приготовлении пищи и консервировании. Кроме того, натрий применяется в процессе получения щелочи и соды, которые широко используются в производстве мыла, стекла, моющих средств и водоочистки.
Калий играет ключевую роль в сельском хозяйстве, так как он является необходимым питательным элементом для растений. Калийные удобрения помогают улучшить качество и урожайность сельскохозяйственных культур. Кроме того, калий применяется в производстве стекла, мыла и статистических красителей.
Рубидий и цезий, благодаря своим свойствам светоизлучения, нашли применение в производстве светодиодов, лазеров и ядерных энергетических установок. Они также используются в научных исследованиях, медицине и разработке новых материалов.
Все эти примеры демонстрируют важность щелочных металлов в различных отраслях и их значительный вклад в нашу повседневную жизнь и технологический прогресс.
Вопрос-ответ

Какие элементы относятся к щелочным металлам?
К щелочным металлам относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Какие основные свойства имеют щелочные металлы?
Основные свойства щелочных металлов включают: низкую плотность, мягкость, низкую температуру плавления и кипения, хорошую проводимость тепла и электричества, реакционную способность с водой, образование щелочных растворов и соединений.
Какие соединения образуют щелочные металлы?
Щелочные металлы образуют различные соединения, включая оксиды, гидроксиды и соли. Они также могут образовывать соединения с другими элементами, такими как кислород, сера и азот.
Какие применения имеют щелочные металлы?
Щелочные металлы имеют широкий спектр применений. Например, литий используется в аккумуляторах, натрий используется в пищевой промышленности, калий является необходимым элементом питания для растений, рубидий используется в лазерной технологии, а цезий применяется в ядерных исследованиях.
