Разбавленная серная кислота – одна из наиболее распространенных кислот, используемых в химических и промышленных процессах. Она является сильно электролитическим веществом, обладающим выраженными кислотными свойствами. Также серная кислота обладает способностью взаимодействовать с различными металлами, приводя к образованию газообразного продукта.
Реакция разбавленной серной кислоты с металлами происходит по следующей схеме: металл реагирует с серной кислотой, при этом выделяется водород. Реакция протекает по типу односторонней замены, когда металл вытесняет водород из серной кислоты, в результате чего образуется соль металла и образуется газовый продукт.
При этой реакции разбавленная серная кислота может реагировать со множеством металлов, однако скорость реакции и процентное соотношение продуктов зависят от конкретного металла и его активности. Металлы, обладающие высокой активностью, способны быстро реагировать с разбавленной серной кислотой, образуя большое количество газообразного продукта.
Реакция разбавленной серной кислоты с металлами имеет широкое применение в химической промышленности и лабораторных условиях. Газообразный продукт, в данном случае водород, может быть использован в различных производственных процессах и энергетических целях. Кроме того, данная реакция является примером химической реакции, которая происходит с участием кислоты и металла, и позволяет изучать основы химии, взаимодействия веществ и образование новых веществ.
Реакция серной кислоты с металлами

Серная кислота — одна из самых популярных химических соединений, широко используемая в промышленности и научных исследованиях. Она обладает сильной жидкостью и способна реагировать с различными веществами. Особо интересной и быстро протекающей реакцией, связанной с серной кислотой, является ее взаимодействие с металлами.
Реакция серной кислоты с металлами — это экзотермические реакции, при которых металлы разрушаются, а присутствующая кислота выделяет газовый продукт. Например, одной из самых распространенных реакций является реакция серной кислоты с цинком. В ходе этой реакции цинк растворяется в серной кислоте, образуя сульфат цинка и выделяя газ-водород.
Интересно отметить, что реакция серной кислоты с металлами происходит гораздо быстрее при повышенной температуре. Также она может быть интенсифицирована путем использования металлов с более высокой активностью, например, магния или алюминия.
Реакция серной кислоты с металлами широко используется в химической промышленности, а также в лабораторных исследованиях. Она может применяться для получения различных соединений, включая сульфаты металлов, а также для выделения водорода, который могут использовать в различных процессах, например, водородного соединения или производства электроэнергии.
Определение разбавленной серной кислоты
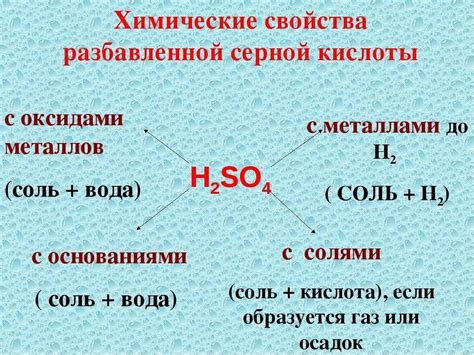
Разбавленная серная кислота — это водный раствор серной кислоты с низкой концентрацией. Ее концентрация обычно представлена в виде процентной величины или в молярной концентрации. Разбавленная серная кислота широко применяется в лаборатории и промышленности.
Для определения концентрации разбавленной серной кислоты необходимо провести титрование. Титрование — это метод анализа, основанный на реакции химического вещества (титранта) с известным количеством другого вещества (титруемого). В данном случае титрантом выступает разбавленная серная кислота, а титруемым — щелочное растворное вещество, такое как натриевая гидроксид или гидроксид аммония.
Процесс титрования проводится путем добавления титранта до достижения точки эквивалентности, при которой происходит полное нейтрализация титруемого вещества. Это можно определить с помощью индикатора, который меняет свой цвет при достижении точки эквивалентности.
После проведения титрования можно определить концентрацию разбавленной серной кислоты, используя закон особой эквивалентности. Зная мольное соотношение между титрантом и титруемым, можно вычислить искомую концентрацию по формуле.
Реакция серной кислоты с металлами

Серная кислота – это одна из самых распространенных кислот, используемых в химической промышленности. Она обладает высокой активностью и способностью взаимодействовать с различными веществами. Особенно интересно ее взаимодействие с металлами.
При взаимодействии серной кислоты с металлами происходит реакция окисления, в результате которой образуется газообразный продукт. Например, серная кислота может взаимодействовать с цинком, что приводит к образованию сероводорода (H2S) и сульфата цинка (ZnSO4). Эта реакция имеет широкое применение в лабораторных и промышленных условиях.
Взаимодействия серной кислоты с металлами зависят от их активности. Некоторые металлы, такие как цинк, железо и алюминий, проявляют высокую реакционную способность и могут разрушить кислоту, освобождая при этом водород. Это объясняет их способность растворяться в серной кислоте.
Реакция серной кислоты с металлами часто сопровождается выделением тепла и образованием пены, а при достаточной концентрации кислоты может наблюдаться коррозия металла. Поэтому при работе с серной кислотой необходимо соблюдать меры безопасности и использовать защитные средства, чтобы избежать возможных травм и повреждений.
Итак, реакция серной кислоты с металлами – это важный химический процесс, который находит применение в различных областях науки и промышленности. Понимание этого процесса и его особенностей позволяет эффективно использовать серную кислоту как реактив и достичь необходимых результатов.
Газообразный продукт реакции

Реакция разбавленной серной кислоты с металлами приводит к образованию газообразного продукта. Это связано с тем, что разбавленная серная кислота обладает высокой активностью и способна выделять молекулярный кислород при взаимодействии с металлами.
Образование газообразного продукта является результатом окислительного взаимодействия металла с разбавленной серной кислотой. В ходе реакции металл отдает электроны, которые передаются на атомы кислорода в молекуле серной кислоты.
Газообразный продукт, который образуется при реакции разбавленной серной кислоты с металлами, зависит от типа металла, используемого в реакции. Например, при взаимодействии серной кислоты с цинком образуется водородный газ (H2), а при взаимодействии с медью - оксид серы (SO2).
Образование газообразного продукта при реакции разбавленной серной кислоты с металлами можно наблюдать путем накопления газа в колбе или реакционной смеси. Газ, выделяющийся в результате реакции, обычно сопровождается пузырьками и может быть легко улавливаем и идентифицирован.
Таким образом, реакция разбавленной серной кислоты с металлами приводит к образованию газообразного продукта, который зависит от типа металла и может быть использован для его идентификации. Эта реакция имеет широкое применение в химическом анализе и производстве различных веществ.
Области применения реакции

1. Производство водорода: Реакция разбавленной серной кислоты с металлами широко используется в производстве водорода. Эта реакция является одним из дешевых и эффективных способов получения водорода, который затем может быть использован в различных отраслях промышленности.
2. Очистка металлической поверхности: Разбавленная серная кислота проявляет свойства растворения металлов, поэтому ее можно использовать в процессе очистки поверхностей металлических изделий от окислов, ржавчины и других загрязнений. Это позволяет сохранить и восстановить их первоначальный внешний вид.
3. Производство удобрений: Разбавленная серная кислота может использоваться в процессе производства удобрений. Она используется для синтеза различных соединений серы, которые являются необходимыми элементами питания для растений. Такие удобрения способствуют повышению урожайности и качества сельскохозяйственных культур.
4. Аналитическая химия: Разбавленная серная кислота является важным реагентом в аналитической химии. Она используется для проведения различных химических анализов, включая определение концентрации различных веществ, исследование структуры химических соединений и т. д. Благодаря своим химическим свойствам, серная кислота обеспечивает точность и надежность получаемых результатов.
5. Производство электроники: Разбавленная серная кислота используется в процессе производства электронных компонентов. Она применяется для очистки и эцентрирования поверхностей полупроводниковых материалов, что позволяет создавать более эффективные и надежные электронные устройства.
6. Производство химических соединений: Реакция разбавленной серной кислоты с металлами может использоваться в процессе синтеза различных химических соединений. Такие соединения могут иметь широкий спектр применения в различных отраслях промышленности, включая фармацевтику, пищевую промышленность, производство пластмасс и многие другие.
Список металлов, реагирующих с серной кислотой

Серная кислота — это химическое соединение, которое является одним из самых распространенных кислот в химии. Она образуется при окислении сероводорода и широко используется в различных промышленных процессах и лабораторных исследованиях. Взаимодействие серной кислоты с различными металлами может привести к образованию газообразного продукта.
Список металлов, реагирующих с серной кислотой:
- Железо (Fe) – при взаимодействии с серной кислотой образуется два продукта: сложное соединение железа и серной кислоты, а также образуется водородный газ.
- Цинк (Zn) – серная кислота окисляет цинк, образуя соли и выделяется водородный газ.
- Медь (Cu) – медь при реакции с серной кислотой образует сульфат меди и выделяется двуокись серы (SO2) в газообразной форме.
- Алюминий (Al) – алюминий реагирует с серной кислотой, образуя алюминий сульфат и выделяется газообразный продукт – еще один оксид серы (SO3).
Вышеперечисленные металлы — не полный список тех, с кем может вступать в реакцию серная кислота. Однако эти реакции особенно интересны из-за образования газообразных продуктов. Это позволяет использовать эти реакции в различных химических процессах и аналитических методиках.
Важность реакции

Реакция разбавленной серной кислоты с металлами и образование газообразного продукта имеют большое практическое значение. Эта реакция является одной из основных реакций в химии и применяется в различных сферах деятельности.
В первую очередь, реакция использования серной кислоты с металлами играет важную роль в промышленных процессах. Серная кислота широко используется в производстве удобрений, веществ для промывки и очистки, а также в обработке металлов и полупроводников.
Кроме того, реакция разбавленной серной кислоты с металлами находит применение в лабораторной практике. Она используется для анализа и определения присутствия и концентрации различных элементов в образцах. Эта реакция позволяет получить газовый продукт, который можно проанализировать на его состав и свойства.
Важность этой реакции заключается также в ее применении в окружающей среде. Например, разложение серной кислоты с помощью металлов может быть использовано для нейтрализации опасных химических отходов, таких как старые батарейки или аккумуляторы. Это позволяет сократить загрязнение окружающей среды и предотвратить негативное воздействие на здоровье человека и животных.
В целом, реакция разбавленной серной кислоты с металлами и образование газообразного продукта не только является основой химических процессов в промышленности и лаборатории, но и играет важную роль в охране окружающей среды и безопасности человека.
Вопрос-ответ

Чем опасна реакция разбавленной серной кислоты с металлами?
Реакция разбавленной серной кислоты с металлами может быть опасна из-за образования газообразного продукта. При взаимодействии кислоты с металлами освобождается водород, который является горючим и может образовывать взрывоопасные смеси с воздухом.
Почему при реакции разбавленной серной кислоты с металлами образуется газообразный продукт?
Образование газообразного продукта при реакции разбавленной серной кислоты с металлами связано с диспропорционированием водородных ионов. Серная кислота (H2SO4) содержит в себе ионы H+ и SO4 2-. При контакте с металлом, ионы H+ отдают свои электроны, образуя молекулы водорода (H2), тогда как ионы SO4 2- соединяются с металлом, формируя соли серной кислоты.
Какие металлы реагируют с разбавленной серной кислотой?
Разбавленная серная кислота может реагировать с различными металлами, в том числе с цинком (Zn), железом (Fe), медью (Cu), свинцом (Pb), алюминием (Al) и многими другими. Реакция происходит из-за того, что эти металлы обладают достаточным потенциалом для отдачи электронов и образования соответствующих ионов.
