Железо - химический элемент, который имеет высокую реакционность с большинством кислот. Однако при разбавлении кислот свойства железа могут изменяться. В данной статье мы рассмотрим отсутствие реакции железа с разбавленными кислотами и причины этого явления.
Железо обычно реагирует с кислородом воздуха, образуя ржавчину, и сильно взаимодействует с сильными кислотами, такими как серная и соляная. Однако, когда кислоты разбавляются водой, их реакционная способность снижается, что влияет на реакцию с железом. Разбавленные кислоты становятся менее активными, и это может приводить к отсутствию реакции с железом.
Значительное влияние на отсутствие реакции железа с разбавленными кислотами оказывает также концентрация кислоты. Чем более разбавлена кислота, тем меньшее количество ионоизированных частиц содержится в растворе, что влияет на химическую реакцию с железом. При низкой концентрации ионов кислоты реакция между железом и разбавленными кислотами может быть практически незаметной.
Влияние разбавленных кислот на реакцию железа
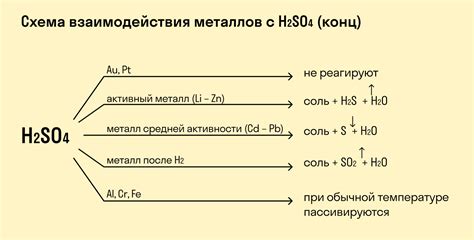
Железо – это химический элемент, который имеет отношение к группе переходных металлов. Оно является одним из самых распространенных элементов на земле, и его соединения широко используются в различных отраслях промышленности.
Взаимодействие железа с кислотами является важным аспектом его химических свойств. Кислоты могут иметь разную концентрацию и разбавленные кислоты могут оказывать разное влияние на реакцию железа.
При взаимодействии железа с разбавленными кислотами, такими как разбавленная серная кислота или разбавленная соляная кислота, происходит образование соответствующих солей и выделение водорода. Эти реакции характеризуются образованием пузырьков газа и изменением цвета раствора.
Однако, реакция железа с разбавленными кислотами происходит медленно и не так эффективно, как с концентрированными кислотами. Это связано с тем, что разбавленные кислоты обладают значительно меньшей концентрацией активных ионов, что снижает скорость реакции. Кроме того, разбавленные кислоты также могут образовывать защитные слои оксидов или солей на поверхности железа, что замедляет реакцию.
В целом, разбавленные кислоты оказывают ограниченное влияние на реакцию железа. Для более интенсивного процесса растворения железа рекомендуется использовать концентрированные кислоты или иные методы обработки.
Физические свойства железа
Железо – один из самых распространенных и широко используемых металлов в мире. Оно обладает рядом уникальных физических свойств, которые делают его ценным материалом в различных отраслях промышленности.
Магнитные свойства. Железо является ферромагнитным металлом, то есть способным притягиваться к магнитному полю. Это свойство позволяет использовать его в производстве постоянных магнитов, электромагнитов и других устройств, связанных с магнитизмом.
Пластичность. Железо отличается высокой пластичностью, что позволяет легко давить, катать, вытягивать и прочностной обрабатывать этот металл. Благодаря этому свойству железо широко используется в ковке, горячей и холодной штамповке, листовой прокатке, а также во многих других процессах формообразования.
Теплопроводность. Железо обладает высокой теплопроводностью, что делает его прекрасным материалом для передачи тепла и использования в системах отопления, охлаждения и кондиционирования воздуха. Также благодаря этому свойству железо широко используется в изготовлении кастрюль, сковородок и другой посуды для приготовления пищи.
Электропроводность. Железо является хорошим электропроводником и используется в производстве проводов, кабелей и электротехнической арматуры. Благодаря своим электрическим свойствам, оно также применяется в производстве электромоторов и трансформаторов.
Биохимический аспект взаимодействия железа с кислотами

Железо играет важную роль в биохимических процессах организма, так как является неотъемлемой частью многих ферментов и белков. Однако взаимодействие железа с кислотами может иметь определенные особенности.
Разбавленные кислоты, такие как соляная кислота или уксусная кислота, обычно не вызывают значительной реакции с железом. Это объясняется тем, что железо в чистом состоянии обладает покровной пленкой оксида, которая защищает его от агрессивных действий кислот. Таким образом, оно остается стабильным и не растворяется в разбавленных кислотных растворах.
Однако, когда кислота имеет достаточно высокую концентрацию и агрессивность, она может проникать через пленку оксида и начинать реагировать с железом. Это может привести к образованию солей железа, таких как хлорид железа (III) или сульфат железа (II). Такие соли могут вызывать различные химические реакции в организме человека или других организмах. Кроме того, при реакции железа с кислотами может выделяться водород.
Биохимический аспект взаимодействия железа с кислотами имеет большое значение для понимания процессов, происходящих в организме. Например, понимание того, как кислые условия могут влиять на активность ферментов, содержащих железо, позволяет лучше понять механизмы метаболических процессов и разработать эффективные методы лечения различных заболеваний.
Причины отсутствия реакции между разбавленными кислотами и железом

1. Защитная оксидная пленка
Одной из главных причин отсутствия реакции между разбавленными кислотами и железом является защитная оксидная пленка, которая образуется на поверхности металла при контакте с воздухом. Эта пленка состоит в основном из оксида железа (III) - Fe2O3, который нерастворим в большинстве разбавленных кислот.
2. Устойчивость оксидной пленки
Оксидная пленка очень устойчива и не дает разбавленным кислотам проникнуть до металлической поверхности железа. Благодаря этой пленке, железо не окисляется и не реагирует с кислотами. Это позволяет предотвратить негативные химические процессы, которые могли бы привести к разрушению металла.
3. Инертность разбавленных кислот
Разбавленные кислоты, такие как серная кислота и соляная кислота, обладают невысокой активностью и не обладают достаточной агрессивностью, чтобы проникнуть через оксидную пленку и совершить реакцию с железом. Они могут реагировать с более активными металлами, но не с железом.
4. Потенциал окислительно-восстановительных свойств
Железо обладает достаточно низким потенциалом окислительно-восстановительных свойств, что также способствует его инертности к разбавленным кислотам. Это означает, что железо не обладает достаточной активностью, чтобы поступать в окислительно-восстановительные реакции с кислотами.
В целом, оксидная пленка, устойчивость, невысокая активность разбавленных кислот и низкий потенциал окислительно-восстановительных свойств железа, являются основными причинами отсутствия реакции между этим металлом и разбавленными кислотами.
Вопрос-ответ

Почему железо не реагирует с разбавленными кислотами?
Железо не реагирует с разбавленными кислотами из-за образования плотной пассивной пленки оксида железа на его поверхности, которая предотвращает дальнейшую реакцию с кислотой.
Какую пленку образует железо при взаимодействии с кислотами?
Железо образует пассивную пленку оксида железа (Fe2O3), которая предотвращает дальнейшую реакцию железа с кислотой. Пленка является защитной и обладает хорошей адгезией к поверхности металла.
Какой процесс происходит при образовании пассивной пленки?
Образование пассивной пленки на поверхности железа происходит благодаря реакции между железом и окислителем (кислотой). При этом происходит окисление железа, образуется оксид железа, который затем реагирует с водой, образуя гидроксид железа. Затем гидроксид железа окисляется окислителем, образуя оксид железа, который и является пассивной пленкой.
Возможно ли растворение пассивной пленки оксида железа?
Пассивная пленка оксида железа может быть растворена сильнокислотными растворами или в присутствии окислителей. В таких условиях пленка разрушается, и реакция между железом и кислотой становится возможной.
