Фосфаты металлов являются важными соединениями, которые находят широкое применение в различных областях науки и техники. Они обладают уникальными свойствами и могут использоваться как катализаторы, стабилизаторы, противокоррозионные и антибактериальные добавки.
Наиболее распространенными фосфатами металлов являются фосфаты натрия, кальция и алюминия. Формулы этих соединений определяются наличием группы атомов остатка, которая представляет собой совокупность атомов фосфора, кислорода и других элементов.
Фосфат натрия имеет формулу Na3PO4. Он является белым кристаллическим соединением, которое хорошо растворяется в воде. Этот фосфат широко используется в пищевой промышленности, медицине и других отраслях народного хозяйства.
Фосфат кальция обладает формулой Ca3(PO4)2. Это белый порошок, плохо растворимый в воде. Он является важным компонентом костной ткани и используется в производстве медицинских препаратов, удобрений и косметических средств.
Фосфат алюминия имеет формулу AlPO4. Это белый аморфный порошок, который легко растворяется в кислотах. Этот фосфат применяется в производстве керамики, электроники, а также используется в качестве катализатора в химической промышленности.
Фосфаты металлов

Фосфаты металлов представляют собой химические соединения, состоящие из ионов металла и фосфатного иона. Фосфатные ионы обладают отрицательным зарядом, а металлы - положительным. Именно такое сочетание зарядов позволяет создавать стабильные фосфатные соединения.
Один из наиболее распространенных фосфатов металлов - фосфат натрия (Na3PO4). Он обладает высокой прочностью и стабильностью, а также хорошо растворяется в воде. Фосфат натрия широко используется в производстве моющих средств, удобрений и керамики.
Фосфат кальция (Ca3(PO4)2) - еще один важный фосфат металла. Он представляет собой основной компонент костной ткани и зубов. Фосфат кальция также используется в медицине для производства лекарственных препаратов, а также в пищевой промышленности в качестве добавки E341.
Фосфат алюминия (AlPO4) - обладает высокой устойчивостью в кислых средах и является одним из основных компонентов алюминиевых соляных растворов. Фосфат алюминия часто используется в производстве фармацевтических препаратов, красителей и антикоррозионных покрытий.
В заключение, фосфаты металлов являются важными химическими соединениями, которые находят широкое применение в различных отраслях промышленности и медицине. Они обладают высокой прочностью, стабильностью и различными полезными свойствами, которые делают их незаменимыми во многих процессах и продуктах.
Формулы фосфатов натрия
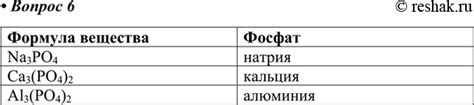
Фосфаты натрия представляют собой химические соединения, состоящие из атомов натрия и фосфата. Фосфаты натрия широко используются в различных отраслях промышленности и науки.
Одним из наиболее распространенных фосфатов натрия является фосфат натрия двухсложный (Na2HPO4), также известный как соли натрия фосфорной кислоты или дигидроортофосфат натрия. Формула указывает на наличие двух атомов натрия (Na), одного атома фосфора (P) и четырех атомов кислорода (O).
Другой важный фосфат натрия - фосфат натрия моноосновный (NaH2PO4), который может быть получен путем нейтрализации фосфорной кислоты натриевой гидроксидом. Формула этого фосфата указывает на наличие одного атома натрия (Na), двух атомов водорода (H), одного атома фосфора (P) и четырех атомов кислорода (O).
Кроме того, существуют фосфаты натрия более высокой степени окисления, такие как триосновный фосфат натрия (Na3PO4) и тетраосновный фосфат натрия (Na4P2O7). Формулы этих соединений указывают на наличие соответственно трех и четырех атомов натрия (Na), одного или двух атомов фосфора (P) и семи или двенадцати атомов кислорода (O).
Формулы фосфатов кальция
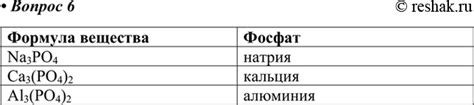
Фосфат кальция (Ca3(PO4)2) является одним из наиболее распространенных фосфатов, которые образуются при взаимодействии кальция и фосфата. Он обладает структурой, в которой две группы атомов остатка фосфата связаны с тремя ионами кальция. Такая структура позволяет фосфату кальция образовывать кристаллы и быть прочным и твердым материалом.
Фосфат кальция имеет широкий спектр применений. Он используется как пищевая добавка в продуктах, чтобы обеспечить организм кальцием и фосфором. Также его применяют в медицине, где его свойства поддерживать здоровье костей используют для лечения остеопороза и других заболеваний скелетной системы. Благодаря своей нерастворимости в воде, фосфат кальция также применяется в фармацевтической промышленности для создания пролонгированных формул лекарственных препаратов.
Кроме того, фосфат кальция широко используется в сельском хозяйстве в качестве удобрения. Вношение фосфатов в почву позволяет увеличить содержание фосфора, которое является необходимым элементом для роста и развития растений. Фосфат кальция долгое время сохраняет свою активность, поэтому его применение дает стабильный и долгосрочный эффект в повышении урожайности.
Итак, формула фосфата кальция (Ca3(PO4)2) отображает его химическую структуру, состоящую из трех ионов кальция и двух групп атомов остатка фосфата. Этот соединение широко используется в различных отраслях, таких как пищевая промышленность, медицина и сельское хозяйство, благодаря своим свойствам и способности обеспечивать необходимый организму кальций и фосфор.
Формулы фосфатов алюминия
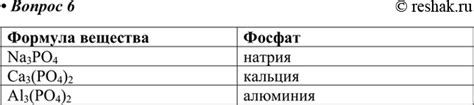
Фосфаты алюминия представляют собой химические соединения, состоящие из алюминия и фосфата. Формула фосфата алюминия зависит от соотношения атомов фосфата и алюминия в соединении.
Одним из наиболее распространенных фосфатов алюминия является трехосный фосфат алюминия, обозначаемый формулой AlPO4. В этом соединении каждый атом алюминия соединен с тремя атомами фосфора и образует кристаллическую решетку.
Другим видом фосфата алюминия является гидратный фосфат алюминия, обозначаемый формулой AlPO4 · 2H2O. В этом соединении к алюминию и фосфату добавлены молекулы воды, которые участвуют в образовании кристаллической структуры.
Также существуют различные участки, на которых атомы алюминия и фосфата могут занимать разные позиции в кристаллической решетке, что влияет на свойства фосфата алюминия.
Фосфаты алюминия находят широкое применение в различных отраслях, таких как строительство, катализ, пищевая промышленность и другие. Изучение и получение различных форм фосфатов алюминия является актуальной задачей современной материаловедения.
Группа атомов остатка

Группа атомов остатка представляет собой набор атомов, которые остаются после отщепления всех атомов из соединения за исключением атома кислорода. Группа атомов остатка играет важную роль в составе фосфатов металлов натрия, кальция и алюминия, определяя их свойства и реакции.
В фосфатах металлов натрия, кальция и алюминия группа атомов остатка представлена фосфорной кислотой, H3PO4. Отщепление трех молекул воды приводит к образованию основного остатка, который определяет щелочные свойства данных соединений.
Участвуя в реакциях, группа атомов остатка в фосфатах проявляет свою кислотность, образуя соли с щелочами и основаниями. Эти соли являются важными компонентами в промышленности, медицине и сельском хозяйстве.
Использование группы атомов остатка в составе фосфатов металлов натрия, кальция и алюминия позволяет создавать материалы с различными свойствами, такие как устойчивость к высоким температурам, электропроводность, адгезия и другие. Такие материалы находят применение в промышленности строительных материалов, керамики, лакокрасочных покрытий и других отраслях производства.
Вопрос-ответ

Какие формулы фосфатов металлов существуют?
Существует множество фосфатов металлов, но наиболее распространены формулы фосфатов натрия, кальция и алюминия с группой атомов остатка
Какая формула фосфата натрия?
Формула фосфата натрия Na3PO4
