Растворы металлов - это особый вид химических растворов, в которых металлические ионы находятся в расплавленном или растворенном состоянии. Задачи, связанные с растворами металлов, являются важной частью изучения химии и неотъемлемой частью практического применения металлов.
Одной из основных задач, связанных с растворами металлов, является расчёт концентрации металлических ионов в растворе. Для этого необходимо знать массу металла, количество растворителя и несколько других параметров. Решение таких задач требует применения различных формул и уравнений, что позволяет определить не только концентрацию раствора, но и его плотность, электропроводность и другие физические свойства.
Другой важной задачей, связанной с растворами металлов, является определение растворимости металлических солей. Здесь важно знать, какие факторы влияют на растворимость, какие методы измерения используются и какие физические процессы происходят при образовании раствора. Решение таких задач позволяет прогнозировать поведение металлических солей в различных условиях и оптимизировать их применение в различных областях науки и техники.
Определение понятия "растворы металлы"

Растворы металлы - это гомогенные смеси, состоящие из двух или более металлических элементов. В таких растворах один металл находится в кристаллической решетке другого металла. Важным свойством растворов металлов является их способность образовывать сплавы, то есть гомогенные смеси металлических элементов.
Растворы металлы широко применяются в различных областях промышленности и науки. Они играют важную роль в металлургии, электротехнике, специальных технологиях и других отраслях. Например, сплавы на основе растворов металлов применяются в производстве прочных и легких материалов для авиации и автомобилестроения.
Одним из ключевых понятий в растворах металлов является растворимость. Растворимость металлов может быть разной и зависит от многих факторов, включая температуру, давление и наличие других веществ в растворе. Изучение растворимости металлов позволяет предсказывать и контролировать их взаимодействия и свойства в различных условиях.
Для анализа растворов металлов используются различные методы и приборы, такие как спектрометры, хронометры, вискозиметры и другие. Эти методы позволяют определить концентрацию металлов в растворе, исследовать их физические и химические свойства, а также проводить эксперименты для получения новых материалов с улучшенными характеристиками.
Свойства растворов металлы

Растворы металлов представляют собой химические соединения, в которых металлы находятся в ионной форме. Одним из важных свойств растворов металлов является электропроводность. Металлы обладают высокой электропроводностью, поэтому растворы металлов также являются хорошими проводниками электрического тока.
Еще одним важным свойством растворов металлов является их способность к образованию гальванических элементов. Металлы различными способами могут образовывать электрохимические клетки, в которых происходят химические реакции. Это свойство находит применение в производстве батарей и аккумуляторов.
Растворы металлов также обладают способностью к каталитическим реакциям. Металлы могут ускорять or замедлять химические превращения без изменения своего состояния. Это свойство широко используется в промышленности при производстве различных химических соединений.
Растворы металлов имеют также специфические свойства, которые обусловлены характеристиками каждого конкретного металла. Например, растворы железа могут обладать окрашивающими свойствами, а растворы меди - противокоррозионными. Такие свойства металлов находят применение в различных отраслях промышленности, в том числе в производстве красок, лаков и покрытий.
Таким образом, растворы металлов обладают рядом уникальных свойств, которые находят применение в различных сферах научных и промышленных исследований. Эти свойства делают растворы металлов важными объектами изучения в области химии и материаловедения.
Подраздел 1
Растворы металлов - это смеси, в которых металлы находятся в ионной форме. Однако, в отличие от растворов солей, растворы металлов обладают своими особенностями. Вместе с тем, растворы металлов широко используются в различных областях, таких как металлургия, электротехника, химическая промышленность и другие.
Типы растворов металлов:
- Электролитические растворы - это растворы, полученные путем растворения металлов в водных растворителях при помощи электролиза. Эти растворы играют важную роль в электротехнике и гальванотехнике, например, в процессе гальванического покрытия.
- Сплавы - это растворы металлов друг в друге при определенных условиях. Сплавы могут иметь различные свойства и применяются для создания различных материалов, таких как металлические сплавы, цветные сплавы и др.
- Металлические растворы - это растворы, в которых один металл полностью растворен в другом металле. Такие растворы широко используются в металлургии и машиностроении для изменения свойств материала.
Также стоит отметить, что растворы металлов имеют такие характеристики, как проводимость электрического тока, теплопроводность и активность. Эти свойства делают растворы металлов полезными во многих процессах и технологиях.
Растворимость металлов в воде
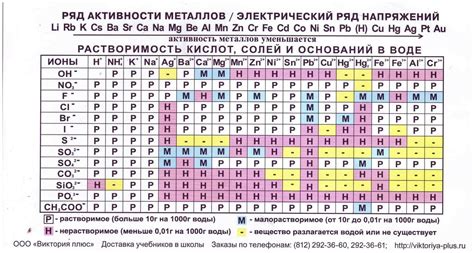
Металлы могут быть растворимыми или нерастворимыми в воде в зависимости от своих физических и химических свойств. Растворимость металлов в воде может быть полной или частичной, а иногда металлы могут быть совсем не растворимы.
Многие металлы обладают высокой растворимостью в воде. Некоторые из них, такие как натрий, калий и магний, растворяются полностью и образуют ионные растворы. Эти металлы обычно находятся в виде катионов в растворе и играют важную роль в регуляции гидроэлектролитного равновесия в организмах живых организмов.
Однако существуют также металлы, которые практически не растворимы в воде. К ним относятся, например, серебро, золото и платина. Эти металлы имеют низкую растворимость в воде и в растворе образуются только незначительные количества положительных ионов. Именно из-за этой низкой растворимости они часто используются для изготовления украшений и ювелирных изделий.
Растворимость металлов в воде зависит от ряда факторов, таких как температура, pH раствора и наличие других химических веществ. Например, некоторые металлы могут быть растворимыми при определенном pH, но нерастворимыми при другом. Также некоторые металлы могут образовывать сложные соединения с другими веществами, что может повлиять на их растворимость.
Подраздел 2
Механизм образования растворов металлов
Образование растворов металлов происходит благодаря взаимодействию металла с растворителем. Ключевым фактором, влияющим на способность металла растворяться, является его химическая активность. Чем выше активность металла, тем проще он растворяется в растворителе.
Металлы могут растворяться как полностью, так и частично. Полное растворение металла происходит, когда он полностью вступает в химическую реакцию с растворителем и ионы металла полностью диссоциируют в растворе. Частичное растворение металла происходит, когда только некоторая его часть реагирует с растворителем и образует ионы металла в растворе.
Образование растворов металлов может происходить различными способами, включая химические и электрохимические реакции. В результате взаимодействия металла с растворителем образуется комплексный ионный соединение, которое растворяется в растворе.
На образование растворов металлов также могут влиять другие факторы, такие как температура, давление, pH-значение раствора и наличие других химических веществ. Кроме того, некоторые металлы могут образовывать амальгамы при взаимодействии с ртутью, что также является одним из способов образования растворов металлов.
Образование и свойства сплавов

Сплавы - это материалы, получаемые путем смешивания двух или более металлов. Образование сплавов может происходить при плавлении отдельных металлов в определенных пропорциях. При этом атомы одного металла встраиваются в решетку атомов другого металла, образуя новую кристаллическую структуру.
Свойства сплавов зависят от состава и структуры материала. В связи с этим сплавы могут обладать различными свойствами, которые находят широкое применение в различных отраслях промышленности. Например, сплавы могут быть прочнее, более твердыми или иметь специальные физические и химические свойства.
Одним из важных свойств сплавов является их пластичность. Благодаря этому свойству сплавы легко поддаются обработке и формовке, что позволяет их использовать для создания сложных деталей и изделий. Кроме того, сплавы могут быть устойчивыми к коррозии, что делает их эффективными для использования в условиях высокой влажности или агрессивных сред.
Еще одним важным свойством сплавов является их температурная стойкость. Некоторые сплавы способны сохранять свои свойства при высоких температурах, что позволяет им использоваться в производстве котлов, турбин и других устройств, работающих при повышенных температурах.
Подраздел 3: Определение концентрации растворов металлов

Определение концентрации растворов металлов является важным этапом в химическом анализе. Концентрация раствора - это количество вещества, содержащегося в единице объема раствора.
Для определения концентрации раствора металлов существует несколько методов. Один из них - гравиметрический метод. При его использовании основной принцип заключается в осаждении или выпадении твердого вещества из раствора, после чего массу осадка измеряют и вычисляют концентрацию раствора.
Другим способом определения концентрации растворов металлов является волюметрический метод. При этом методе раствор металла титруют раствором титранта, содержащим вещество, реагирующее с металлом. Измеряют объем титранта, необходимый для полного реагирования с металлом, и на основе этого вычисляют концентрацию металла в исходном растворе.
Реакции металлов с кислотами

Реакции металлов с кислотами являются одной из основных реакций в химии. Кислоты, обладающие кислотными свойствами, способны образовывать с металлами соли и выделять водород. Реакции с металлами происходят благодаря химическому взаимодействию между ионами металла и ионами водорода кислоты.
Металлы, обладающие большей степенью активности, реагируют с кислотами более интенсивно. Например, щелочные металлы, такие как натрий и калий, реагируют с водой с образованием гидроксидов и выделением водорода. Некоторые металлы, такие как цинк и железо, реагируют с соляной кислотой и образуют соли металлов и выделяют водород.
Реактивность металлов с кислотами зависит от их электрохимического потенциала. Чем больше потенциал у металла, тем он более активен и реактивен будет реагировать с кислотами. Металлы могут реагировать не только с сильными минеральными кислотами, но и с органическими кислотами, такими как уксусная и яблочная кислота.
Реакц
Подраздел 4

В данном подразделе рассматривается вопрос о свойствах растворов металлов, а именно их электропроводности.
Растворы металлов относятся к типу проводящих растворов, то есть они способны проводить электрический ток.
Это связано с наличием в растворе свободных электронов, которые перемещаются под воздействием электрического поля.
Свойства электропроводности растворов металлов зависят от их концентрации и состава.
Чем больше концентрация металла в растворе, тем выше электропроводность.
Также влияние на свойства растворов металлов оказывает ионный состав, то есть тип металла и ионы, которые образуются при диссоциации металлического соединения.
Электропроводность растворов металлов может быть измерена с помощью проводимости.
Проводимость раствора зависит от его электропроводности и концентрации металла.
Электропроводность измеряется в см/см и может быть вычислена по формуле проводимости, где L - длина раствора, S - его площадь поперечного сечения, R - сопротивление раствора.
Таким образом, проведение эксперимента по измерению электропроводности позволяет определить основные свойства растворов металлов и их поведение в электрическом поле.
Металлы в растворах солей

Металлы в растворах солей представляют собой ионы положительного заряда, которые возникают в результате химической реакции между металлами и кислотами. В растворах солей металлы проявляют определенные свойства, которые определяют их химическую активность и возможности в различных реакциях.
Один из главных факторов, влияющих на поведение металлов в растворах солей, - это их атомный радиус. Атомный радиус определяет размер ионов в растворе и влияет на их взаимодействие с другими частицами. От размера иона зависит его способность к образованию комплексов и реактивность в растворе.
Металлы в растворах солей могут также образовывать осадки, когда раствор становится насыщенным и ионы металла начинают выпадать в виде нерастворимых соединений. Такие осадки могут быть различной природы и их образование зависит от взаимодействия ионов металла с анионами, содержащимися в растворе.
Важным свойством металлов в растворах солей является их потенциал окисления - способность отдавать электроны. В реакциях окисления-восстановления металлы могут выступать в роли окислителей или восстановителей, что позволяет им участвовать в различных химических процессах.
Вопрос-ответ

Что такое растворы металлов?
Растворы металлов - это смеси, в которых металл находится в растворенном состоянии в другом веществе. Они обладают специфическими свойствами и используются в различных областях, включая промышленность, электроэнергетику и науку.
Какие виды растворов металлов существуют?
Существует несколько видов растворов металлов. Один из них - растворы металлов в жидких металлах, где металл растворяется в другом металле. Еще одним типом растворов металлов являются растворы металлов в воде, где металл растворяется в воде. Также существуют растворы металлов в органических растворителях, где металл растворяется в органическом растворителе.
Какие свойства имеют растворы металлов?
Растворы металлов имеют ряд специфических свойств. Они обладают хорошей электропроводностью из-за наличия в них ионов металла. Кроме того, растворы металлов обладают высокой теплопроводностью и могут быть магнитными в зависимости от свойств растворенного металла и растворителя. Они также могут обладать специфическими физико-химическими свойствами, такими как растворимость и степень окисления металла.
