Хлор (Cl) - это один из самых известных элементов в периодической системе. Он находится в плохих положениях, поскольку его классификация вызывает дебаты и неоднозначность. В данной статье мы рассмотрим аргументы, которые поддерживают оба варианта: хлор может быть как неметаллом, так и металлом.
С одной стороны, хлор может быть рассмотрен как неметалл. Он относится к группе галогенов в периодической системе и имеет характерные свойства неметаллов: низкую температуру плавления и кипения, электроотрицательность и склонность к образованию отрицательных ионов. Хлор является крайне реактивным веществом и образует соединения с другими элементами, в основном, с металлами. Эти свойства говорят в пользу его неметаллической природы.
С другой стороны, хлор также имеет некоторые свойства, которые могут быть характерны для металлов. Например, хлор обладает положительным окислительным потенциалом, может образовывать положительные ионы и часто ведет себя как окислитель. Кроме того, хлор имеет способность образовывать комплексные соединения с другими элементами, подобно металлам. Эти свойства говорят в пользу его металлической природы.
В целом, классификация хлора как неметалла или металла остается предметом научных дискуссий. Очевидно, что данный элемент имеет свойства, которые сочетают черты обоих классов. Возможно, дальнейшие исследования и открытия проложат путь к более точному определению природы хлора и помогут урегулировать дебаты по этому вопросу.
Химическая свойства хлора: неметалл или металл?

Хлор - химический элемент симли, который находится в 17 группе периодической системы элементов. Он имеет атомный номер 17 и обозначается символом Cl.
Хлор является неметаллом и проявляет типичные химические свойства данной группы элементов. Неметаллы, в отличие от металлов, обычно образуют газообразные или нетвердые вещества с низкой плотностью и температурой плавления.
Хлор обладает такими химическими свойствами, как высокая электроотрицательность, способность образовывать летучие соединения и сильную агрессивность в отношении железа и других металлов. Он реагирует со многими другими элементами, образуя различные химические соединения.
Хлор широко используется в промышленности и быту. Он является важным компонентом многих химических веществ, в том числе солей, кислот и оснований. Хлор также используется для дезинфекции воды и обработки питьевой воды.
Итак, хлор - неметалл, проявляющий характерные химические свойства данной группы элементов. Его высокая реактивность и широкое использование делают его важным и неотъемлемым компонентом в различных сферах жизни человека.
История открытия хлора и его место в Периодической системе

Хлор - один из самых известных химических элементов, который обладает ярко выраженными химическими свойствами. История открытия хлора насчитывает несколько веков и тесно связана с развитием науки и химии.
Первые упоминания о существовании хлора встречаются в древних греческих и римских источниках, где он описывается как отравляющий и едкий газ. Однако настоящее открытие и изучение химических свойств хлора началось только в XVIII веке.
В 1774 году шведский химик Карл Вильгельм Шеле открыл хлоровистоводородную кислоту, которая стала первым соединением, из которого удалось получить хлор. Следующий важный этап в истории хлора произошел в 1810 году, когда химик Джозеф Гейлуссакер получил хлор в чистом виде путем электролиза раствора хлористого калия.
Не смотря на то, что ранее хлор принимался как неметалл, в настоящее время он относится к халогенам и занимает седьмое место в Периодической системе Д.И.Менделеева. Позиция хлора в Периодической системе определена его атомным номером (17) и химическими свойствами. Хлор обладает выраженной окислительной и вытесняющей активностью, что делает его важным элементом в различных процессах и химических реакциях.
Физические свойства хлора и его состояние при комнатной температуре
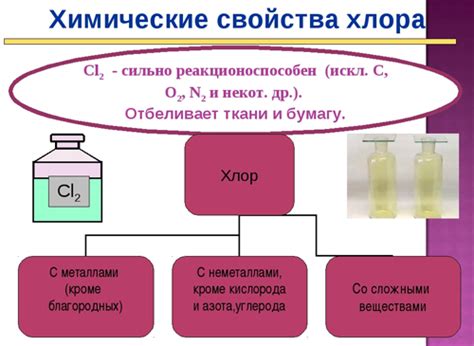
Хлор (Cl) - это неметаллический химический элемент из группы галогенов с атомным номером 17. Он имеет ярко-желтый цвет и обладает рядом характерных физических свойств.
Хлор при комнатной температуре и нормальном давлении находится в газообразном состоянии. Его плавление происходит при температуре -101,5 °С, а кипение при температуре -34,04 °С. Приобретая жидкое состояние, хлор образует ярко-желто-зеленую жидкость.
Хлор обладает сильным характеристическим запахом, напоминающим запах отбеливателя. Этот газ очень токсичен и ядовит, поэтому при работе или контакте с ним необходимо соблюдать соответствующие меры предосторожности.
Хлор обладает высокой растворимостью в воде и может образовывать с ней гипо- и хлороводородные кислоты. Он также реагирует с большинством органических и неорганических веществ, образуя хлориды и другие соединения.
В природе хлор встречается либо в свободной форме, либо в виде минералов, таких как хлориды или хлоркалий. Он широко используется в промышленности в качестве дезинфицирующего средства, отбеливателя, противоодорного средства и в производстве различных химических соединений.
Химические свойства хлора и его реакции с другими веществами
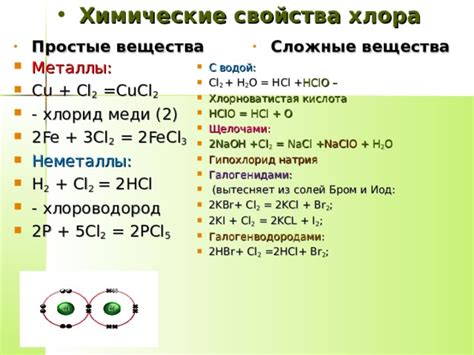
Хлор (Cl2) – ярко-желтый газ, который обладает характерным запахом. Он является одним из самых активных элементов в химии. Хлор обладает разнообразными свойствами и способен взаимодействовать с большим количеством веществ.
Хлор – хороший окислитель и встречается во многих окислительно-восстановительных реакциях. Он может окислять различные вещества, образуя соединения с более низкой степенью окисления.
С водородом хлор формирует соляную кислоту (HCl). Это одна из самых важных реакций хлора, поскольку соляная кислота широко используется в промышленности, медицине и других отраслях. Реакция происходит по следующему уравнению: Cl2 + H2 → 2HCl
Хлор также может реагировать с многими металлами, образуя хлориды. Например, с натрием хлор образует натрий хлорид (NaCl), наиболее известную соль. Эта реакция имеет место по уравнению: Cl2 + 2Na → 2NaCl
Хлор реагирует с органическими соединениями, такими как углеводороды, алкены и алканы. При этом образуются хлорированные продукты. Например, реакция хлора с метаном (CH4) приводит к образованию хлорметана (CH3Cl), хлорэтана (C2H5Cl) и других хлорированных соединений.
Хлор может реагировать с некоторыми элементами, образуя сложные соединения. Например, с серой хлор формирует хлорид серы (S2Cl2), который используется в процессах химического синтеза и получения других соединений.
Кроме того, хлор может взаимодействовать с кислородом, образуя оксигалогены. Например, реакция хлора с кислородом приводит к образованию хлората (ClO3-) и хлорита (ClO2-).
Хлор является важным компонентом многих химических процессов и обладает широким спектром химических свойств. Его реактивность и способность взаимодействовать с различными веществами делают его неотъемлемой частью химической промышленности и науки.
Применение хлора в промышленности и быту

Хлор является важным компонентом в различных отраслях промышленности, а также находит широкое применение в быту.
В промышленности хлор используется в процессе производства многих химических продуктов. Он является основным сырьем при производстве пластмасс, резины, каучука, а также в процессе обработки и очистки металлов. Также хлор используется в производстве хлорированного поливинилхлорида (ПВХ) - одного из наиболее распространенных видов пластиков.
В быту хлор применяется для улучшения качества питьевой воды. Он используется для дезинфекции и очистки воды от бактерий и вирусов. Хлор также применяется в процессе беления и отбеливания тканей, бумаги и других материалов. Благодаря своим дезинфицирующим свойствам, хлор также широко используется в производстве моющих средств, дезинфицирующих средств и отбеливателей для очистки и поддержания гигиены в доме.
Однако, несмотря на широкое применение хлора в промышленности и быту, его использование требует осторожности, так как хлор является токсичным веществом. При работе с хлором необходимо соблюдать меры безопасности и использовать защитное снаряжение.
Важность хлора для живых организмов и влияние его на окружающую среду

Хлор является неметаллом, но его роль в живых организмах невероятно важна. Во-первых, хлор является необходимым элементом в составе соли, которая является основным источником хлоридов в организме. Хлориды, в свою очередь, играют важную роль в биохимических процессах, таких как образование желудочного сока, участие в метаболических реакциях и поддержание водного баланса.
Кроме того, хлор широко используется в процессе очистки воды, как питьевой, так и воды бассейнов и других водоемов. Хлор применяется для дезинфекции воды и уничтожения микроорганизмов, что способствует предотвращению распространения инфекций и защите здоровья людей.
Однако, влияние хлора на окружающую среду также имеет свои отрицательные стороны. При использовании хлора в больших количествах для очистки воды, образуются хлорорганические соединения, которые не только могут быть вредными для здоровья, но и негативно влиять на экосистемы водоемов.
Одним из основных негативных последствий использования хлора является образование трихлорметана и других хлорорганических соединений, которые могут быть канцерогенными и вредными для окружающей среды. Также, хлор может вызывать загрязнение воздуха и почвы из-за выбросов в процессе производства и использования различных хлорсодержащих веществ.
В целом, хлор является необходимым элементом для живых организмов, но его использование и влияние на окружающую среду требует более внимательного и осознанного подхода, чтобы минимизировать потенциальные негативные последствия.
Вопрос-ответ

Каковы основные свойства хлора?
Хлор – это химический элемент, относящийся к галогенам. Он является неметаллом и имеет характеристики такие, как высокая электроотрицательность, невоспламеняемость, ядовитость и сильно выраженную окислительную активность.
Почему хлор часто используется в промышленности?
Хлор широко используется в промышленности благодаря своей высокой окислительной активности. Он используется для производства многих химических веществ и материалов, таких как строительные материалы, пластмассы, резины, белизны для текстиля, и многих других продуктов и веществ.
Является ли хлор металлом или неметаллом?
Хлор является неметаллом. Он обладает основными свойствами неметаллов, включая низкую теплопроводность, невоспламеняемость и высокую электроотрицательность.
Какое значение хлора для организмов и природной среды?
Хлор имеет важное значение для организмов и природной среды. Например, хлор является необходимым элементом для живых организмов, и он играет роль в процессах дыхания, пищеварения и других биохимических процессах. Однако избыток хлора в природной среде или организме может быть вредным и даже опасным для здоровья.
