Металлы - это особый класс элементов, которые обладают рядом уникальных свойств, таких как прочность, теплопроводность и электропроводность. Для обозначения каждого отдельного металла используется химический знак, который состоит из одной или двух букв, и является сокращенным обозначением названия элемента. Эти знаки были разработаны учеными для упрощения и стандартизации обозначения элементов.
Строение атома металлов состоит из ядра и облака электронов. Ядро атома содержит протоны и нейтроны, а облако электронов вращается вокруг ядра. У металлов особенное строение атома, которое делает их особенно проводящими и сильными. В ядре металла находится большое количество протонов, что приводит к электропроводности материала. Облако электронов, в свою очередь, обеспечивает металлы своей характерной металлической блеской и прочностью.
Кроме химического знака и строения атома, металлы обладают еще рядом других уникальных свойств. В частности, они обладают высокой теплопроводностью, что позволяет им эффективно передавать тепло. Благодаря этому свойству, металлы используются в различных областях, таких как строительство, электротехника, их медицина и промышленность. Кроме того, металлы имеют высокую пластичность, что позволяет им быть легко обработанными и использованными в различных формах и конструкциях.
Металлы играют важную роль в нашей жизни и обладают множеством уникальных свойств. Использование их химических знаков и понимание строения атома позволяет ученым и инженерам разрабатывать новые материалы и улучшать существующие технологии.
Химический знак и строение атома металлов

Химический знак металлов является графическим обозначением элемента и используется в химических уравнениях и формулах для обозначения атомов металлов. Химический знак представляет собой упрощенное обозначение элемента и состоит из одной или двух букв, которые являются символом элемента в периодической системе Д.И. Менделеева.
Строение атома металлов включает в себя ядро и электронную оболочку. Ядро атома состоит из протонов и нейтронов, а электронная оболочка содержит электроны. Протоны имеют положительный заряд, нейтроны не имеют заряда, а электроны имеют отрицательный заряд. В металлах число протонов в ядре обычно равно числу электронов, что делает атом металла нейтральным по заряду.
Металлы обладают определенными свойствами и характеристиками, которые связаны с их строением атома. Например, электроны в металлических атомах образуют так называемую "электронную облако", которое характеризуется свободным перемещением электронов. Это объясняет высокую проводимость электричества и тепла у металлов.
Еще одним важным свойством металлов, связанным со строением их атомов, является их способность образовывать ионные соединения. Металлы обычно имеют низкую электроотрицательность и легко отдают электроны другим элементам, образуя положительно заряженные ионы.
- Металлы имеют благородную и электропроводную структуру атома.
- Атомы металлов обычно имеют малую связанную энергию электронов.
- В металлах электроны связаны слабо и способны легко перемещаться.
- Металлы могут образовывать ионные соединения с неметаллами.
Основные принципы
Химический знак – символ, используемый для обозначения химического элемента. Он является сокращенным обозначением имени элемента на латинском языке или сокращением латинского названия.
Строение атома металлов основано на модели атома, предложенной нуклеарным физиком Эрнестом Резерфордом. Согласно этой модели, атом состоит из положительно заряженного ядра, вокруг которого движутся электроны по орбитам на определенном расстоянии от ядра.
Основные свойства атомов металлов связаны с их электронной структурой. Металлы характеризуются высокой электропроводностью, пластичностью, тугоплавкостью и блеском. Эти свойства обусловлены наличием свободных электронов в валентной оболочке металла.
Очень сильная металлическая связь обеспечивает высокую температуру плавления металлов. При нагревании атомы металла начинают двигаться с большой скоростью, но при этом остаются связанными благодаря сильным электростатическим притяжением между положительно заряженными ядрами и свободными электронами.
Основные свойства

Металлы - это группа химических элементов, которые обладают определенными свойствами.
Одним из основных свойств металлов является электропроводность. Большинство металлов обладают высокой проводимостью электрического тока. Это связано с наличием свободных электронов в их атомах, которые легко перемещаются под действием электрического поля.
Еще одним важным свойством металлов является теплопроводность. Металлы хорошо проводят тепло, что делает их эффективными материалами для использования в различных технических и промышленных процессах.
Также металлы обладают пластичностью и прочностью. Их атомы располагаются в решетке, которая может деформироваться без разрушения. Благодаря этому, металлы легко поддаются обработке и формованию.
Другим важным свойством металлов является блеск. Металлы, когда они находятся в чистом состоянии, обладают характерным блеском. Это связано с их способностью поглощать и отражать свет.
В целом, металлы обладают рядом уникальных свойств, которые делают их важным и неотъемлемым материалом в различных отраслях промышленности и науки.
Строение атома металлов
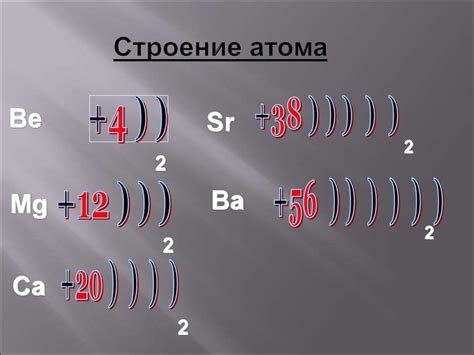
Атом металла является основным строительным блоком всех металлических материалов. Он состоит из ядра и облака электронов.
Ядро атома металла содержит нейтроны и протоны. Протоны имеют положительный заряд, а нейтроны не имеют заряда. Число протонов в ядре называется порядковым номером и определяет химический знак элемента. Например, у меди (Cu) 29 протонов в ядре.
Вокруг ядра атома металла движутся электроны. Электроны имеют отрицательный заряд и образуют электронные оболочки. Наиболее близка к ядру и наиболее энергетически стабильна первая электронная оболочка, на которой расположены 2 электрона.
Вторая и последующие электронные оболочки могут вмещать больше электронов. Общее число электронов в атоме металла равно числу протонов в ядре и определяется его порядковым номером. Например, у железа (Fe) 26 электронов.
Стабильность атома металла достигается путем заполнения электронных оболочек. Металлы стремятся получить полностью заполненные оболочки за счет обмена или передачи электронов другим атомам. Это объясняет их свойства проводить ток, быть хорошими проводниками, иметь блестящую поверхность и обладать высокой пластичностью.
Процесс образования химического знака
Химический знак – это универсальное обозначение элемента или соединения в химии. Он состоит из символов, которые отображают химический состав вещества. Процесс образования химического знака основан на принципах системы символов, разработанной Менделеевым для классификации элементов.
Каждый элемент имеет свой уникальный символ, который состоит из одной или двух латинских букв. Символы обозначают начальные буквы или первые несколько букв названия элемента на латинском языке. Некоторые символы совпадают с начальными буквами названия элемента на других языках. Например, символ для железа – Fe, от слова "ferrum" на латыни.
Комбинируя символы элементов, можно создать химический знак для соединений. Например, вода состоит из атомов водорода (H) и атомов кислорода (O), поэтому её химический знак будет H2O. Здесь цифра 2 нижним индексом указывает на количество атомов водорода.
Химический знак позволяет легко сопоставить символы с элементами и соединениями, основываясь на их атомном составе. Он является важным инструментом химиков для описания реакций, составления химических уравнений и расчета количества вещества.
Способы определения химического знака

В химии существует несколько способов определения химического знака металлов. Один из них - это использование периодической системы химических элементов. В периодической системе каждому химическому элементу соответствует уникальный символ, который называется химическим знаком. Для металлов химический знак обычно состоит из одной или двух латинских букв.
Еще одним способом определения химического знака металлов является анализ их свойств и химических реакций. Многие металлы обладают уникальными свойствами, которые позволяют их легко идентифицировать. Например, золото является блестящим, пластичным и инертным металлом, который не реагирует с кислородом и большинством химических веществ. Это позволяет легко определить его химический знак - Au.
Также для определения химического знака металлов применяется спектральный анализ. Каждый металл имеет свой специфический спектр поглощения или испускания электромагнитного излучения. С помощью спектрального анализа можно определить химический знак металла по его спектру.
Определение химического знака металлов является важным шагом в изучении их свойств и реакций. Знание химического знака позволяет установить взаимодействия металлов с другими веществами, предсказать их способность к окислению или восстановлению, а также использовать их в различных химических процессах и промышленности.
Влияние строения на свойства металлов
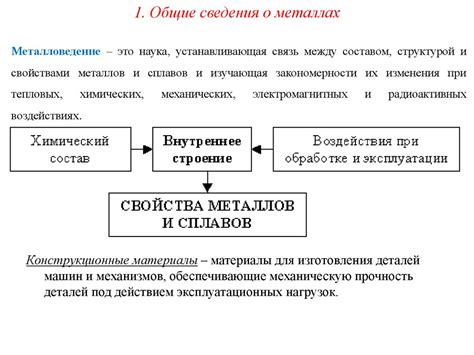
Одной из основных характеристик металлов является их кристаллическая решетка. Строение этой решетки определяет множество свойств металлов, включая их механические, электропроводность и теплопроводность.
Кристаллическая решетка металлов состоит из атомов, объединенных в металлические связи. Такие связи обладают особыми свойствами, такими как высокая прочность и пластичность. Благодаря этому металлы могут быть легко деформированы без разрушения. Такое строение решетки также позволяет металлам обладать высокими значениями тепло- и электропроводности, так как электроны в металле могут свободно двигаться по решетке.
Строение решетки также влияет на плотность металлов. Часто металлы обладают высокой плотностью из-за компактного упаковки атомов в решетке. Кристаллическое строение также влияет на оптические свойства металлов, такие как отражательная способность и цветность. К примеру, золото обладает ярким желтым цветом благодаря определенной структуре его решетки.
Взаимное расположение атомов в решетке также влияет на химическую активность металлов. Например, наличие свободных электронов в решетке делает металлы хорошими проводниками электричества и тепла, а также позволяет им легко вступать в химические реакции и образовывать соединения с другими веществами.
Вопрос-ответ

Чем отличаются химические знаки металлов от знаков других химических элементов?
Химические знаки металлов обозначаются большими буквами в латинской азбуке, в то время как знаки других химических элементов обозначаются маленькими буквами или комбинацией маленьких и больших букв.
В чем заключается основное свойство металлов?
Основное свойство металлов заключается в их способности проводить тепло и электричество.
