Железо – химический элемент с атомным номером 26. Оно является одним из самых распространенных и важных металлов в природе. Железо обладает уникальными химическими свойствами, которые определяют его широкое применение в различных областях науки и техники.
Одним из основных свойств железа является его высокая реакционная способность. Оно быстро окисляется на воздухе, образуя слой ржавчины. Эта особенность делает железо неустойчивым и требует особого внимания к его сохранению и защите от коррозии.
Железо обладает также химической активностью, что позволяет использовать его во многих синтезах и химических реакциях. Железо способно образовывать соединения с различными элементами, включая кислород, серу, азот и фосфор. Эти соединения имеют важное значение в промышленности, в частности, железные сплавы являются основой для изготовления стали.
Химические свойства железа

Железо — химический элемент из группы переходных металлов, обладающий разнообразными химическими свойствами. Важнейшими характеристиками железа являются его активность и способность образовывать реактивные соединения.
Железо относится к активным элементам и легко вступает в химические реакции. Оно реагирует с водой с образованием водорода, что является основой его коррозии. Железо также способно реагировать с кислородом из воздуха, образуя оксиды железа, такие как Fe2O3 (окись железа(III)). Это является причиной образования ржавчины на поверхности железа при длительном контакте с воздухом и влагой.
Железо способно образовывать соединения с различными элементами. Например, оно вступает в реакцию с серой и образует сульфид железа (FeS). Железо также может образовывать комплексные соединения с органическими и неорганическими лигандами, при этом образуется стабильная связь железо-лиганда.
Важным химическим свойством железа является его способность к окислительно-восстановительным реакциям. Железо может претерпевать окисление, увеличивая свою валентность, а также восстанавливаться, уменьшая ее. Это свойство используется в производстве металлургических сплавов и в электрохимических процессах.
Строение и состав железа
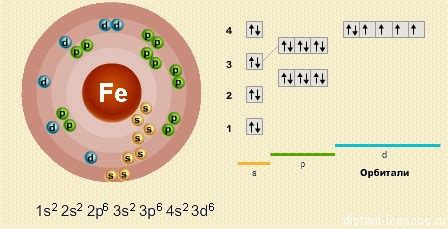
Железо является химическим элементом с атомным номером 26 и символом Fe. Оно принадлежит к группе переходных металлов и находится в 4-м энергетическом уровне. Строение железа включает в себя ядро, состоящее из 26 протонов и, соответственно, 26 электронов.
Железо имеет довольно сложный состав. В его кристаллической решетке присутствуют атомы железа и другие элементы в сплавах, такие как углерод, марганец, кремний и другие. Присутствие этих примесей влияет на физические и химические свойства железа, придавая ему различные виды и свойства.
Большую роль в строении железа играет его кристаллическая структура. В результате охлаждения плавких масс железа образуются различные кристаллические фазы, такие как аустенит, феррит, цементит и перлит. Каждая из этих фаз обладает своими уникальными свойствами, определяющими применение железа в различных отраслях промышленности.
Состав железа также включает в себя следующие изотопы: железо-54, железо-56, железо-57 и железо-58. Изотоп железа-56 является самым распространенным, составляя около 91,75% от всех атомов железа. Именно этот изотоп является стабильным и не обладает радиоактивностью.
Физические свойства железа
Железо — это химический элемент с атомным номером 26 и символом Fe. Оно является металлом, который обладает рядом особых физических свойств.
Магнитные свойства: Железо является ферромагнетиком, то есть обладает способностью притягиваться к магниту и образовывать собственное магнитное поле. Это свойство делает железо незаменимым материалом в производстве магнитов и электромагнитов.
Проводимость: Железо является хорошим проводником электричества и тепла. Благодаря этому свойству оно широко используется в производстве проводов, электрических моторов, трансформаторов и других устройств.
Плотность: Железо имеет высокую плотность – около 7,87 г/см³. Благодаря этому свойству, оно обладает большой массой на единицу объема и является одним из самых тяжелых металлов.
Температура плавления: Точка плавления железа составляет около 1535 °C. Это означает, что при нагреве до этой температуры железо превращается из твердого в жидкое состояние. Такая высокая температура плавления делает железо благоприятным для использования в высокотемпературных процессах, например, в производстве стали.
Вопрос-ответ

Какие химические свойства у железа?
Железо является самым распространенным металлом на Земле и обладает рядом химических свойств. Оно обладает высокой реакционной способностью и активностью, особенно при нагревании. Железо легко соединяется с кислородом, образуя оксиды и гидроксиды. Кроме того, железо растворяется в нескольких кислотах, таких как серная и хлористоводородная, образуя соответствующие соли.
Какие физические характеристики у железа?
Железо обладает рядом физических характеристик. Оно является серебристо-серым металлом, мягким и пластичным, что позволяет его легко обрабатывать. Железо имеет плотность около 7,86 г/см³ и температуру плавления приблизительно 1535 °C. Оно также обладает магнитными свойствами и становится магнитным при нагревании до определенной температуры, называемой точкой Кюри (770 °C для чистого железа).
Что происходит, когда железо взаимодействует с кислородом?
Когда железо взаимодействует с кислородом, образуется оксид железа (III) (Fe2O3), который называется также ржавчиной. При увлажнении оксид железа может растворяться и формировать гидроксидное соединение (Fe(OH)3). Взаимодействие железа с кислородом является основой для коррозии железа и образования ржавчины на его поверхности.
Как используют химические свойства железа в промышленности?
Химические свойства железа широко используются в промышленности. Например, железо используется для производства стали - одного из самых популярных строительных материалов. Железо также используется в производстве различных пищевых добавок, медикаментов, красителей, магнитов и других продуктов. Кроме того, многие реактивы и катализаторы основаны на железе и его соединениях.
