Соли - это химические соединения, которые образуются в результате реакции между кислотами и основаниями. Они являются основными составными частями многих жизненно важных процессов и материалов, таких как пища, лекарства, удобрения и многое другое.
У солей есть ряд характеристических свойств, которые делают их уникальными. Одно из таких свойств - это их растворимость. Некоторые соли легко растворяются в воде, образуя прозрачные растворы, в то время как другие соли мало растворимы и образуют характерные осадки.
Важной ролью солей в химии является их участие в реакциях металлов с основаниями и оксидами. Многие металлы реагируют с основаниями, образуя соли и выделяя водород. Например, реакция между металлом натрием и гидроксидом натрия приводит к образованию соли натрия и выделению водорода.
Металл + Основание = Соль + Водород
Также соли играют важную роль в реакциях металлов с оксидами. Многие металлы реагируют с оксидами, образуя соли и выделяя кислород. Например, реакция между металлом железом и оксидом железа приводит к образованию соли и выделению кислорода.
Металл + Оксид = Соль + Кислород
Понимание химических свойств солей и их роли в реакциях металлов с основаниями и оксидами является важным для различных отраслей науки и технологии, включая химическую промышленность, пищевую промышленность и фармацевтику. Исследования в этой области помогают разработке новых материалов и процессов, а также обеспечивают понимание химических превращений, происходящих в природе и живых организмах.
Химические свойства солей и их роль в реакциях
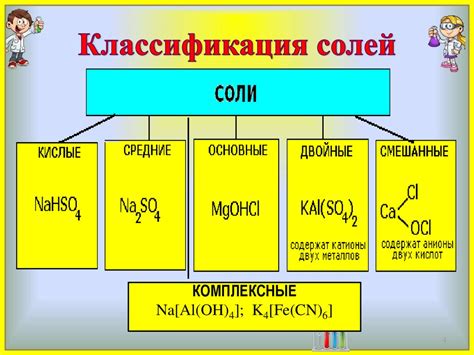
Соли - это класс химических соединений, образованных в результате реакции нейтрализации кислот с основаниями. Они обладают уникальными химическими свойствами, которые определяют их роль в различных реакциях.
Первое химическое свойство солей - это их способность растворяться в воде и образовывать ионные растворы. Вода, как известно, является отличным растворителем для ионных соединений. Поэтому соли легко диссоциируют в растворе на положительные и отрицательные ионы, что делает их реактивными и способными участвовать в химических превращениях.
Второе химическое свойство солей - это их способность производить реакции окисления и восстановления. В химии, реакции окисления и восстановления играют важную роль и являются основой множества химических процессов. Соли могут участвовать в таких реакциях в качестве окислителей или восстановителей, что позволяет им взаимодействовать с другими веществами, изменяя их окислительно-восстановительный статус.
Третье химическое свойство солей - это их способность каталитической активности. Катализаторы - это вещества, которые повышают скорость химической реакции, не изменяясамо своего состава. Соли могут выступать в роли катализаторов и ускорять протекание химических процессов. Они могут активировать молекулы реагентов, улучшая их взаимодействие и повышая эффективность реакции.
В заключение, химические свойства солей делают их важными участниками различных реакций. Они могут служить источником ионов для других реагентов, изменять окислительно-восстановительное состояние веществ и ускорять протекание химических процессов в качестве катализаторов.
Металлы с основами
Основы, или гидроксиды, являются химическими соединениями, состоящими из металла и гидроксильной группы (OH). При реакции металлов с основами происходит образование солей и выделение воды. Эта реакция называется щелочной реакцией.
В щелочной реакции металл сначала реагирует с гидроксидом, образуя гидроксоксидное соединение. Затем, в результате образования ионной связи между металлами и гидроксилами, происходит образование соли.
Металлы могут реагировать с различными основами, такими как гидроксид натрия (NaOH), гидроксид калия (KOH) и гидроксид аммония (NH4OH). Результаты реакций могут быть различными в зависимости от металла и основы, с которыми он реагирует.
Например, натрий (Na) реагирует с гидроксидом натрия (NaOH), образуя соль натрия (NaCl) и выделяя воду. Эта реакция является типичным примером щелочной реакции.
Однако не все металлы реагируют с основами. Некоторые металлы, такие как золото (Au) и платина (Pt), не реагируют с гидроксидами и не образуют солей.
Важно отметить, что реактивность металлов с основами зависит от электрохимической активности металла. Такие металлы, как натрий (Na) и калий (K), являются очень активными и легко реагируют с основами, в то время как металлы, такие как железо (Fe) и алюминий (Al), не так активны и могут реагировать в определенных условиях.
В целом, реакция металлов с основами является важным аспектом в химии и имеет широкое применение в промышленности и научных исследованиях.
Металлы с оксидами
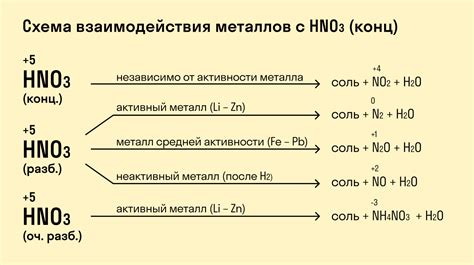
Оксиды металлов - это химические соединения, состоящие из атомов металла и кислорода. Они имеют важное значение в химии и промышленности. Металлы реагируют с оксидами, образуя соли и выделяя кислород. Эти реакции могут быть использованы для получения металлов из их оксидов или для их химического анализа.
При взаимодействии металла с оксидом происходит реакция окисления-восстановления. Металл в данном случае является восстановителем, а оксид - окислителем. В результате реакции окисления металла и восстановления оксида образуется соль металла и кислород. В реакции могут участвовать различные виды оксидов, включая основные и нейтральные оксиды.
Например, реакция металла меди с оксидом свинца PbO приводит к образованию соли меди и выделению кислорода: 2Cu + PbO = Cu2O + Pb + O2. В этой реакции медь восстанавливается из своего оксида до нижней степени окисления, а свинец окисляется из своего оксида до высшей степени окисления.
Металлы с оксидами также могут реагировать с основами, образуя соли и воду. В этой реакции оксид металла работает как кислота и реагирует с основой, которая работает как щелочь. Образуется соль металла и вода. Например, реакция оксида железа(III) Fe2O3 с гидроксидом натрия NaOH приводит к образованию соли железа(III) и воды: Fe2O3 + 6NaOH = 2Fe(OH)3 + 3Na2O.
Таким образом, металлы с оксидами могут реагировать, образуя соли и кислород, или с основами, образуя соли и воду. Эти реакции играют важную роль в химической промышленности и являются основой для получения металлов из их оксидов или для их химического анализа.
Взаимодействие солей с основаниями
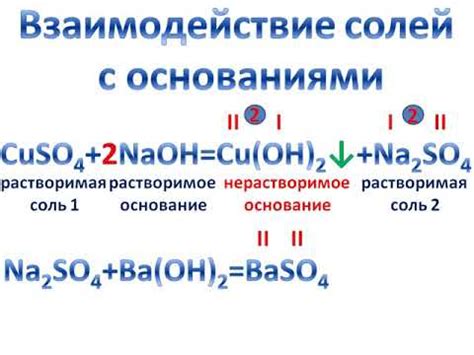
Основания - это химические вещества, которые при растворении в воде образуют ион гидроксида (OH-). Взаимодействие солей с основаниями порождает сложные реакции, в ходе которых образуются новые соединения.
Процесс взаимодействия солей с основаниями называется нейтрализацией. В результате нейтрализации происходит образование солей, воды и, иногда, газа. Данный процесс широко применяется в различных технологических процессах и в химическом анализе.
При нейтрализации образующаяся соль часто оказывает важное влияние на окружающую среду. Например, некоторые ионы солей могут быть токсичными или оказывать антимикробное действие.
Важно отметить, что реакция нейтрализации соли с основанием характеризуется выделением тепла. Это вызвано освобождением энергии при образовании связей между ионами воды и ионами гидроксида.
Другой важной особенностью реакций нейтрализации является изменение pH-значения раствора. Изменение pH особенно заметно в реакциях сильных оснований с кислотами, при которых pH поднимается до щелочного значения.
Взаимодействие солей с оксидами
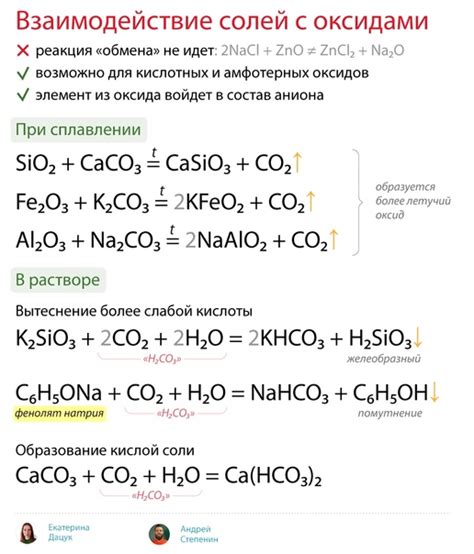
Взаимодействие солей с оксидами является одной из важных реакций в химии. Оксиды представляют собой химические соединения, состоящие из элемента и кислорода. Данные соединения имеют свойства оксидов, такие как щелочность, кислотность или нейтральность.
В химии существуют несколько типов реакций между солями и оксидами. Один из них - реакция нейтрализации, при которой соль и оксид взаимодействуют, образуя новое соединение и основу или кислоту. Например, реакция нейтрализации между солью натрия и гидроксидом калия приводит к образованию соли калия и натрия и воды.
В другом типе реакции, называемой реакцией осаждения, соль и оксид взаимодействуют, образуя новое соединение, которое обычно является осадком. Реакции осаждения широко используются в аналитической химии для определения присутствия и количества определенных соединений.
Взаимодействие солей с оксидами также может приводить к образованию газовых продуктов. Это происходит в реакциях, в которых один из реагентов - соль, содержит ион, который может реагировать с кислородом оксида и образовывать газ. Например, реакция между сульфатом кальция и оксидом углерода приводит к образованию углекислого газа.
В целом, взаимодействие солей с оксидами представляет собой важный аспект в химии, который позволяет изучать свойства и реактивность различных соединений. Эти реакции имеют широкое применение как в научных исследованиях, так и в промышленности.
Роль солей в химических реакциях
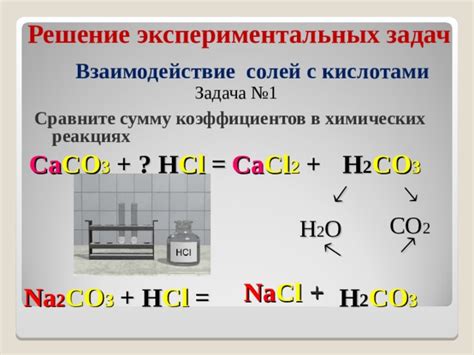
Соли играют важную роль в химических реакциях, так как они могут быть как ионными соединениями, так и содержать комплексные ионы. Ионы солей могут стать источником различных ионов в реакциях между металлами и основаниями или оксидами.
В реакциях с металлами соли могут выступать как источник кислорода, когда соединение распадается, освобождая кислород или кислородную группу. Например, соль перекиси водорода, H2O2, может распадаться при нагревании, выделяя кислород и оставляя металлическое окисление.
Соли также могут играть роль катализаторов в химических реакциях. Например, соль меди может катализировать реакцию между алюминием и водой, ускоряя распад воды на водород и кислород.
Кроме того, соли могут участвовать в реакциях комплексообразования, образуя комплексные ионы с металлами. Комплексные ионы могут иметь особую структуру и химический характер, что может изменить характер реакции. Например, соль синяя кровь, гемоглобин, содержит комплексный ион, который связывает и переносит кислород в организме.
Таким образом, соли играют важную роль в химических реакциях, предоставляя ионы и участвуя в различных химических процессах, таких как окисление, катализ и комплексообразование.
Вопрос-ответ

Какие химические свойства обладают соли?
Соли - это химические соединения, образованные из катиона металла и аниона кислоты. Они обладают рядом характерных свойств, таких как твёрдое состояние при комнатной температуре, высокая степень растворимости в воде, образование характерных кристаллических структур, электролитическая диссоциация в растворах и ионное поведение. Соли также могут быть окрашены, обладать специфическим запахом и светятся в ультрафиолетовом свете.
Какую роль играют соли в реакциях металлов с основами?
В реакциях металлов с основами соли играют роль продукта реакции. При взаимодействии металла с основой образуется вода и соль. Например, при реакции натрия с гидроксидом натрия образуется вода и соль натрия, а при реакции калия с гидроксидом калия образуется вода и соль калия. Соли, образующиеся при таких реакциях, могут быть использованы в различных отраслях промышленности, медицине и других областях человеческой деятельности.
Как влияют соли на реакции металлов с оксидами?
Соли могут влиять на реакции металлов с оксидами различными способами. Например, соли могут быть использованы в качестве каталитических агентов, повышающих скорость реакций или изменяющих их механизм. Они также могут быть использованы как реагенты, изменяющие условия проведения реакции или обеспечивающие необходимые реакционные условия. При реакциях металлов с оксидами образуются соли и вода или другие продукты.
Какие химические свойства солей определяют их роль в реакциях металлов с основами и оксидами?
Химические свойства солей, определяющие их роль в реакциях металлов с основами и оксидами, включают их способность образовывать ионы в растворах, образовывать кристаллические структуры, растворяться в воде и проявлять электролитическую диссоциацию, а также способность катализировать реакции или влиять на реакционные условия. Кроме того, химические свойства солей также могут быть связаны с их структурой и химическим составом.
