Металлы – это элементы, обладающие высокой термической и электропроводностью, отличающиеся способностью образовывать положительные ионы. Когда металлы вступают в реакцию с кислородом, происходит окисление металла.
Окисление – это процесс, при котором вещество теряет электроны, а окислитель – приобретает их. В случае металлического окисления кислород является окислителем. Кислород воздуха проникает в поверхностные слои металла, где происходит реакция, образуется оксид металла.
Оксиды металлов обладают различными свойствами. Некоторые оксиды слабо реагируют с водой и кислотами, другие - растворяются в воде, образуя щелочи. Отдельные оксиды являются простыми соединениями, а другие – сложными. Реактивность металлов при взаимодействии с кислородом может быть использована в различных областях, таких как химическая промышленность и энергетика.
Примеры металлов, реакция которых с кислородом является практически значимой: алюминий, кальций, цинк, железо.
Знание химических свойств металлов при взаимодействии с кислородом позволяет улучшить процессы окисления в промышленности, создать более эффективные материалы и разработать новые технологии производства.
Механизм взаимодействия металлов с кислородом

Взаимодействие металлов с кислородом, или окисление, является основным процессом, определяющим химические свойства металлов. В результате окисления металла образуется оксид, что приводит к изменению его химических и физических свойств. Механизм взаимодействия металлов с кислородом может быть представлен различными способами, в зависимости от конкретных условий.
Одним из основных механизмов является реакция окисления, при которой металл вступает в прямое взаимодействие с кислородом. В результате этой реакции образуется оксид металла. Например, железо вступает в реакцию с кислородом воздуха и образует оксид железа, известный как ржавчина. Данный процесс протекает с выделением тепла и энергии.
Кроме того, взаимодействие металлов с кислородом может происходить через образование промежуточного соединения, такого как гидроксид или перекись. Например, алюминий, при контакте с влагой, образует гидроксид алюминия, который затем может окислиться до оксида. Этот процесс называется пассивацией и позволяет защитить металл от дальнейшего окисления.
Некоторые металлы, такие как золото или платина, обладают высокой степенью стабильности и не вступают в прямое взаимодействие с кислородом. Однако они все же могут быть окислены при повышенных температурах или при наличии катализаторов.
Окисление металлов при контакте с кислородом

Кислород является одним из самых распространенных и активных химических элементов, и его взаимодействие с металлами может приводить к процессу окисления.
Окисление металлов – это процесс, при котором металлы реагируют с кислородом, образуя оксиды. Оксиды металлов обладают различными свойствами и могут быть как полезными, так и вредными.
Реакция окисления металлов с кислородом является химической реакцией окисления, то есть передачи электронов от металла к кислороду. В процессе этой реакции металлы теряют электроны и превращаются в положительно заряженные ионы.
Процесс окисления металлов может быть виден наличием оксидной пленки на их поверхности. Например, на поверхности железа образуется ржавчина – оксид железа, а на поверхности алюминия – оксид алюминия.
Введите параграф или таблицу
Образование оксидов и оксидов металлов
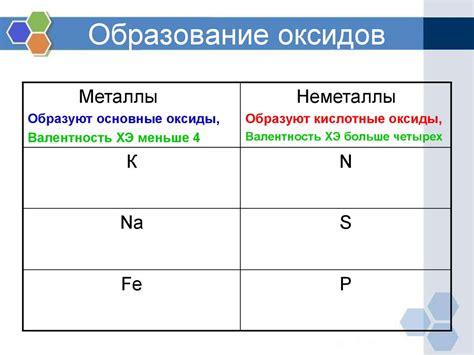
Металлы, взаимодействуя с кислородом, образуют различные оксиды и оксиды металлов. Оксиды - это химические соединения, состоящие из металлического катиона и кислородного аниона. Они могут быть различных типов в зависимости от валентности металла и количества атомов кислорода.
Оксиды металлов могут иметь как ионные, так и ковалентные связи. Образование оксидов и оксидов металлов происходит как в реакции с кислородом воздуха, так и в реакции с кислородсодержащими соединениями, например, водой. Вода может действовать как окислитель, приводя к образованию оксидов, или как восстановитель, приводя к образованию оксидов металлов.
Некоторые металлы, такие как натрий и калий, образуют легко растворимые оксиды, которые смешиваются с водой и образуют щелочные растворы. Другие металлы, например, алюминий и цинк, образуют оксиды, которые не растворяются в воде и обладают амфотерными свойствами.
Свойства оксидов и оксидов металлов могут использоваться в различных отраслях промышленности. Они могут быть использованы как катализаторы, а также в процессах окисления и восстановления. Более того, некоторые оксиды металлов обладают свойствами, которые их делают полезными в производстве стекла, электроники, лакокрасочных материалов и других продуктов.
Вопрос-ответ

Какие металлы реагируют с кислородом и каковы результаты их взаимодействия?
С кислородом реагируют металлы первой группы периодической системы (литий, натрий, калий) и некоторые металлы из второй группы (магний и кальций). В результате их взаимодействия с кислородом образуются оксиды. Например, натрий при реакции с кислородом образует оксид натрия (Na2O), а магний образует оксид магния (MgO).
Почему металлы реагируют с кислородом?
Металлы обладают высокой активностью и легко отдают свои электроны. При контакте с кислородом, который обладает высокой электроотрицательностью, происходит перенос электронов с поверхности металла на кислород. Это приводит к образованию ионов металла и оксидов. Реакция металлов с кислородом является окислительно-восстановительной, где металл окисляется, а кислород восстанавливается.
Какие свойства оксидов металлов, образующихся при взаимодействии с кислородом?
Оксиды металлов, образующиеся при взаимодействии с кислородом, являются основаниями. Они растворяются в воде и образуют гидроксиды, которые обладают щелочными свойствами. Например, оксид натрия растворяется в воде и образует гидроксид натрия (NaOH), который является одним из самых распространенных щелочных растворов. Гидроксиды металлов имеют губительное действие на ткани и кожу, поэтому необходимо соблюдать предосторожность при работе с ними.
