Металлы - это элементы периодической системы, которые обладают некоторыми общими свойствами. Они обладают металлическим блеском, проводят ток и тепло, имеют высокую пластичность и хорошую прочность. Металлы обладают отличными электропроводными свойствами, так как их внешняя оболочка состоит из небольшого количества свободных электронов, которые легко передают электрический ток.
Неметаллы - это элементы, которые обладают противоположными свойствами по сравнению с металлами. Они не имеют металлического блеска, обычно не проводят ток и тепло, а также обладают хрупкостью и низкой пластичностью. Неметаллы образуют коваралентные и ионные соединения и обычно обладают электроотрицательностью - способностью притягивать электроны во время химических реакций.
Кислород - неметалл, который является одним из наиболее распространенных элементов в природе. Он имеет атомный номер 8 и символ O в периодической таблице. Кислород является очень активным элементом и в химических реакциях образует соединения с другими элементами. Он играет особую роль в жизни на Земле, так как является необходимым для дыхания живых организмов и поддержания горения. Кислород также играет важную роль в образовании озона в стратосфере, который защищает Землю от вредных ультрафиолетовых лучей.
Металлы: светимость, проводимость и прочность

Металлы - это класс веществ, обладающих рядом характерных свойств, которые делают их незаменимыми материалами в различных областях промышленности и строительства. Одно из главных свойств металлов - их светимость. Металлы способны отражать свет, благодаря чему ими можно создавать эффектные отражающие поверхности, например, в зеркалах или автомобильных кузовах.
Второе важное свойство металлов - их высокая электропроводность. Металлы являются отличными проводниками электричества благодаря наличию свободно движущихся электронов в их структуре. Благодаря этому металлы применяются для создания проводников, электрических соединений и компонентов электронных устройств.
Кроме того, металлы обладают высокой прочностью и упругостью. Они способны выдерживать большие нагрузки без разрушения и имеют высокий предел прочности. Благодаря этому металлы широко используются в строительстве и производстве машин и оборудования.
Неметаллы: прозрачность, химическая активность и электроотрицательность
Неметаллы - это элементы, обладающие рядом характеристик, которые отличают их от металлов. Одной из особенностей неметаллов является их непрозрачность. Неметаллы не пропускают свет и обычно имеют матовый или полуматовый вид. Однако, среди неметаллов также встречаются исключения, такие как сера и алмаз, которые могут обладать некоторой степенью прозрачности.
Химическая активность неметаллов является еще одной особенностью данной группы элементов. Неметаллы обычно имеют высокую активность и способны реагировать с другими элементами и соединениями. Они часто образуют химические связи с металлами, образуя ионы и молекулы, которые играют важную роль в различных химических процессах и реакциях.
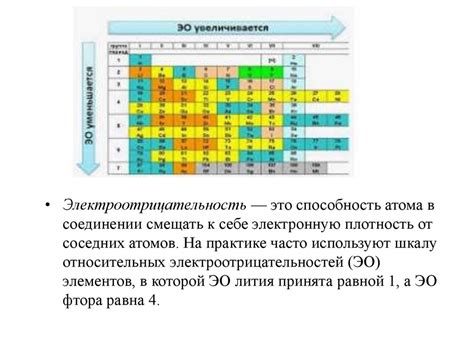
Электроотрицательность также является характеристикой неметаллов. Электроотрицательность - это способность атома притягивать электроны к себе в химической связи. Неметаллы обычно обладают высокими значениями электроотрицательности, что делает их способными привлекать электроны от других элементов и образовывать ковалентные связи. Эта особенность неметаллов объясняет их химическую активность и возможность образования различных соединений.
Кислород: жизненная необходимость, окислительность и влияние на окружающую среду

Кислород является одним из ключевых элементов, обеспечивающих жизнь на Земле. Он необходим для поддержания дыхательного процесса у живых организмов и является основным компонентом воздуха. Без кислорода невозможно существование большинства животных и растений, включая человека.
Окислительные свойства кислорода позволяют ему принимать участие во множестве химических реакций. Кислород способен окислять другие вещества, что является основой для многих биохимических процессов в организмах. При взаимодействии с другими элементами, кислород может образовывать оксиды, которые присутствуют в природе в большом количестве и имеют различные свойства.
Однако кислород также оказывает влияние на окружающую среду. Он может быть участником различных химических реакций, которые влияют на состояние атмосферы и глобального климата. Например, увеличение концентрации кислорода в атмосфере может привести к усилению горения, что может способствовать возникновению лесных пожаров и ухудшению качества воздуха.
Кроме того, кислород может играть роль в образовании озонового слоя. Озоновый слой расположен в верхних слоях атмосферы и оказывает влияние на проникновение ультрафиолетовых лучей на поверхность Земли. Снижение концентрации кислорода в атмосфере может иметь негативные последствия для озонового слоя и стать причиной усиления ультрафиолетового излучения, что может быть опасным для живых организмов.
Таким образом, кислород является не только жизненно важным элементом для живых организмов, но и имеет существенное влияние на окружающую среду. Понимание характеристик и свойств кислорода позволяет более глубоко изучить его роль в природе и принять меры для поддержания его равновесия в окружающей среде.
Реакции с другими элементами: способность к образованию соединений и катализу

Металлы обладают высокой способностью к образованию соединений с другими элементами. Они могут образовывать ионы с положительным зарядом, которые легко соединяются с отрицательно заряженными ионами неметаллов. Металлы могут также образовывать сплавы с другими металлами, при этом сохраняя свои металлические характеристики.
Неметаллы, в отличие от металлов, образуют соединения с положительными ионами. Они обладают высокой электроотрицательностью, что позволяет им притягивать электроны от металлов и образовывать соединения с отрицательным зарядом. Неметаллы могут образовывать молекулы, состоящие из атомов того же элемента или разных элементов, а также полимеры через коэвалентные связи.
Кислород, как неметалл, обладает особой способностью к катализу химических реакций. Он может выступать в качестве катализатора, ускоряющего химическую реакцию, без самого участия в ней. Кислород может быть активным катализатором в реакциях окисления, где он принимает электроны от других веществ и способствует их окислению. Кислород также способствует распаду сложных органических соединений, освобождая энергию и обеспечивая необходимые условия для метаболических процессов в организмах.
Вопрос-ответ

Что такое металлы и каковы их особенности?
Металлы - это элементы, которые обладают способностью проводить тепло и электричество. Основные особенности металлов включают высокую пластичность, прочность, блеск, хорошую теплопроводность и электропроводность. Они также часто обладают высокой плотностью и точкой плавления.
Каковы особенности неметаллов?
Неметаллы - это элементы, которые не обладают свойствами металлов, такими как проводимость тепла и электричества. Основные особенности неметаллов включают низкую плотность, хрупкость, непроводимость электричества и блеска. Они часто образуют ковалентные соединения друг с другом и с металлами.
Каковы особенности кислорода?
Кислород - это химический элемент с атомным номером 8. Он является неметаллом и основным составным элементом воздуха. Основные особенности кислорода включают высокую электроотрицательность, реактивность и окислительные свойства. Он имеет два основных аллотропичных формы: О2 (двухатомный кислород, который мы дышим) и О3 (озон).
