Металлы - это группа химических элементов, которые обладают особыми свойствами. Они обычно имеют металлическую блеск, высокую теплопроводность и электропроводность, а также способность образовывать положительные ионы. Металлы являются важной частью нашей повседневной жизни, так как они используются в различных отраслях промышленности, от строительства до электроники.
Одним из наиболее известных химических свойств металлов является их способность образовывать ионы положительного заряда. Это происходит из-за особенной структуры исходных атомов металлов, у которых наружные электронные оболочки состоят из отдельных или общих электронов, легко отделяющихся от своих атомов. Таким образом, металлы способны образовывать положительные ионы, которые могут образовывать связи с другими атомами, образуя различные соединения.
Кроме того, металлы имеют высокую теплопроводность и электропроводность. Это объясняется их особой структурой и способностью электронов свободно двигаться. В металлах электроны наружной оболочки не связаны с конкретными атомами, а образуют «море» электронов. Это позволяет электрическим зарядам легко перемещаться по металлической структуре, что делает металлы отличными проводниками электричества и тепла.
Некоторые металлы также обладают некоррозионной стойкостью, то есть они не реагируют с окружающей средой и не подвергаются химическому разрушению. Это особенно ценно при использовании металлов в промышленности и строительстве, где они должны выдерживать различные воздействия и сохранять свои свойства на протяжении длительного времени.
Химические свойства металлов еще далеко не полностью изучены, и наука продолжает исследовать их уникальные возможности и потенциальные применения. Изучение этих свойств может иметь важное значение для развития новых материалов и технологий, а также для понимания и прогнозирования поведения металлов в различных условиях и средах.
Особенности химических свойств металлов

Металлы обладают рядом особенных химических свойств, которые делают их уникальными материалами.
Реактивность: Металлы реагируют с кислородом, водой и кислотами, образуя оксиды, гидроксиды и соли. Это свойство позволяет им участвовать во многих химических процессах и быть активными катализаторами реакций.
Электропроводность: Большинство металлов обладают высокой электропроводностью. Это связано с наличием свободных электронов в их кристаллической структуре, которые могут легко перемещаться под воздействием электрического поля.
Пластичность и формоизменяемость: Металлы имеют способность быть подверженными пластической деформации - изменению формы без разрушения. Благодаря этому свойству, металлы можно легко обрабатывать и формировать различные изделия.
Изготовление сплавов: Металлы могут быть сплавлены вместе для получения материала с новыми свойствами. Например, добавление небольшого количества другого металла может повысить прочность и твердость материала или изменить его цвет.
Способность к восстановлению: Многие металлы могут вступать в реакции с химическими веществами и возвращаться в исходное состояние. Это позволяет повторно использовать металлы и уменьшать их потребление в производстве.
Коррозионная стойкость: Некоторые металлы, такие как нержавеющая сталь и алюминий, обладают высокой стойкостью к химической коррозии. Это делает их очень популярными в промышленности и строительстве.
Базовые свойства металлов
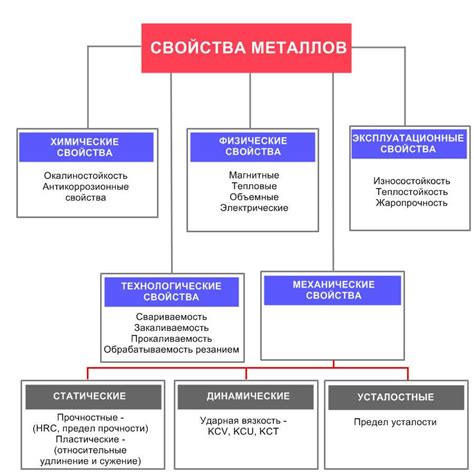
Металлы - это группа химических элементов, которые обладают несколькими характеристическими свойствами. Одно из основных свойств металлов - это высокая теплопроводность. Именно благодаря своей структуре и наличию свободных электронов металлы отлично проводят тепло, что позволяет им быть широко использованными в различных отраслях промышленности, включая производство теплообменников и электрических проводов.
Еще одной важной особенностью металлов является высокая электропроводность. Это означает, что металлы хорошо проводят электрический ток и используются в производстве электроники, электрических контактов и различных электродов.
Металлы также обладают высокой пластичностью и прочностью. Они могут быть легко деформированы и изгибаться без поломки. Благодаря этим свойствам металлы используются для изготовления конструкций, машин, транспортных средств, а также в строительстве.
Еще одной важной характеристикой металлов является их способность образовывать сплавы. Многие металлы могут быть смешаны с другими металлами или неметаллическими элементами, чтобы создать сплавы с новыми свойствами. Например, железо в сплаве с углеродом образует сталь, которая обладает высокой прочностью.
Также металлы обычно обладают блестящей поверхностью, что связано с их способностью отражать свет. Это свойство металлов используется в производстве зеркал и различных отражающих поверхностей.
Коррозионная стойкость металлов
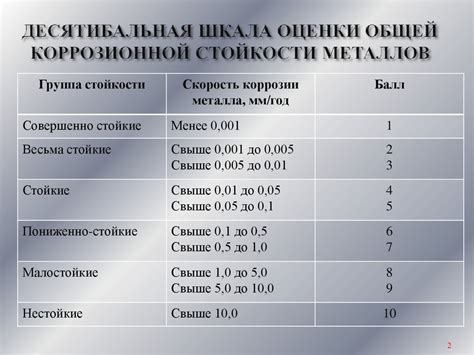
Коррозионная стойкость металлов - это их способность сопротивляться разрушению под воздействием агрессивных сред. Различные металлы проявляют разную степень стойкости к коррозии, что связано с их химическим составом и структурой.
Одним из самых коррозионно-стойких металлов является нержавеющая сталь. Она содержит хром, который образует пассивную оксидную пленку на поверхности металла, защищающую его от воздействия окружающей среды. За счет этой пленки, нержавеющая сталь остается стойкой к коррозии в различных условиях, включая воздействие влаги и агрессивных химических веществ.
Алюминий также обладает хорошей коррозионной стойкостью благодаря образованию пассивной оксидной пленки на его поверхности. Это позволяет алюминию использоваться в строительстве, производстве авиационной и космической техники, а также в пищевой промышленности. Однако, алюминий может подвергаться коррозии в щелевых и трещинных зонах, а также при воздействии солевых растворов и кислот.
Цинк также имеет высокую коррозионную стойкость. Специально созданный цинковый слой, нанесенный на поверхность металла, называется гальваническим покрытием. Оно позволяет защитить сталь от коррозии и часто применяется для обработки металлических изделий, например, при производстве автомобилей и бытовой техники.
Однако, существует ряд металлов, которые обладают низкой коррозионной стойкостью и подвержены быстрому разрушению при взаимодействии с окружающей средой. К таким металлам относятся железо и его сплавы, которые подвергаются окислению воздухом и водой, а также медь, которая подвержена окислению и образованию зеленой патины при воздействии влаги и газов.
В целом, знание коррозионной стойкости различных металлов позволяет правильно выбирать материалы для конкретных задач и обеспечивать долговечность изделий и конструкций.
Специфичные реакции металлов

Металлы обладают широким спектром химических свойств, что делает их важными в различных отраслях промышленности и научных исследованиях. Они способны проявлять специфичные реакции, в зависимости от своих физических и химических свойств.
Кислотные реакции являются одной из наиболее распространенных специфичных реакций металлов. Металлы могут реагировать с кислотами, образуя соли и выделяя водород. Например, цинк реагирует с соляной кислотой, образуя хлорид цинка и выделяя водород.
Окислительно-восстановительные реакции также характерны для металлов. Они могут проявлять свою способность окисляться или восстанавливаться. Например, медь может взаимодействовать с серной кислотой, при этом окисляться до двухвалентной формы катиона меди(II) и восстанавливать серную кислоту до диоксида серы.
Кроме того, некоторые металлы могут реагировать с веществами, образуя осадки или специфичные соединения. Например, при взаимодействии железа с солевым раствором меди формируется осадок меди. Это явление называется реакцией нагревания.
Прохождение электрического тока через металлы сопутствует специфичным реакциям. Металлы, обладающие хорошей проводимостью электрического тока, могут реагировать с электролитами в электролитических реакциях. Например, медь может раствориться в серной кислоте при протекании электрического тока.
Таким образом, специфичные реакции металлов обусловлены их уникальными свойствами и могут использоваться в различных областях науки и промышленности, от химической синтеза до электрохимических процессов.
Вопрос-ответ

Какие свойства у металлов связаны с их химической активностью?
Химическая активность металлов связана с их способностью образовывать ионные соединения, окисляться и восстанавливаться. Металлы обычно имеют большую склонность отдавать электроны и образовывать положительные ионы.
Почему аллюминий считается химически активным металлом?
Аллюминий считается химически активным металлом, потому что он имеет высокую электроотрицательность и способен с легкостью реагировать с водой и кислородом. Он образует пассивную пленку оксида на своей поверхности, что защищает его от окисления воздухом.
Какую роль играют металлы в химических реакциях?
Металлы могут играть разные роли в химических реакциях. Они могут быть окислителями, веществами, которые отдают электроны и окисляются в процессе реакции. Они также могут быть восстановителями, веществами, которые принимают электроны и восстанавливаются в процессе реакции.
Как металлы реагируют с кислотами?
Многие металлы реагируют с кислотами. При этом образуется соль и выделяется водород. Некоторые металлы, такие как магний и алюминий, реагируют с кислотами очень активно, тогда как другие металлы, например, золото и платина, реагируют с кислотами очень медленно или вообще не реагируют.
