Взаимодействие кислот с металлами является одной из основных тем изучения химических свойств веществ. Кислоты - это вещества, способные отдавать H+ и образовывать ионы при растворении в воде. Металлы, в свою очередь, представляют собой элементы с высокой электропроводностью и способностью образовывать положительные ионы.
Опыты по взаимодействию кислот с металлами позволяют наглядно продемонстрировать различные химические реакции, происходящие при контакте этих веществ. Один из распространенных опытов - взаимодействие соляной кислоты с металлическим цинком. При смешивании этих веществ происходит реакция, в ходе которой выделяется водородный газ и образуется соответствующая соль. При аналогичном взаимодействии соляной кислоты с алюминием образуется алюминий хлорид и выделяется водород.
Химические свойства кислот и металлов играют важную роль не только в лабораторных опытах, но и в реальной жизни. Одним из примеров может служить сохранение и усиление металлических конструкций, покрытых кислотоустойчивыми материалами. Это позволяет предотвратить коррозию и сохранить исходный внешний вид и функциональность металлических изделий на протяжении длительного времени.
Таким образом, изучение взаимодействия кислот с металлами и их химических свойств имеет большое практическое значение и позволяет лучше понять принципы химии и ее применение в различных областях нашей жизни.
Важность изучения взаимодействия кислот и металлов

Взаимодействие кислот и металлов – это сложный процесс, имеющий большое значение в химии. Это взаимодействие позволяет изучать химические свойства различных металлов и составлять соответствующие реакционные схемы.
Одно из важных практических применений этого взаимодействия – коррозия металлов, которая может приводить к разрушению различных конструкций и повышенным затратам на их ремонт и замену. Изучение процессов коррозии помогает разрабатывать защитные покрытия и материалы, продлевающие срок службы металлических изделий.
Также изучение взаимодействия кислот и металлов позволяет понять особенности химических процессов, происходящих при различных экологических условиях. Например, изучение реакций с металлами может помочь лучше понять, какие вещества и в каком количестве выделяются в окружающую среду в результате преобразования химических соединений.
Изучение взаимодействия кислот и металлов также находит применение в медицине и фармакологии. Многие лекарственные препараты содержат ионы металлов, и изучение их взаимодействия с кислотами позволяет оптимизировать их химический состав и улучшить их эффективность.
Опыты по взаимодействию соляной кислоты и цинка

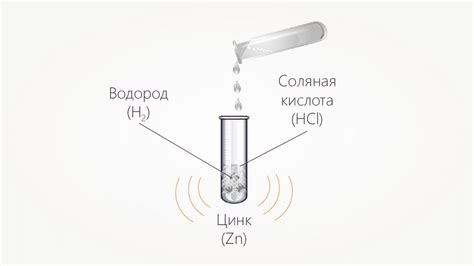
Опыты по взаимодействию соляной кислоты и цинка представляют собой одно из наиболее известных химических экспериментов. Данная реакция позволяет наглядно продемонстрировать процесс образования газа в результате взаимодействия кислоты с металлом.
Во время проведения опыта в реакционную колбу соляной кислоты добавляется цинка, который активно взаимодействует с кислотой. В результате реакции образуется хлорид цинка и выделяется водородный газ. Наблюдение выделения газа можно сделать с помощью нанесения горящей спички к отверстию колбы, что приводит к короткому всплеску пламени.
Опыты по взаимодействию соляной кислоты и цинка широко используются в школьных лабораториях, так как позволяют детально изучить химическую реакцию и закрепить знания о свойствах кислот и металлов. Это также отличный способ практического применения полученных знаний о балансировке химических уравнений и характеристиках веществ.
Проведение этих опытов рекомендуется осуществлять с соблюдением всех необходимых мер предосторожности, так как во время реакции выделяется ядовитый хлористый газ и возникает огнеопасность. Проведение опытов должно осуществляться под руководством опытного преподавателя или химика.
Химические свойства соляной кислоты и железа

Соляная кислота, также известная как хлороводородная кислота, является одной из наиболее распространенных кислот в химических лабораториях. Она обладает рядом химических свойств, включая высокую коррозионную активность, растворительную способность и кислотность.
Соляная кислота реагирует с железом и вызывает образование водорода и хлорида железа. Эта реакция может быть использована для определения содержания железа в различных материалах. При взаимодействии с металлическим железом, соляная кислота протекает с выделением тепла и образованием химических соединений.
Железо, в свою очередь, также обладает своими уникальными химическими свойствами. Оно является мягким металлом, но под действием кислот, таких как соляная кислота, может производить реакцию окисления, образуя соединения с различными кислородными атомами.
- Соляная кислота позволяет растворить железо, образуя хлорид железа.
- Реакция между соляной кислотой и железом является экзотермической, то есть сопровождается выделением тепла.
- Железо может быть использовано в качестве катализатора для некоторых реакций соляной кислоты.
В целом, взаимодействие соляной кислоты с железом является важным аспектом в исследовании и понимании химических процессов и свойств этих веществ. Оно позволяет изучать проявление коррозии, растворительных способностей и реакционной активности данной кислоты.
Эксперименты с уксусной кислотой и медью

Уксусная кислота – это одна из наиболее распространенных кислот, которая широко используется в химических экспериментах. При взаимодействии с металлами она проявляет свои химические свойства.
Один из интересных экспериментов – это реакция уксусной кислоты с медью. При взаимодействии этих веществ возникает химическая реакция, которая можно наблюдать невооруженным глазом.
В начале эксперимента необходимо взять кусок меди и поместить его в стакан с уксусной кислотой. После некоторого времени начинается активное выделение пузырьков – это результат образования газа при реакции кислоты с медью.
Реакция уксусной кислоты с медью может быть представлена следующим уравнением: Cu + 2CH3COOH → Cu(CH3COO)2 + H2
Образовавшийся при взаимодействии газ – это водород. Поэтому в ходе эксперимента можно провести дополнительные наблюдения, например, посмотреть, как водород загорается от открытого огня.
Химические реакции между серной кислотой и алюминием

Серная кислота является одним из наиболее распространенных и активных минеральных кислот. Она обладает высокой коррозионной активностью и способна реагировать с большим количеством веществ, включая металлы.
Когда серная кислота вступает в контакт с алюминием, происходит реакция, которая может быть описана следующим образом:
- Серная кислота взаимодействует с поверхностью алюминия, образуя гидроксид алюминия и сероводород:
- Al + H2SO4 —> Al(OH)3 + H2S
- Al(OH)3 + 3H2SO4 —> Al(SO4)3 + 3H2O
Таким образом, результатом реакции между серной кислотой и алюминием является образование соли алюминия и выделение сероводорода. Образовавшаяся соль алюминия может быть использована в различных областях, включая производство бумаги, кожи, стекла и других химических продуктов. Реакция также может протекать с выделением тепла, что делает ее обратимой, если регулировать условия в реакционной среде.
Реакция соляной кислоты с свинцом
Соляная кислота (хлороводородная кислота) воздействует на свинец, вызывая реакцию между металлом и кислотой. Эта реакция приводит к образованию хлоридов свинца и выделению газа водорода.
Контакт между соляной кислотой и свинцом приводит к образованию белых кристаллических отложений, состоящих и
Реакция между соляной кислотой и магнием

Соляная кислота (HCl) – это одна из самых распространенных и известных кислот. Магний (Mg) – это щелочноземельный металл, который является активным веществом и реагирует с многими кислотами, включая соляную кислоту.
Реакция между соляной кислотой и магнием происходит с образованием хлорида магния (MgCl2) и выделением водорода (H2). Эта реакция является экзотермической, то есть выделяется тепло.
Химическое уравнение реакции выглядит следующим образом:
Mg + 2HCl -> MgCl2 + H2
Важно отметить, что магний реагирует с соляной кислотой только при наличии воды, так как реакция происходит через образование протолитической воды (H2O) в результате диссоциации соляной кислоты.
Данная реакция может быть визуализирована при проведении лабораторного опыта. Для этого в реакционную колбу добавляют магнийную стружку и наливают соляную кислоту. При вступлении магния в контакт с кислотой начинается выделение газа – водорода, который можно заметить по искрам и плавающим в колбе пузырькам. Также можно измерить образовавшееся количество газа с помощью специального объемного сосуда.
Вопрос-ответ

Как происходит взаимодействие кислот с металлами?
Взаимодействие кислот с металлами происходит посредством образования солей и выделения водорода. Когда металл вступает в реакцию с кислотой, происходит окислительно-восстановительное взаимодействие. Металл окисляется, а водород и ион кислоты восстанавливаются.
Какие кислоты реагируют с металлами?
Реакция кислот с металлами происходит только с кислотами, которые могут отдавать протоны (H+) - это минеральные и органические кислоты. Примерами таких кислот могут служить серная H2SO4, соляная HCl, азотная HNO3 и уксусная CH3COOH кислоты.
Какие металлы реагируют с кислотами?
Реакция металлов с кислотами зависит от активности металла. Наиболее активные металлы, такие как натрий Na и калий K, реагируют с большинством кислот, включая сильные. Более редкие и менее активные металлы, такие как медь Cu или серебро Ag, не реагируют со многими кислотами.
Какие свойства проявляются при взаимодействии кислот с металлами?
При взаимодействии кислот с металлами проявляются ряд химических свойств. Во-первых, металл окисляется, отдавая электроны кислоте. В результате этой реакции на месте металла образуется ион металла, а в раствор выделяются положительно заряженные ионы кислоты. Во-вторых, в раствор выделяется водород - признак газообразной реакции. Также может наблюдаться выделение тепла и плавление металла при взаимодействии с кислотой.
Какие опыты можно провести, чтобы наблюдать взаимодействие кислот с металлами?
Для наблюдения взаимодействия кислот с металлами можно провести несколько простых опытов. Например, можно добавить небольшой кусочек металла в колбу с кислотой и наблюдать, как металл растворяется и образуется пузырьки газа. Также можно провести опыт с использованием газового сборника - при взаимодействии кислоты с металлом внутри сборника будет накапливаться выделяющийся водород. Эти опыты можно проводить с разными металлами и кислотами, чтобы наблюдать различные реакции.
