Щелочноземельные металлы – это группа химических элементов, расположенная во второй группе периодической таблицы. К ним относятся бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Щелочноземельные металлы имеют сравнительно малую электроотрицательность и высокую ионизационную энергию. Они являются металлами, легкими, блестящими и хорошо проводящими электричество и тепло.
Эти элементы получили свое название "щелочноземельные" из-за своего химического поведения, которое напоминает поведение щелочных металлов из первой группы. Однако, щелочноземельные металлы менее реактивны и менее электроотрицательны, чем щелочные металлы.
Соединения щелочноземельных металлов имеют широкий спектр применения в различных отраслях науки и техники. Например, окись магния (MgO) используется в производстве огнеупорных материалов и кабельных изоляторов. Карбид кальция (CaC2) применяется в производстве ацетилена и кальциевых солей, а сульфат бария (BaSO4) используется в медицине и рентгенологии для рентгеновской съемки и улучшения контраста на рентгенограммах.
В целом, щелочноземельные металлы являются важными элементами, которые широко используются в промышленности и науке благодаря своим физическим и химическим свойствам. Изучение и применение соединений этих элементов является актуальной задачей современной химии и материаловедения.
Щелочноземельные металлы - что это такое?

Щелочноземельные металлы - это группа химических элементов, которая включает в себя бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они относятся к группе элементов второго периода семи периодической системы.
Щелочноземельные металлы характеризуются ярко выраженными металлическими свойствами. Они обладают высокой термической и электрической проводимостью, имеют серебристо-белый цвет и мягкую консистенцию. Более того, они имеют низкую плотность, что делает их легкими.
Щелочноземельные металлы активно реагируют с водой, выделяя водород и образуя гидроксиды. Они также образуют соединения с кислородом, хлором, серой и другими элементами. Бериллий является исключением, поскольку он не образует гидроксид и реактивен только с концентрированными кислотами.
Щелочноземельные металлы широко используются в различных отраслях промышленности и технологий. Например, магний используется в производстве сплавов, углеродного волокна и пиротехнических смесей, а кальций применяется как добавка в стали и как компонент в производстве строительных материалов.
Физические свойства щелочноземельных металлов

Щелочноземельные металлы представляют собой группу химических элементов, которые обладают рядом уникальных физических свойств.
Во-первых, щелочноземельные металлы характеризуются низкой плотностью, что делает их легкими и мягкими металлами. Высокая мягкость позволяет легко резать и формировать эти металлы.
Во-вторых, щелочноземельные металлы имеют низкую температуру плавления, что делает их подверженными быстрой коррозии. Однако при наличии покрытий или специальной обработки, они могут быть защищены от окисления и воздействия влаги.
В-третьих, щелочноземельные металлы обладают хорошей теплопроводностью и электропроводностью, что делает их ценным материалом для использования в различных электронных и электрических устройствах.
Кроме того, щелочноземельные металлы обладают высокой реактивностью и способностью образовывать стабильные и сильные ионы. Это делает их важными компонентами во многих химических реакциях и соединениях.
В целом, физические свойства щелочноземельных металлов определяют их широкое применение в различных областях науки и техники, от производства сплавов до создания батарей и радиоэлектроники.
Химические свойства щелочноземельных металлов

Щелочноземельные металлы представляют собой вторую группу периодической системы элементов и включают в себя бериллий, магний, кальций, стронций, барий и радий. Эти металлы имеют ряд характеристических химических свойств, которые делают их уникальными.
Одной из ключевых особенностей щелочноземельных металлов является их высокая реакционность. Они реагируют с водой, кислородом, кислотами и прочими веществами, образуя различные соединения. Например, магний горит на воздухе, образуя белую пыль, а бериллий реагирует с водой, образуя щелочь и водород.
Другим важным свойством щелочноземельных металлов является их способность образовывать ионы с положительным зарядом. Например, ион магния имеет заряд +2, а ион кальция - +2. Это позволяет им образовывать соли с отрицательными ионами, такими как карбонаты, оксиды и гидроксиды.
Щелочноземельные металлы также обладают хорошей термической и электрической проводимостью. Это позволяет им использоваться в различных промышленных и научных областях, например, в производстве сплавов, легировании сталей и в электронике.
Кроме того, такие металлы как барий и стронций имеют свойства эмитировать атомы при возбуждении и использоваться в медицине для проведения рентгеновской томографии и других исследовательских процедур.
Таким образом, щелочноземельные металлы обладают уникальными химическими свойствами, которые делают их важными в различных областях науки и промышленности.
Соединения щелочноземельных металлов
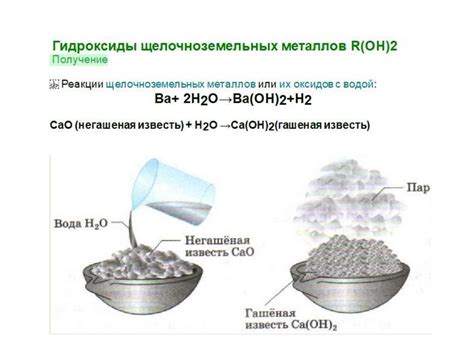
Щелочноземельные металлы обладают высокой активностью и образуют многочисленные соединения с другими элементами. Одним из наиболее распространенных типов соединений щелочноземельных металлов являются оксиды. Оксиды щелочноземельных металлов имеют общую формулу MO, где M - металл щелочноземельной группы. Они обладают щелочными свойствами, что объясняется высокой алкальностью металлов данной группы.
Еще одним типом соединений щелочноземельных металлов являются гидроксиды. Гидроксиды имеют формулу MOH и образуются в результате реакции металлов щелочноземельной группы с водой. Гидроксиды также обладают щелочными свойствами и являются сильными основаниями.
Карбонаты щелочноземельных металлов также являются широко распространенными соединениями. Имея общую формулу MCO3, карбонаты щелочноземельных металлов представляют собой соли угольной кислоты. Они обладают щелочными свойствами и часто используются в производстве стекла, шамотных изделий и прочих материалов.
Большое значение имеют также сульфаты щелочноземельных металлов. Они имеют общую формулу MSO4 и широко используются в промышленности. Сульфаты щелочноземельных металлов обладают губительными свойствами, что делает их эффективными в процессах очистки воды.
Кроме того, щелочноземельные металлы образуют многочисленные другие соединения, включая фосфаты, нитраты, хлориды и многие другие. Их свойства и применение зависят от специфики каждого конкретного соединения и могут быть разнообразными.
Вопрос-ответ

Что такое щелочноземельные металлы и какие они бывают?
Щелочноземельные металлы – это группа химических элементов, включающая бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они находятся во второй группе периодической системы и имеют общие характеристики. Все они обладают низкой плотностью, низкой температурой плавления и высокой химической реактивностью.
Какие вещества можно получить из щелочноземельных металлов?
Из щелочноземельных металлов можно получить различные соединения. Например, оксиды, которые широко используются в промышленности и в нашей повседневной жизни. Также можно получить гидроксиды, которые являются основаниями и часто используются в химической промышленности. Еще одним важным соединением, получаемым из щелочноземельных металлов, являются соли, которые широко используются в пищевой промышленности и медицине.
Каким образом щелочноземельные металлы взаимодействуют с водой?
Щелочноземельные металлы взаимодействуют с водой, образуя гидроксиды и высвобождая водород. Реакция происходит очень быстро и выделяется большое количество тепла. Например, магний реагирует с водой, образуя гидроксид магния и высвобождая водород. Реакция имеет следующий вид: Mg + 2H2О -> Mg(OH)2 + H2.
Какова роль щелочноземельных металлов в биологических системах?
Щелочноземельные металлы играют важную роль в биологических системах. Например, кальций является основным строительным элементом костей и зубов у животных и людей. Он также участвует в сокращении мышц и передаче нервных импульсов. Магний является важным элементом во многих ферментах и играет роль в обмене веществ. Бериллий и его соединения почти не взаимодействуют с органическими веществами, но все же имеют некоторое значение в биологии и медицине.
