Химические реакции с металлами представляют собой значительную часть изучаемого в химии материала. Интерес к ним заключается в их важной роли в различных процессах, применяемых в нашей повседневной жизни. Металлы, включая железо, алюминий, медь и цинк, широко используются в производстве металлоконструкций, электроники, автомобилей и многих других отраслях промышленности. Поэтому освоение химических реакций с металлами имеет большое значение для понимания их свойств и возможностей использования.
Во время химических реакций металлы могут образовывать различные соединения и ионы. Например, при взаимодействии с кислотой металлы образуют соли и выделяются газы. Такие реакции широко применяются в химической промышленности и лабораториях для получения нужных соединений и проведения различных анализов.
Задачи, связанные с химическими реакциями с металлами, включают в себя расчеты, описания реакций и практическую работу в лаборатории. Они требуют знания основных принципов химии и умения применять их для решения конкретных задач.
Для успешного решения задач, связанных с химическими реакциями с металлами, необходимо уметь выполнять расчеты на основе химических уравнений и знать правила балансировки реакций. Также важно понимать основные характеристики металлов, их реакционную способность и взаимодействие с другими веществами. При решении задач необходимо учитывать условия реакции, температуру, давление и концентрацию реагентов.
Химические реакции с металлами
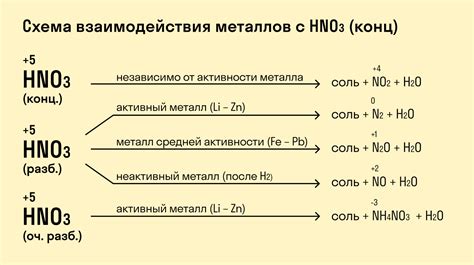
Химические реакции с металлами являются одной из основных тем в изучении химии. Металлы, благодаря своим химическим свойствам, обладают способностью образовывать соединения с другими веществами. При этом металлы могут вступать в различные реакции, в том числе окислительные, восстановительные и замещения.
Одной из наиболее известных химических реакций с металлами является реакция с кислородом, называемая окислительной реакцией. В результате этой реакции металлы окисляются, образуя оксиды. Например, при контакте железа с кислородом происходит образование оксида железа (III) Fe2O3.
Восстановительные реакции с металлами характеризуются обратным процессом - металлы выступают в роли восстановителей, способных окислиться при взаимодействии с другими веществами. Например, при взаимодействии алюминия с кислотой соляной происходит выделение водорода и образование соединения алюминия и хлора.
Химические реакции с металлами также могут включать в себя замещение одного металла другим. Это реакция обмена, при которой металлы замещают друг друга в соединении. Например, при реакции меди с серной кислотой происходит замещение меди атомами металла, образуя сульфат меди и выделяя водород.
Изучение химических реакций с металлами позволяет лучше понять и выявить особенности химического взаимодействия различных веществ. Оно является важной составляющей в обучении химии и науке в целом.
Понятие о химических реакциях

Химическая реакция - это процесс превращения одних веществ в другие, когда изменяются их состав и свойства. В результате химической реакции образуются новые вещества с различными химическими свойствами.
Химические реакции могут происходить при взаимодействии различных веществ, включая металлы. Металлы являются химически активными элементами и способны вступать в реакцию с другими веществами, образуя новые соединения.
- Окислительно-восстановительные реакции: одно вещество окисляется (получает кислород или теряет электроны), а другое вещество восстанавливается (теряет кислород или получает электроны).
- Кислотно-основные реакции: реакции между кислотами и основаниями, в результате которых образуются соли и вода.
- Диспропорционирование: процесс, при котором одно вещество окисляется и восстанавливается одновременно.
- Комплексообразование: образование комплексных соединений при взаимодействии металлов с третьими веществами (лигандами).
В химических реакциях с металлами возможно образование осадков или газов, сопровождающихся изменением цвета, температуры или других свойств веществ. Эти реакции часто используются в химическом анализе, производстве материалов и промышленных процессах.
| Пример | Реакция |
|---|---|
| Окисление железа | 3Fe + 4H2O + O2 → Fe3O4 + 4H2O |
| Реакция кислорода с магнием | 2Mg + O2 → 2MgO |
Типы химических реакций с металлами

Химические реакции с металлами представляют собой важный раздел химии. Металлы могут реагировать с различными веществами, образуя различные продукты.
Одним из типов реакций с металлами является реакция металла с кислотой. При этом образуется соль и выделяется водород. Например, при реакции цинка с соляной кислотой образуется хлорид цинка и выделяется водород.
Еще одним типом реакции является реакция металла с кислородом. При этом образуется металлический оксид. Например, при реакции железа с кислородом образуется оксид железа.
Также существует реакция металла с водой. В зависимости от активности металла, образуются различные продукты. Например, при реакции натрия с водой образуется гидроксид натрия и выделяется водород.
Другим типом реакции с металлами является реакция металла с кислотно-основной парой. В результате образуется соль и выделяется вода. Например, при реакции цинка с серной кислотой образуется сульфат цинка и выделяется вода.
Таким образом, разнообразные химические реакции с металлами играют важную роль в химии и науке в целом. Они позволяют изучать свойства металлов, а также использовать их в различных промышленных и бытовых целях.
Решение задач по химическим реакциям с металлами

1. Задача: При взаимодействии меди со соляной кислотой образуется раствор меди (II) хлорида и выделяется газы. Необходимо определить массу полученного медного хлорида, если изначально было использовано 10 г меди.
Решение: Сначала определим стехиометрический коэффициент реакции между медью и соляной кислотой. Уравнение этой реакции выглядит следующим образом: Cu + 2HCl → CuCl2 + H2.
Исходя из уравнения, стехиометрический коэффициент между медью и медным хлоридом равен 1:1. Следовательно, масса медного хлорида будет равна массе использованной меди.
Таким образом, полученная масса медного хлорида будет составлять 10 г.
2. Задача: В результате реакции цинка с серной кислотой образуется сульфат цинка и выделяется водород. Необходимо определить массу полученного сульфата цинка, если изначально было использовано 30 г цинка.
Решение: Сначала определим стехиометрический коэффициент реакции между цинком и серной кислотой. Уравнение этой реакции выглядит следующим образом: Zn + H2SO4 → ZnSO4 + H2.
Исходя из уравнения, стехиометрический коэффициент между цинком и сульфатом цинка равен 1:1. Следовательно, масса сульфата цинка будет равна массе использованного цинка.
Таким образом, полученная масса сульфата цинка будет составлять 30 г.
В решении задач по химическим реакциям с металлами необходимо учитывать стехиометрический коэффициент реакции и использовать соответствующие формулы и уравнения. Также необходимо следить за правильным переводом массы из одних единиц в другие и учитывать, что масса реагентов и продуктов реакции должна сохраняться. Задачи такого типа позволяют закрепить знания о химических реакциях и применить их на практике для решения конкретных задач.
Практические примеры химических реакций с металлами
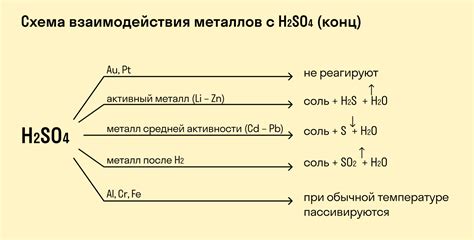
Химические реакции с металлами имеют широкий спектр практического применения в различных областях науки и промышленности. Они могут использоваться для получения новых материалов, проведения анализа веществ, а также в процессах электролиза, гальванизации и даже изготовления украшений.
Одним из примеров реакции с металлом является реакция железа с кислородом, в результате которой образуется ржавчина. Это практически важный процесс, так как ржавые стали и железо часто применяются в строительстве и производстве, а поверхностная окись, образующаяся при реакции железа с кислородом, защищает металл от дальнейшего окисления.
Другим примером реакции металла может быть реакция алюминия с кислородом, в результате которой образуется оксид алюминия. Эта реакция важна при производстве алюминиевых изделий и материалов, так как оксид алюминия обладает высокой степенью стойкости к действию различных химических веществ и высокой температуре.
Также стоит отметить реакцию цинка с серной кислотой, при которой образуется водород. Эта реакция может быть использована для проведения химического анализа серной кислоты или для получения чистого водорода, который применяется в водородных топливных элементах или в процессе синтеза различных органических соединений.
Все эти примеры демонстрируют, что химические реакции с металлами играют важную роль в различных областях науки и техники, позволяя получать новые материалы, проводить анализ веществ и создавать инновационные технологии.
Вопрос-ответ

Какие бывают химические реакции с металлами?
Химические реакции с металлами могут быть разными и зависят от конкретного металла и вещества, с которым он взаимодействует. Некоторые общие типы реакций с металлами включают окислительно-восстановительные реакции, реакции с кислородом, реакции с кислотами и реакции с основаниями.
Какая реакция происходит между металлами и кислотами?
Металлы могут реагировать с кислотами, образуя соли и выделяя водород. Например, реакция железа с соляной кислотой может быть представлена следующим уравнением: Fe + 2HCl -> FeCl2 + H2. В этой реакции железо (Fe) реагирует с соляной кислотой (HCl) и образует соль железа (FeCl2) и молекулярный водород (H2).
