Железо является одним из самых распространенных элементов на Земле и имеет множество химических характеристик, которые делают его уникальным и полезным в различных областях нашей жизни. Металлическое железо имеет атомный номер 26 и химический символ Fe.
Одна из главных характеристик железа - его способность образовывать химические соединения с другими элементами. Железо может образовывать соединения с кислородом, серой, фосфором и многими другими элементами. Это позволяет использовать железо в различных промышленных и технологических процессах, а также делает его неотъемлемым элементом в составе многих веществ и материалов.
Железо также обладает химической реакционной способностью, что делает его подверженным окислению. Когда железо взаимодействует с кислородом, образуются окислы железа, которые могут быть как полезными (например, в виде ржавчины), так и вредными (например, при окислении в организме человека). Эта химическая реакционная способность приводит к необходимости защиты и консервации изделий из железа, таких как металлические конструкции и автомобили.
Важно отметить, что химические характеристики железа определяют его широкое применение в многих отраслях, таких как металлургия, строительство, машиностроение, электроника и многих других.
Таким образом, химические характеристики железа делают его уникальным и полезным элементом, не только в промышленности, но и в нашей повседневной жизни. Знание и понимание этих характеристик помогают нам использовать железо более эффективно и безопасно, а также разрабатывать новые и улучшенные материалы и технологии на его основе.
Химический состав железа

Железо – это химический элемент с атомным номером 26 и символом Fe. Оно является одним из самых распространенных элементов на Земле и составляет большую часть ядра нашей планеты. Химический состав железа обладает рядом интересных особенностей, которые определяют его уникальные свойства и применение в различных областях науки, промышленности и повседневной жизни.
Железо является благородным металлом и химически неактивно в сухом состоянии. Его активность проявляется при контакте с воздухом и влагой, когда на поверхности металла образуется тонкая слой гематита или ржавчины. Химический состав железа также включает минимум 95% железа, с незначительным содержанием других элементов, таких как углерод, марганец, сера, фосфор и кремний.
Углерод имеет значительное влияние на свойства железа и является одной из его основных примесей. Углерод может быть присутствует в железе в виде цементита или включений графита, определяющих различные типы чугуна и стальных сплавов. Марганец также часто добавляется к железу для улучшения его свойств, таких как прочность и твердость.
Железо обладает богатой историей использования человеком благодаря своим уникальным химическим и физическим свойствам. Оно применяется в производстве стальной и чугунной продукции, инструментов, машин, электроники, медицинского оборудования и многих других сферах. Обширное применение железа основано на его уникальной химической природе и способности принимать различные формы и структуры.
Физические свойства железа
Железо – это химический элемент, который обладает уникальными физическими свойствами. Одной из основных характеристик железа является его магнитная свойство. Железо является ферромагнетиком и спонтанно обладает намагниченностью. Кроме того, железо обладает высокой плотностью, что делает его одним из самых тяжелых элементов, легированных металлов.
Еще одной характеристикой железа является его высокая пластичность. Железо может быть легко обработано, что делает его идеальным материалом для различных применений, включая строительство, машиностроение и промышленную обработку. Кроме того, железо обладает высокой теплопроводностью, что позволяет использовать его в процессах с тепловым воздействием.
Железо также обладает высокой плотностью, что обеспечивает прочность и устойчивость его структуры. Это позволяет использовать железо в конструкциях, подверженных большим нагрузкам и воздействию внешних сил. Кроме того, железо обладает высокой плотностью, что делает его хорошим проводником электричества.
Таким образом, железо обладает рядом уникальных физических свойств, которые делают его одним из наиболее востребованных материалов в различных отраслях производства и строительства. Благодаря своим магнитным, пластичным, теплопроводным и прочностным свойствам, железо является незаменимым элементом для создания различных объектов и высокотехнологичных изделий.
Окисление железа воздухом

Железо является химическим элементом, склонным к окислению при взаимодействии с воздухом. Этот процесс называется окислением железа и происходит вследствие реакции железа с кислородом воздуха.
Окисление железа является необратимым процессом, при котором металл переходит в свою оксидированную форму. В результате образуются оксиды железа, такие как Fe2O3 и Fe3O4, которые известны как ржавчина. Ржавчина имеет красно-коричневый цвет и обычно образуется на поверхности железа под влиянием воздуха и влаги.
Процесс окисления железа является ускоренным в присутствии влаги и ионов кислорода. Вода играет роль электролита, а кислород из воздуха становится окислителем, протекающей электрохимической реакции. Окисление железа происходит с выделением энергии и может привести к разрушению металлической структуры.
Однако существуют способы предотвратить окисление железа. К примеру, нанесение защитных покрытий на поверхность металла, таких как покрытия из цинка или хрома, может предотвратить взаимодействие железа с окружающей средой и сохранить его металлический вид. Также возможно использование специальных антиокислительных покрытий, которые замедляют процесс окисления и защищают железо от коррозии.
Взаимодействие железа с водой

Железо является элементом, который может активно взаимодействовать с водой, образуя различные химические соединения. При контакте с водой, железо начинает процесс окисления, образуя окислы и гидроксиды.
Одним из наиболее распространенных соединений железа с водой является гидроксид железа (III), который образуется при окислении железа (III) в воде. Гидроксид железа (III) обладает характерной желто-коричневой окраской и низкой растворимостью в воде. Он может оседать в виде осадка в воде, образуя неравномерное окрашивание воды, что может привести к ее пятнистости.
Взаимодействие железа с водой также может привести к образованию ржавчины. Ржавчина – это окисленное соединение железа, которое образуется при контакте железа с водой и кислородом из воздуха. Ржавчина имеет красно-коричневую окраску и обычно имеет пористую структуру.
Кроме того, взаимодействие железа с водой может привести к изменению химического состава воды. Увеличение концентрации железа в воде может вызывать повышенную жесткость и изменение рН воды, что может негативно сказываться на ее качестве и использовании в бытовых и промышленных целях.
Химические реакции железа с кислородом
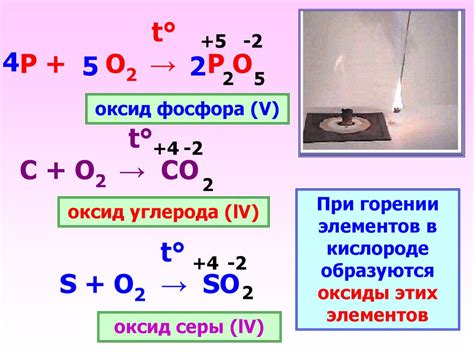
Железо является активным элементом, способным взаимодействовать с кислородом. Эти реакции играют важную роль в многочисленных процессах, таких как коррозия железа и его окисление. В результате окисления железа образуются оксиды железа, которые могут иметь различные степени окисления.
Одной из основных реакций, при которой железо окисляется кислородом, является образование ржавчины. Когда железо вступает в контакт с водой или влажным воздухом, происходит реакция между железом и кислородом из воздуха. В результате образуется гидроксид железа(III) и диоксид железа(III), которые являются основными компонентами ржавчины.
Другой важной реакцией является образование оксида железа(II). При нагревании железа в отсутствие влаги или при воздействии сильного кислорода происходит образование черного порошка, который представляет собой оксид железа(II) – FeO.
Оксид железа(III) в свою очередь образуется при воздействии сильного кислорода при высокой температуре. При этом происходит образование красно-коричневого порошка, который используется в производстве красок, стекла и других материалов.
Образование оксида железа

Оксид железа – один из самых распространенных оксидов в природе и существует в нескольких различных формах, в зависимости от конкретных условий окружающей среды. Одной из наиболее известных форм оксида железа является гематит, который образуется при окислении железа при взаимодействии с кислородом.
Образование гематита происходит на поверхности железа при взаимодействии с влажным воздухом, так как оксиген в кислороде реагирует с железом, образуя оксид железа. Этот процесс является необратимым и может занимать некоторое время в зависимости от условий окружающей среды, таких как влажность и температура.
Гематит является красным оксидом железа и обладает хорошей устойчивостью к окружающей среде. Он образует кристаллическую структуру, которая может быть использована в качестве пигмента для окраски различных материалов, включая краски и косметические продукты.
В целом, процесс образования оксида железа является важным аспектом его химических характеристик и может наблюдаться как в природных условиях, так и в промышленных процессах.
Явления коррозии железа

Железо является химически активным элементом, подверженным процессу коррозии. При воздействии кислорода и влаги происходит окисление железа, что приводит к образованию ржавчины. Коррозия железа происходит на поверхности металла, приводя к его разрушению и ухудшению свойств.
Основными факторами, влияющими на скорость коррозии железа, являются влажность, температура, наличие кислорода и различных химических веществ. В жарком и влажном климате процесс коррозии протекает более активно, поскольку вода содержит растворенные соли и кислоты, которые способствуют окислению железа.
Коррозия железа может привести к значительному снижению прочности и долговечности металлических конструкций, а также к возникновению аварийных ситуаций. Для защиты железа от коррозии применяются различные методы, такие как использование антикоррозионных покрытий, катодной защиты и химической обработки поверхностей.
Однако, даже при использовании защитных мер, невозможно полностью исключить коррозию железа. Поэтому регулярное обслуживание и ремонт металлических конструкций необходимы для обеспечения их надежности и безопасности. Также важно контролировать условия эксплуатации, чтобы минимизировать воздействие влаги и химических веществ на железо.
Роль железа в организме человека

Железо является одним из важнейших микроэлементов для организма человека. Оно играет важнейшую роль во многих процессах, происходящих в нашем теле.
Кровь и кислородообеспечение:
Железо является неотъемлемой частью красных кровяных клеток (эритроцитов), которые отвечают за транспортировку кислорода по всему организму. Это особенно важно для мышц, сердца и мозга, так как они нуждаются в постоянном поступлении кислорода для нормального функционирования.
Участие в обмене веществ:
Железо играет важную роль в метаболических процессах и обмене веществ в организме. Оно участвует в синтезе белков, а также в образовании определенных ферментов, необходимых для многих химических реакций в нашем теле.
Опора иммунной системы:
Железо играет роль в поддержании нормального функционирования иммунной системы. Оно участвует в продуцировании и активации белка трансферрина, который помогает переносить железо в крови и участвует в обороне организма от бактерий и вирусов.
Роль в нервной системе:
Железо играет важную роль в нервной системе и участвует в передаче нервных импульсов по всему телу. Оно необходимо для синтеза некоторых нейротрансмиттеров, таких как серотонин и допамин, которые влияют на наше настроение, сон и аппетит.
Важно помнить, что правильное питание и сбалансированная диета являются ключевыми факторами для поддержания нормального уровня железа в организме. Недостаток железа может привести к различным проблемам со здоровьем, таким как анемия и повышенная утомляемость.
Вопрос-ответ

Что такое химические характеристики железа?
Химические характеристики железа описывают его взаимодействие с другими элементами и соединениями, его способность окисляться или восстанавливаться, а также его реакции с кислотами и основаниями.
Какова химическая формула железа?
Химическая формула железа - Fe.
Какие соединения железа существуют?
Железо может образовывать различные соединения, такие как FeO (оксид железа(II)), Fe2O3 (оксид железа(III)), FeCl3 (хлорид железа(III)), FeSO4 (сульфат железа(II)) и многие другие.
Какие свойства железа делают его полезным в различных областях?
Железо обладает магнитными свойствами, что делает его полезным для изготовления магнитов и электромагнитов. Оно также хорошо проводит электричество и тепло, поэтому используется в проводах и конструкциях с высокой теплопроводностью. Кроме того, железо является важным компонентом гемоглобина - белка, который переносит кислород в нашем организме.
