Химическая связь – это фундаментальный понятие в химии, которое описывает силу, с помощью которой атомы и ионы простых веществ связываются друг с другом. Различные типы химической связи обладают разными характеристиками и особенностями, особенно в отношении металлических веществ. В данной статье мы рассмотрим основные типы химической связи, которые присутствуют в простых веществах металлов и рассмотрим их особенности.
Одним из наиболее распространенных типов химической связи в металлических веществах является металлическая связь. Она характеризуется тем, что атомы металла образуют кристаллическую решетку, в которой положительно заряженные ядра атомов находятся в отрицательно заряженном электронном облаке. Такая связь позволяет металлам обладать высокой электропроводностью, теплопроводностью и пластичностью. Она также позволяет металлам формировать сплавы и создавать различные конструкции.
Другим типом химической связи в металлических веществах является ионная связь. В этом случае положительно заряженные металлические ионы связываются с отрицательно заряженными не металлическими ионами. Ионные связи характеризуются высокой степенью электронного перекачивания, что обусловливает их прочность и точку плавления. Примером металла, образующего ионную связь, может служить соль, состоящая из положительно заряженных ионов металла и отрицательно заряженных ионов не металла.
Основные типы химической связи простых веществ металлов

Металлы образуют различные типы химической связи с другими атомами, что определяет их химические и физические свойства. Существуют три основных типа химической связи, которые характерны для простых веществ металлов: ионная связь, ковалентная связь и металлическая связь.
Ионная связь - это тип связи, которая образуется между металлическими и неметаллическими атомами. В этом случае металлический атом отдает один или несколько электронов неметаллическому атому, образуя положительно заряженные ионы металла и отрицательно заряженные ионы неметалла. Эти ионы притягиваются друг к другу особым образом и образуют кристаллическую решетку.
Ковалентная связь - это тип связи, который образуется между атомами металла и неметалла, когда они делят электроны. Образуется общая область, в которой электроны перемещаются между атомами. Ковалентная связь обычно является более слабой, чем ионная связь, и в простых веществах металлов может быть недостаточно сильной, чтобы образовать твердое вещество.
Металлическая связь - это тип связи, который образуется между атомами металла в металлической структуре. В этом случае свободные электроны перемещаются между положительно заряженными ядрами металлических атомов. Это делает металлы хорошими проводниками электричества и тепла.
Различные типы химической связи имеют свои особенности и влияют на свойства металлов. Ионные связи делают простые вещества металлов кристаллическими и хрупкими, ковалентные связи обеспечивают более мягкую и пластичную структуру, а металлические связи делают металлы проводниками электричества и тепла. Эти типы связей взаимосвязаны и дополняют друг друга, определяя уникальные свойства и поведение металлических веществ.
Положительное ионообменное взаимодействие

Положительное ионообменное взаимодействие является одним из основных типов связи между простыми веществами металлов. В данном типе связи образуется положительно заряженное ионное соединение, которое обладает определенными характеристиками.
Одной из особенностей положительного ионообменного взаимодействия является передача электронов от металла к другому простому веществу. Это происходит в результате образования катионов металла, которые обладают положительным зарядом и способны привлекать к себе отрицательно заряженные анионы.
В результате положительного ионообменного взаимодействия образуются ионные соединения с характерными свойствами, такими как высокая температура плавления и кристаллическая структура. Эти соединения обладают хорошей проводимостью электрического тока и отличаются высокой степенью долговечности.
Примерами положительного ионообменного взаимодействия являются соединения многих металлов, таких как натрий, калий, магний и другие. Например, катионы натрия образуют соединения с различными анионами, такими как хлорид, сульфат и нитрат. Эти соединения широко используются в промышленности и находят применение в различных областях, таких как производство стекла, пищевая промышленность, металлургия и другие.
Ковалентная связь в реакциях с неметаллами
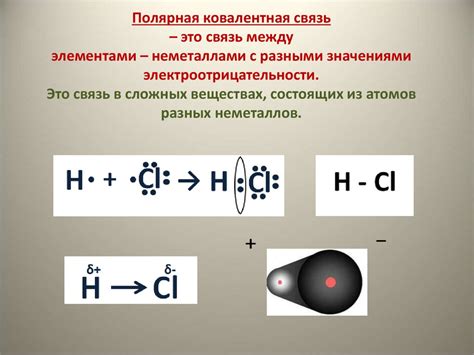
Ковалентная связь – это тип химической связи, который образуется при совместном использовании электронных пар двумя атомами. В реакциях металлов с неметаллами, металлы обычно отдают электроны неметаллам, чтобы образовать ионическую связь. Однако, некоторые неметаллы могут образовывать ковалентную связь с металлами.
Ковалентная связь между металлами и неметаллами образуется, когда электроны обоих атомов участвуют в образовании связи и они образуют общую область электронной плотности. В результате образуется молекула, в которой электроны распределены между атомами равномерно и образуют общие пары электронов.
Реакции между металлами и неметаллами с ковалентной связью могут приводить к образованию различных соединений. Например, реакция металла с кислородом может привести к образованию оксида металла. В такой реакции между атомами металла и кислорода образуется ковалентная связь, где общие пары электронов образуют область электронной плотности.
Ковалентная связь в реакциях с неметаллами обычно обладает высокой прочностью и устойчивостью. Это позволяет соединениям, образованным при таких реакциях, иметь различные свойства и использоваться в различных областях науки и техники.
Металлическое связывание в кристаллической решетке
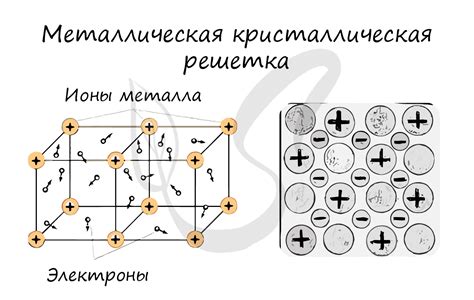
Металлическое связывание – один из основных типов химической связи в простых веществах металлов. Оно осуществляется путем образования кристаллической решетки, состоящей из положительно заряженных ионов металла и свободных электронов.
В кристаллической решетке металла каждый металлический ион окружен большим количеством свободных электронов. Эти электроны не принадлежат конкретному атому, а движутся по всей решетке, связывая весь металл внутренней структурой.
Металлическое связывание обладает рядом характеристик, отличающих его от других типов связей. Во-первых, оно обладает высокой проводимостью электричества. Благодаря наличию свободных электронов, они свободно передвигаются внутри решетки и обеспечивают электрическую проводимость материала.
Кроме того, металлическое связывание обеспечивает высокую теплопроводность материала. Свободные электроны эффективно передают тепловую энергию от одного места к другому внутри металла.
Металлическое связывание также отвечает за высокую пластичность и прочность металлических материалов. Свободные электроны обеспечивают подвижность металлических ионов, позволяя материалу легко деформироваться без разрушения структуры.
В целом, металлическое связывание является одним из ключевых факторов, определяющих химические и физические свойства металлов и делающих их важными в различных областях промышленности и технологии.
Вопрос-ответ

Какие основные типы химической связи металлов существуют?
Основными типами химической связи металлов являются ионная связь, ковалентная связь и металлическая связь.
В чем заключается ионная связь металлов?
Ионная связь металлов образуется между ионами металла и ионами неметалла или другого металла. Металл отдает электроны, становится положительно заряженным ионом, а неметалл или другой металл принимает эти электроны, образуя отрицательно заряженный ион. Таким образом возникает притяжение между положительно и отрицательно заряженными ионами, что и обуславливает ионную связь.
Что представляет собой ковалентная связь металлов?
Ковалентная связь металлов образуется между атомами металла, когда они обмениваются электронами. В результате обмена электронами образуются пары электронов, которые образуют общую электронную оболочку для атомов металла. Такая связь обладает силой, но она не так сильна, как ионная связь, и обычно характерна для комплексных соединений.
