Металлы являются одним из самых важных и распространенных классов химических элементов, которые оказывают значительное влияние на химические реакции. Их особенности и свойства делают их неотъемлемой частью многих реакций, как в природных процессах, так и в промышленности.
Одной из особенностей металлов, которая привлекает внимание исследователей, является их способность к адсорбции и катализу. Многие металлы, такие как платина, никель, железо и родий, обладают высокой каталитической активностью и используются в промышленных процессах, таких как производство удобрений, нефтепереработка и производство пластмасс.
Кроме того, металлы могут влиять на скорость и направление химических реакций. Они могут служить катализаторами, активировать реагенты и изменять кинетику реакции. Часть металлов также обладает свойством формировать комплексные соединения, которые могут быть использованы в различных отраслях промышленности и науки, от медицины до материаловедения.
Исследования в области влияния металлов на химические реакции имеют большое значение для развития новых технологий и улучшения существующих процессов. Понимание особенностей работы металлов в реакциях позволяет разрабатывать более эффективные и экологически чистые методы синтеза различных веществ и материалов.
Взаимодействие металлов с химическими веществами

Металлы обладают особыми химическими свойствами, которые определяют их взаимодействие с другими веществами. Взаимодействие металлов с химическими веществами является одной из основных областей изучения химии металлов.
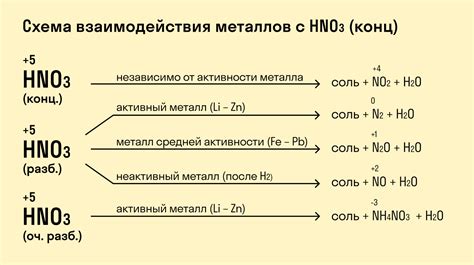
При взаимодействии металлов с кислотами происходит реакция, в результате которой образуются соли и выделяется водород. Эта реакция является характерной особенностью металлов и столь активной, что некоторые из них могут даже растворяться в кислотах. Способность металлов вступать в реакцию с кислотами определяется их электрохимическим потенциалом.
Металлы также могут вступать в реакцию с щелочными и амфотерными веществами. В результате этой реакции образуются соответствующие соли. Взаимодействие металлов с щелочными и амфотерными веществами базируется на различии в их электрохимическом потенциале и способности металлов отдавать электроны.
Кроме того, металлы могут реагировать с другими химическими веществами, такими как кислород, сера, галогены и многие другие. В результате этих реакций образуются различные соединения, которые находят применение в различных сферах, включая промышленность, медицину и научные исследования.
Изучение взаимодействия металлов с химическими веществами позволяет не только более глубоко понять химические свойства металлов, но и разработать новые методы и технологии с использованием этих свойств. Это делает изучение данной темы важной и актуальной в современной науке и промышленности.
Особенности реакций, связанных с присутствием металлов
Металлы являются активными элементами, которые часто участвуют в химических реакциях. Их влияние на реакции может быть разнообразным и проявляться в изменении скорости и направления реакции, а также в образовании сложных соединений.
Одним из важных свойств металлов является их способность к окислению (потере электронов) и восстановлению (приобретение электронов). Это позволяет металлам принимать активное участие в окислительно-восстановительных реакциях, в результате которых происходит обмен электронами между металлом и другими веществами.
Еще одним важным свойством металлов является их способность к катализу реакций. Катализаторы, содержащие металлы, повышают скорость химических реакций, не участвуя при этом в самих реакциях. Они способны изменять активационную энергию реакции, снижая ее значение, что делает реакцию более быстрой и эффективной.
Взаимодействие металлов с кислотами также является важным аспектом химических реакций. Металлы образуют с кислотами соли, при этом происходит обмен ионами. Такие реакции приводят к образованию новых веществ и могут быть использованы в промышленности и в жизни человека.
Еще одним интересным аспектом реакций с металлами является их влияние на органические реакции. Металлы могут служить катализаторами в органических синтезах, способствуя образованию новых соединений. Они также могут быть включены в структуру органических молекул и изменять их свойства и активность.
Значение металлов в химических преобразованиях
Металлы играют ключевую роль во множестве химических реакций и преобразованиях. Одним из основных свойств металлов является их способность служить катализаторами - веществами, которые активируют химические реакции, ускоряют их и позволяют происходить при низкой температуре и давлении.
Металлические катализаторы широко применяются в промышленности для производства различных продуктов. Они могут использоваться для синтеза органических соединений, окислительных и восстановительных реакций, полимеризации и других процессов. Катализаторы на основе металлов позволяют снизить энергетическую стоимость процесса и повысить выход целевого продукта.
Кроме того, металлы могут принимать участие в реакциях, образуя комплексы или соединения с другими веществами. Например, металлы часто действуют как активные электроды в электрохимических реакциях, где они переходят из одной степени окисления в другую.
Важно отметить, что каждый металл вносит свои особенности в реакцию. Некоторые металлы могут обеспечивать высокую активность и стабильность при каталитическом действии, в то время как другие могут быть более селективными, что позволяет получать специфические продукты. Также металлы могут оказывать влияние на скорость реакции, ее механизм или равновесие.
Использование металлов в химических преобразованиях является одним из важных направлений современной химии. Оно позволяет не только эффективно проводить различные реакции, но и улучшать экологическую безопасность процессов, снижая их вредное воздействие на окружающую среду.
Вопрос-ответ

Как металлы влияют на химические реакции?
Металлы могут влиять на химические реакции различными способами. Например, они могут служить катализаторами, ускоряющими реакции. Также, металлы могут изменять окислительно-восстановительные свойства веществ. Они могут участвовать в реакциях переноса электронов и образовывать хелатные соединения, что также может влиять на ход реакции.
Какие именно металлы могут быть использованы в качестве катализаторов?
Многие металлы могут быть использованы в качестве катализаторов. Некоторые из них, такие как платина, палладий и родий, широко применяются в промышленности. Они обладают высокой каталитической активностью и стабильностью. Кроме того, редкоземельные металлы, такие как иттрий и лантан, также могут служить катализаторами.
Как металлы влияют на окислительно-восстановительные реакции?
Металлы могут изменять окислительно-восстановительные свойства веществ. Например, они могут служить в качестве окислителя или восстановителя в реакциях с другими веществами. Некоторые металлы могут образовывать различные заряженные ионы, что также может влиять на окислительно-восстановительные свойства реагентов.
Какие хелатные соединения могут образовываться с участием металлов?
Металлы могут образовывать хелатные соединения с различными лигандами. Например, они могут образовывать хелатные соединения с аминокислотами, этилендиамином, глицином и многими другими органическими соединениями. Хелатные соединения металлов обладают особыми свойствами и могут быть использованы в различных химических реакциях и процессах.
Каким образом металлы могут быть использованы в промышленности?
Металлы имеют широкий спектр применений в промышленности. Они используются в производстве металлических изделий, строительных конструкций, электроники и техники. Кроме того, металлы могут служить катализаторами в химической промышленности, участвовать в процессах очистки воды и воздуха. Они также используются в производстве лекарственных препаратов и пищевых добавок.
