Химическая коррозия металлов - это процесс разрушения металлических материалов под влиянием химических реакций с окружающей средой.
Взаимодействие металлов с различными веществами, такими как вода, кислород, кислоты или соли, может приводить к образованию химических соединений на поверхности металла и изменению его свойств. Такие изменения могут привести к потере прочности, нарушению работы механизмов или даже полному разрушению конструкции.
Причины химической коррозии металлов могут быть разнообразными. Некоторые металлы, такие как железо, реагируют с кислородом из воздуха, образуя оксиды, которые могут быть легко разрушены водой или кислотами. Другие металлы, такие как алюминий или цинк, могут образовывать защитные слои оксидов на своей поверхности, которые могут предотвратить дальнейшую коррозию.
Химическая коррозия металлов может привести к серьезным проблемам в промышленности и повседневной жизни. Поэтому разработка методов защиты от коррозии и поиск устойчивых материалов является важной задачей для многих отраслей науки и техники.
Механизм химической коррозии включает в себя ряд стадий. Сначала происходит адсорбция агрессивного среды на поверхность металла, затем инициируется реакция между металлом и агентом коррозии, образуются соединения и образуется коррозионный продукт. Этот продукт может быть растворен или остаться на поверхности, создавая защищающую пленку или слой.
В целом, понимание причин и механизмов химической коррозии металлов позволяет разрабатывать эффективные методы предотвращения и защиты от коррозии, что способствует увеличению срока службы металлических изделий и обеспечению их надежности и безопасности.
Влияние окружающей среды:

Окружающая среда играет важную роль в процессе химической коррозии металлов. Она может содержать различные вещества, которые могут вызывать коррозию и разрушение металлических конструкций.
Вода является одной из основных причин химической коррозии металлов. Обычная пресная вода содержит растворенные соли, кислород и другие вещества, которые могут образовывать электролиты и проводить электрический ток. Это приводит к возникновению гальванической коррозии, при которой один металл становится анодом, а другой катодом, что приводит к разрушению анодного металла.
Воздух также может быть причиной коррозии металлов. В атмосфере содержатся различные газы, такие как кислород и сероводород, которые могут проникать через поры в защитном слое на поверхности металла и вызывать его окисление. Это особенно важно для металлов, таких как железо и сталь, которые являются основными строительными материалами и повсеместно используются в различных конструкциях и изделиях.
Кроме того, промышленные и химические загрязнения, такие как кислотные или щелочные вещества, могут также способствовать химической коррозии металлов. Эти загрязнения могут образовывать агрессивные среды, которые разрушают защитные покрытия на поверхности металла и проникают в его структуру.
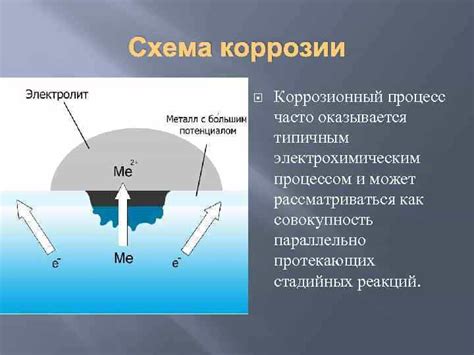
Электрохимический процесс:
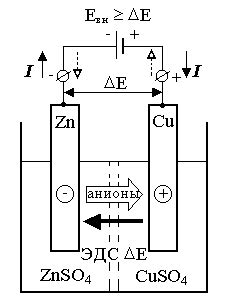
Электрохимическая коррозия металлов является результатом электрохимических процессов, которые происходят при контакте металла с окружающей средой. Этот процесс основан на химической реакции, при которой металл переходит в ионное состояние и образует гальваническую пару с окружающим веществом.
Коррозию металла можно представить как два основных процесса: анодный и катодный. В анодном процессе металл окисляется и переходит в ионное состояние, отдавая электроны в окружающую среду. В катодном процессе ионы окружающего вещества принимают электроны и редуцируются, возвращая металл в его исходное состояние.
Важным фактором, влияющим на электрохимический процесс коррозии, является разность потенциалов между анодом и катодом. Если данная разность высока, то коррозия будет более интенсивна, так как процесс перехода электронов будет более быстрым. К разности потенциалов также приводит наличие различных элементов, растворенных в окружающей среде и образующих гальванические связи с металлом.
Процесс электрохимической коррозии является необратимым и приводит к разрушению металлической структуры. Для защиты от коррозии металлы покрывают непроводящими покрытиями, которые препятствуют контакту металла с окружающей средой и тем самым замедляют электрохимический процесс.
Реакции со средой:

Металлы, находясь в окружающей среде, подвержены воздействию различных факторов, в результате чего могут происходить химические реакции с окружающей средой, приводящие к их коррозии. Реакции металлов с окружающей средой могут быть разносторонними и зависят от множества факторов.
Одним из признаков химической коррозии является образование ржавчины. Ржавчина образуется при окислении железа или его сплавов с воздухом и влагой. В процессе реакции между металлом и окружающей средой образуются оксиды и гидроксиды металла, которые обычно имеют плохую адгезию к металлической поверхности и способствуют дальнейшей коррозии.
Окисление металлов также может происходить под воздействием кислорода, который содержится в атмосфере. Кислород обладает высокой реакционной способностью и может проникать через поры в металлической поверхности, вызывая окисление металла. Это приводит к образованию оксидной пленки на поверхности металла, которая может быть нежелательна и способствовать дальнейшей коррозии.
На реакцию металлов с окружающей средой также влияет pH среды. Например, некоторые металлы корродируют при нейтральном или щелочном pH, в то время как другие металлы корродируют при кислом pH. Реакции металлов с кислотными или щелочными средами могут приводить к разрушению металла и образованию соответствующих солей и оксидов.
Также стоит отметить, что реакции металлов с окружающей средой могут быть катализированы другими веществами, содержащимися в окружающей среде. Например, некоторые ионы могут ускорять процесс коррозии металлов, действуя как катализаторы в реакции.
Окисление и редукция:
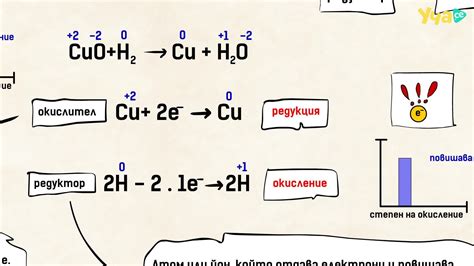
Окисление и регукция – это основные процессы, которые протекают при химической коррозии металлов. Окисление – это процесс, при котором металл взаимодействует с кислородом или другим окислителем. При окислении металла происходит потеря электронов, что приводит к образованию ионов металла. Это ионы образуют окислы металла, которые обычно представлены в реакциях окисления металла с кислородом.
Редукция – это процесс, обратный окислению. Во время редукции металл принимает электроны, ионы металла превращаются в металлическую форму. Этот процесс часто происходит при взаимодействии металла с веществами, способными отдавать электроны. Такие вещества называются восстановителями. Одной из наиболее распространенных реакций редукции в химической коррозии является реакция редукции кислорода, где металл принимает электроны от кислорода, образуя окись металла.
Окисление и редукция играют ключевую роль в химической коррозии металлов. При взаимодействии с окислителями, металлы подвергаются окислению, что приводит к разрушению их структуры. Результом этого процесса является образование окисей металла, которые обычно представляют собой нежелательные продукты коррозии. Однако, редукционные реакции также могут протекать при химической коррозии, что может приводить к образованию восстановленных металлических поверхностей.
Факторы, влияющие на скорость коррозии:
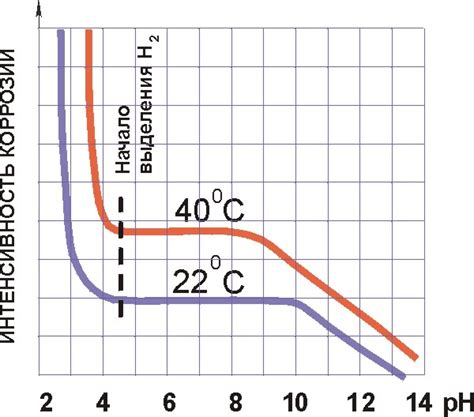
1. Концентрация раствора. Чем выше концентрация раствора окислителя, тем быстрее протекает процесс коррозии. Избыточное количество окислителя создает условия для более активной работы анодных реакций, что приводит к повышенной скорости коррозии.
2. Температура. Повышение температуры вещества способствует активации коррозионных процессов. При повышенной температуре молекулы становятся более подвижными и быстрее взаимодействуют друг с другом, что увеличивает скорость разрушения металла.
3. Влажность. Присутствие влаги является важным предпосылкой для развития коррозии. Влага обеспечивает проводимость электролита и обеспечивает основную среду для протекания электрохимических реакций на поверхности металла.
4. Окружающая среда. Коррозию металлов ускоряют окружающие факторы. Например, наличие агрессивных химических веществ, вредных газов, солей и т.д. При взаимодействии металла с такими веществами происходит активное разрушение его поверхности.
5. Механическое воздействие. Механическое воздействие на поверхность металла может привести к разрушению защитного слоя и позволить коррозии активно развиваться. Например, трение, удары, нагрузки могут вызывать микротравмы и микротрещины, через которые проникают агрессивные среды, способствуя коррозии.
Все эти факторы взаимодействуют друг с другом, поэтому при оценке скорости коррозии необходимо учитывать все упомянутые влияющие факторы и применять соответствующие меры предотвращения и защиты от коррозии.
Роль влаги в коррозии:
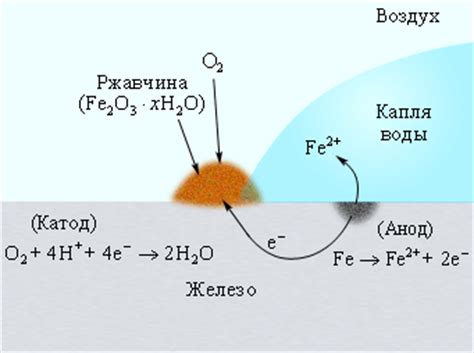
Влага играет одну из ключевых ролей в процессе химической коррозии металлов. Она является средой, которая способствует химическим реакциям, приводящим к разрушению материала. Попадая на поверхность металла, влага активно взаимодействует с диссоцирующимися веществами, содержащимися в окружающей атмосфере, образуя различные химические соединения.
Например, влага может просто растворить некоторые компоненты металла, снижая его прочность и устойчивость к разрушению. Кроме того, влага может образовывать электролитическую среду, в которой происходят электрохимические реакции коррозии. При наличии влаги происходит образование гальванических элементов, в которых разные участки металла служат катодом и анодом.
На поверхности металла влага может вызывать концентрационную поляризацию, что приводит к ускоренной коррозии. При этом на катодном участке поверхности металла происходит снижение pH, а на анодном - повышение pH. Такое разделение потенциалов способствует появлению коррозионных реакций.
Влага также способствует формированию коррозионной среды внутри микротрещин или пор на поверхности металла. Она может проникать внутрь материала и вызывать коррозию внутри него. В том числе влага может быть включена в химические реакции коррозии, вызывая механическое разрушение металла.
Примеры причин и механизмов коррозии:
Кислотные среды: Кислотная коррозия металлов происходит в результате взаимодействия металла с кислотой. Например, при контакте металла с соляной кислотой образуются хлориды, которые разрушают структуру металла и вызывают его коррозию.
Активная металлическая среда: Коррозия может происходить под влиянием активных металлов, таких как медь или цинк. Например, при контакте меди с железом происходит гальваническая коррозия, которая приводит к разрушению железа.
Процессы окисления-восстановления: Коррозия металлов может происходить в результате окисления и восстановления металлических частиц. Например, при контакте железа с влажным воздухом происходит образование ржавчины, которая разрушает структуру железа.
Электролиты: Коррозию металлов могут вызывать различные электролиты, такие как соли или кислотные растворы. Например, при контакте металла с раствором соли происходит электролитическая коррозия, что приводит к разрушению металла.
Механическое воздействие: Механическое воздействие на металлы, такое как трение или удары, может вызывать коррозию. Например, при трении металлической поверхности может происходить истирание защитного покрытия металла и его последующая коррозия.
Биологические факторы: Коррозия металлов может быть вызвана воздействием биологических факторов, таких как микроорганизмы или водоросли. Например, при воздействии микроорганизмов на металл может происходить образование коррозионных продуктов, что приводит к появлению коррозии.
Методы противодействия коррозии:

1. Защитные покрытия: Одним из наиболее распространенных методов борьбы с химической коррозией металлов является нанесение защитных покрытий на поверхность металла. Такие покрытия создают барьер между металлом и средой, предотвращая контакт с агрессивными веществами. Примерами таких покрытий могут быть краска, лак, эмаль и гальваническое покрытие, такое как цинкование или хромирование.
2. Использование коррозионно-стойких металлов: Еще одним способом борьбы с коррозией является выбор металлов, которые самостоятельно обладают высокой устойчивостью к химической коррозии. Некоторые примеры таких металлов включают нержавеющую сталь, алюминий и титан. Эти металлы имеют специальные добавки, которые улучшают их устойчивость к коррозии.
3. Катодная защита: Катодная защита является электрохимическим методом борьбы с коррозией металлов. Он основан на принципе уменьшения потенциала метала в результате подключения катодных защитных средств. В результате этого процесса металл выступает как анод и его коррозия снижается. Этот метод часто используется для защиты подводных металлических конструкций и трубопроводов.
4. Установка анодов: Другим способом борьбы с коррозией является установка анодов. Аноды, выполненные из материала с более высоким потенциалом коррозии, привлекают агрессивные ионные вещества, предотвращая их взаимодействие с металлом. Это позволяет сохранять коррозионную стабильность металла. Установка анодов широко применяется в судостроении и нефтегазовой промышленности.
5. Подбор среды: Последним методом противодействия коррозии является контроль выбора среды, с которой металл будет взаимодействовать. Избегание контакта металла с агрессивными средами или снижение их концентрации может уменьшить вероятность коррозии. Контроль показателей, таких как влажность, pH и содержание химических веществ в среде, может предотвратить коррозию металла и повысить его долговечность.
Вопрос-ответ

Какие причины вызывают химическую коррозию металлов?
Химическая коррозия металлов вызывается взаимодействием металла с окружающей средой, в основном, с водой или влажным воздухом. Главные причины коррозии - воздействие кислорода, присутствие солей и кислот, высокая температура и давление.
Какие механизмы происходят при химической коррозии металлов?
При химической коррозии металлов происходят различные механизмы, но основными являются окисление металла и растворение его ионов в реакции с окружающей средой. Окисление металла происходит под воздействием кислорода или других оксидантов, а растворение его ионов зависит от pH окружающей среды.
Какие металлы наиболее подвержены химической коррозии?
В разной степени металлы подвержены химической коррозии, но наиболее восприимчивыми к коррозии являются железо, алюминий, цинк и их сплавы. Они реагируют с водой и влажным воздухом, образуя оксиды и гидроксиды, которые затем растворяются и вызывают разрушение металла.
Какие методы защиты от химической коррозии металлов существуют?
Существует несколько методов защиты от химической коррозии металлов. Один из них - использование покрытий, таких как краска, лак или порошковое напыление, которые создают барьер между металлом и окружающей средой. Другой метод - использование анодной защиты, при которой металл делается анодом в гальванической паре с другим металлом, что позволяет уменьшить скорость коррозии. Также существуют методы использования специальных добавок или антикоррозионных покрытий на металле.
Какие последствия может иметь химическая коррозия металлов?
Химическая коррозия металлов может иметь серьезные последствия, такие как потеря прочности и устойчивости металла, образование трещин и деформаций, изменение внешнего вида и эстетических характеристик изделия, а также повышение вероятности аварий и неисправностей. Кроме того, коррозия может привести к загрязнению окружающей среды и угрозе для здоровья человека.
