Щелочноземельные металлы образуют ряд химических соединений, среди которых имеют особое значение оксиды. Оксиды щелочноземельных металлов обладают свойством образовывать ионы щелочноземельных металлов при взаимодействии с водой или кислыми оксидами.
Характер оксидов щелочноземельных металлов определяется их основными свойствами. В основном они являются щелочными оксидами, то есть образуют основы, реагирующие с кислотами. При этом образование основ происходит посредством образования ионов гидроксида щелочноземельного металла или ионов металла в соответствующем оксиде.
Другой особенностью оксидов щелочноземельных металлов является их амфотерность, то есть способность проявлять свойства и кислот, и оснований. Это свойство определяется наличием дифференциальных электронов в валентной оболочке металлов. Через разные химические реакции оксиды щелочноземельных металлов могут образовывать соли кислот или соли оснований.
Свойства и особенности оксидов щелочноземельных металлов

Щелочноземельные металлы, такие как бериллий, магний, кальций, стронций, барий и радий, образуют оксиды с характерными свойствами и особенностями.
Оксиды щелочноземельных металлов обычно обладают высокой термической стабильностью и высокой температурой плавления. Они образуют кристаллические структуры и имеют регулярную решетку.
Оксиды щелочноземельных металлов обладают щелочным характером и реагируют с водой, образуя гидроксиды. Эта реакция сопровождается выделением тепла. Некоторые оксиды, такие как оксид магния (MgO), обладают щелочными и кислотными свойствами и могут реагировать как основание и кислота в различных реакциях.
Кроме того, оксиды щелочноземельных металлов могут образовывать различные полиморфные формы, то есть существовать в разных кристаллических структурах. Например, оксид бериллия (BeO) может образовать кристаллическую структуру в центросимметричной гексагональной форме или структуру кубической решетки.
В целом, свойства и особенности оксидов щелочноземельных металлов определяют их важную роль в различных применениях, таких как использование в производстве керамики, электроники, катализа и других отраслях промышленности.
Реактивность оксидов щелочноземельных металлов
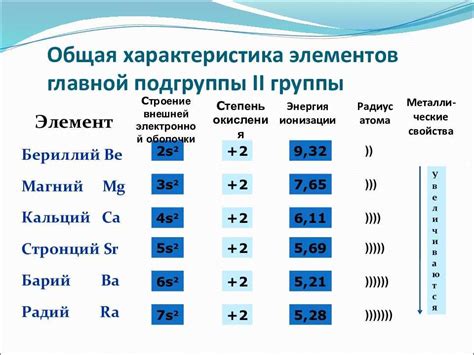
Оксиды щелочноземельных металлов обладают различной реактивностью в зависимости от элемента, к которому они принадлежат. Реактивность оксидов зависит от их структуры и электрохимических свойств.
Одной из особенностей оксидов щелочноземельных металлов является их способность к реакции с водой. Некоторые оксиды, например оксид кальция (CaO) и оксид магния (MgO), обладают базовыми свойствами и образуют щелочные растворы при взаимодействии с водой. Такие оксиды называют гидроксидасами. Кроме того, они могут реагировать с кислотами, образуя соли и воду.
Другие оксиды щелочноземельных металлов, например оксид бериллия (BeO), обладают амфотерными свойствами и могут реагировать как с кислотами, так и с щелочами. Некоторые оксиды, например оксид стронция (SrO) и оксид бария (BaO), образуют то основные, то амфотерные соединения в зависимости от условий реакции.
Реактивность оксидов щелочноземельных металлов может быть связана также с их способностью к каталитическим реакциям, например оксид кальция может использоваться в качестве катализатора в процессах внутреннего сгорания. Кроме того, некоторые оксиды, например оксид стронция, обладают фотокаталитической активностью и могут применяться для очистки воздуха от вредных примесей.
Физико-химические свойства оксидов щелочноземельных металлов

Оксиды щелочноземельных металлов являются неорганическими соединениями, состоящими из атомов металла и кислорода. Они обладают рядом характеристических физико-химических свойств, которые определяют их поведение в различных условиях.
Во-первых, оксиды щелочноземельных металлов обычно являются твердыми веществами при комнатной температуре и давлении. Они обладают высокой температурой плавления и кипения, что связано с наличием межатомных связей и кристаллической структуры.
Во-вторых, оксиды щелочноземельных металлов обладают щелочными свойствами, то есть они способны образовывать гидроксиды в результате реакции с водой. Это связано с высокой электроотрицательностью кислорода и электроположительностью металлов, что позволяет образовывать ионы OH- и положительные металлические ионы.
В-третьих, оксиды щелочноземельных металлов способны растворяться в кислотах, образуя соли и воду. Это связано с процессом нейтрализации, при котором ионы гидроксида окисляются кислородом, а ионы металла образуют соль.
И наконец, оксиды щелочноземельных металлов обладают хорошей электропроводностью. Они являются ионными соединениями, где металлические ионы передают электроны, создавая электронные потоки и проявляя свойства электролитов.
Применение оксидов щелочноземельных металлов

Оксиды щелочноземельных металлов, такие как оксид кальция (CaO), оксид магния (MgO) и оксид бария (BaO), находят широкое применение в различных отраслях промышленности.
1. Строительство и производство материалов.
Оксид кальция и оксид магния используются в производстве цемента, керамики, стекла и других строительных материалов. Они обладают высокой теплостойкостью и способностью устойчиво проявлять свои свойства при высоких температурах. Кроме того, эти оксиды являются основными компонентами известкового строительного раствора, используемого при кладке кирпичных и каменных стен.
2. Сельское хозяйство.
Оксид кальция применяется в сельском хозяйстве для обработки почвы и улучшения ее структуры. Он способствует нейтрализации кислых почв, повышает растворимость питательных веществ, улучшает доступность их для растений. Оксид магния также используется как минеральное удобрение для компенсации дефицита магния в почвах.
3. Производство стали и сплавов.
Оксид кальция, оксид магния и оксид бария используются в процессе выплавки стали и производства сплавов. Они служат для удаления примесей, снижения содержания серы и фосфора в металле, повышения его прочности и термической стабильности.
4. Пищевая промышленность.
Оксид кальция и оксид магния используются в пищевой промышленности в качестве пищевых добавок. Они используются для регулирования кислотности продуктов, стабилизации текстуры и улучшения вкусовых качеств. Оксид бария также может использоваться в пищевой промышленности при производстве некоторых видов кондитерских изделий и консервов.
Взаимосвязь свойств оксидов щелочноземельных металлов
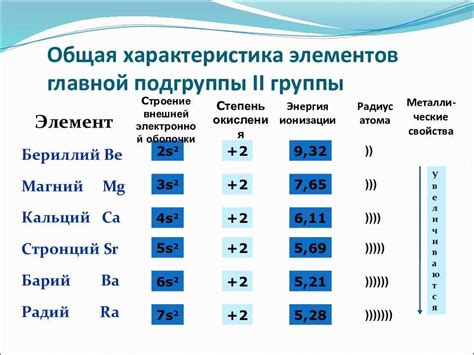
Оксиды щелочноземельных металлов, таких как бериллий, магний, кальций и другие, обладают рядом характеристических свойств, определяющих их взаимосвязь.
Во-первых, щелочноземельные оксиды обычно обладают высокой температурой плавления и кипения. Это объясняется их кристаллической структурой и силой химических связей между атомами металлов и кислородом.
Во-вторых, оксиды щелочноземельных металлов являются основными соединениями и образуют гидроксиды при реакции с водой. Гидроксиды щелочноземельных металлов обычно являются сильными основаниями и обладают щелочными свойствами, что приводит к образованию щелочей.
В-третьих, щелочноземельные оксиды часто обладают высокими щелочностью и щелочностью. Это связано с их способностью образовывать основоподобные растворы при реакции с водой и образовывать соли, которые могут быть использованы в различных индустриальных и научных применениях.
В-четвертых, оксиды щелочноземельных металлов обладают теплопроводностью и электропроводностью. Это связано с наличием свободных электронов между атомами вещества, которые способны передавать энергию и электрический заряд.
Таким образом, свойства оксидов щелочноземельных металлов тесно связаны между собой и обеспечивают им специфические характеристики, определяющие их роль и применение в различных областях науки и техники.
Вопрос-ответ

Какие свойства характерны для оксидов щелочноземельных металлов?
Оксиды щелочноземельных металлов обладают высокой щелочностью и летучестью. Они также обладают высокой термической стабильностью, устойчивостью к окислению и влажности.
Какие особенности имеют оксиды щелочноземельных металлов?
Одной из особенностей оксидов щелочноземельных металлов является их способность образовывать растворимые гидроксиды при контакте с водой. Кроме того, они имеют высокую теплопроводность и химическую инертность.
В чем отличие оксидов щелочноземельных металлов от оксидов щелочных металлов?
Основное отличие заключается в химической активности. Оксиды щелочноземельных металлов менее активны, чем оксиды щелочных металлов. Они также обладают более высокой кислотностью и меньшей растворимостью в воде.
Какова роль оксидов щелочноземельных металлов в промышленности?
Оксиды щелочноземельных металлов широко используются в промышленности в качестве катализаторов, добавок для стекла и керамики, а также для производства щелочей и щелочных металлов.
Какие применения имеют оксиды щелочноземельных металлов в быту?
Оксиды щелочноземельных металлов используются в быту в качестве основных компонентов бытовых продуктов, таких как стекло, мыло, моющие средства и многое другое.
