Водород — один из наиболее распространенных элементов в природе, и его взаимодействие с металлами имеет большое значение в различных областях науки и техники. Водород может быть абсорбирован металлами, что приводит к изменению их механических, физических и химических свойств. Это взаимодействие является результатом сложных физико-химических процессов и может происходить при различных условиях и в разных масштабах. Понимание принципов взаимодействия водорода с металлами не только помогает в разработке новых материалов, но и является основой для создания эффективных систем хранения и использования водорода в различных отраслях промышленности.
Взаимодействие водорода с различными металлами может происходить по нескольким основным механизмам. Один из них - абсорбция водорода атомарными или молекулярными металлами. В этом случае водород встраивается в решетку металла и может существовать в нем в различных формах. Взаимодействие водорода с металлами также может происходить посредством образования химических соединений, например, с образованием металлических гидридов. Большинство металлических гидридов обладают уникальными свойствами, такими как высокая плотность водорода или способность выделять его при нагревании.
Вода - источник водорода, и ее взаимодействие с металлами также играет важную роль. При этом возможно образование оксидов и гидроксидов металлов, которые впоследствии могут взаимодействовать с водородом. Понимание этих сложных процессов позволит разработать новые материалы и технологии, основанные на использовании водорода в качестве недорогого, экологически чистого и перспективного источника энергии.
Взаимодействие водорода с металлами

Водород – это исключительно легкий газ, который обладает рядом интересных свойств и способен взаимодействовать с различными элементами. Особый интерес представляет его взаимодействие с металлами, которое может протекать при определенных условиях.
При взаимодействии водорода с металлами происходит образование металлогидридов. Водородный катион встраивается в кристаллическую решетку металла, образуя стабильное соединение. Это взаимодействие зависит от различных факторов, включая свойства металла, концентрацию водорода и температуру.
Водород способен растворяться в множестве металлов, таких как железо, никель, титан и другие. Образование металлогидридов может изменять свойства металла, влияя на его прочность, электропроводность и другие характеристики. Многие металлогидриды обладают способностью поглощать и выделять водород в процессе отдачи и поглощения тепла, что может быть использовано в различных технологических и энергетических процессах.
Основное применение водорода взаимодействия с металлами связано с его свойствами в качестве энергоносителя. Например, водород может использоваться для производства электроэнергии в горючих элементах, где происходит окисление водорода и образование воды. Также, водород может быть использован в процессах хранения и передачи энергии, что делает его перспективным вариантом для использования в новых энергетических технологиях.
Итак, взаимодействие водорода с металлами является актуальной и интересной темой и может иметь широкие практические применения. Исследования в этой области позволяют улучшить свойства металлов и создать новые технологии, основанные на энергетическом потенциале водорода.
Водород и реакции:
Водород является самым легким и распространенным химическим элементом во вселенной. Он обладает уникальными свойствами и способен образовывать различные соединения, включая реакции с металлами.
Реакция между водородом и металлами происходит под воздействием высокой температуры и/или давления. В результате этой реакции образуется соединение между водородом и металлом - гидрид. Гидриды металлов могут быть как стехиометрические, так и нестехиометрические.
Стехиометрические гидриды образуются при точном соотношении между металлом и водородом. Такие гидриды обладают определенной структурой и принадлежат к классу металлогидридов. Они обычно характеризуются высокой стабильностью и наличием слабой химической связи между металлом и водородом.
Нестехиометрические гидриды, в свою очередь, имеют переменное соотношение между металлом и водородом. Такие гидриды обычно обладают сложной структурой и более высокой активностью. Нестехиометрические гидриды могут быть полезными в качестве активных катализаторов или источников водорода в различных химических процессах.
Водородные реакции с металлами могут иметь как положительное, так и отрицательное влияние. Например, нестабильные гидриды металлов могут вызывать нежелательные эффекты, такие как разрушение материалов или коррозия. С другой стороны, водородные реакции могут быть использованы для создания новых материалов или применения в области энергетики, в частности, для производства водородных топливных элементов.
Металлический водород

Металлический водород – это экзотическое вещество, которое обладает свойствами как металла, так и водорода. Однако его существование и свойства до сих пор достаточно сложно исследовать и понять.
Образование металлического водорода возможно при высоких давлениях и низких температурах. При достижении определенного давления водород переходит в состояние металла, приобретая характерные свойства, такие как проводимость электричества и тепла, а также магнитные свойства.
Особенностью металлического водорода является его сверхпроводимость. При определенных условиях он способен подавлять электрическое сопротивление и вести электрический ток без потерь. Это свойство делает металлический водород интересным для применения в технологии суперпроводников.
Металлический водород также обладает возможностью активного взаимодействия с различными металлами. При этом может происходить образование сплавов и структурных изменений, которые могут влиять на физические и химические свойства металлов. Исследование взаимодействия водорода с различными металлами имеет практическое значение и может найти применение в создании новых материалов и технологий.
Водород и щелочные металлы

Щелочные металлы (литий, натрий, калий, рубидий, цезий) обладают особой реакционной способностью к водороду. Взаимодействие водорода с щелочными металлами происходит при обычных условиях и сопровождается выделением энергии.
Водород и щелочные металлы образуют соли гидридов с общей формулой MH, где M - щелочный металл. Эти гидриды являются ионными соединениями, в которых водородный атом приобретает отрицательный заряд.
Взаимодействие водорода с щелочными металлами является эндотермическим процессом, то есть для его осуществления требуется поступление энергии. Оно происходит при нагревании металла или при его контакте с катализаторами, как, например, палладий или никель.
Водород и щелочные металлы широко используются в различных отраслях промышленности. Например, металлический натрий служит основой для производства гидрида натрия, который применяется как источник водорода в водородных батареях и в процессе окислительно-восстановительных реакций. Кроме того, металлический литий используется в производстве аккумуляторов, а калий - в сельском хозяйстве в качестве удобрения для растений.
Взаимодействие водорода с переходными металлами

Переходные металлы обладают способностью активно взаимодействовать с водородом, образуя различные соединения. В частности, многие переходные металлы способны образовывать гидриды – соединения с водородом.
Образование гидридов переходных металлов может происходить при нагревании металла с водородом или путем поглощения водорода из газовой фазы. Гидриды переходных металлов имеют различные свойства и используются в различных областях, например, в качестве катализаторов в химической промышленности или в процессе синтеза сплавов с различными свойствами.
Одним из наиболее известных гидридов переходных металлов является гидрид никеля, который образуется при взаимодействии никеля с водородом. Гидрид никеля обладает высокой поглощающей способностью и используется в различных промышленных процессах, таких как водородный поглотитель в системах очистки водорода.
Взаимодействие водорода с переходными металлами также может приводить к образованию сплавов. Сплавы водорода с переходными металлами имеют различные свойства и могут применяться в различных отраслях науки и промышленности, включая электронику, металлургию и энергетику.
Водород и легкие металлы

Водород – самый легкий элемент во всей таблице Менделеева, а легкие металлы, такие как литий, натрий, калий и цезий, это группа элементов, которые относятся к первой группе периодической системы. Эти элементы проявляют особый интерес в контексте своего взаимодействия с водородом.
Легкие металлы обладают высокой химической активностью, что позволяет им образовывать соединения с водородом при комнатной температуре и давлении. Водородактивные металлы, такие как литий и натрий, легко реагируют с водой и выделяют водородный газ. Данная реакция протекает гораздо быстрее, чем аналогичная реакция с тяжелыми металлами, такими как железо или свинец.
Водород может вступать в реакцию с легкими металлами не только в водной среде, но и при нагревании. При этом образуются гидриды – соединения водорода с металлами. Гидриды легких металлов обладают рядом полезных свойств, таких как высокая теплопроводность и пониженное электрическое сопротивление, что позволяет использовать их в различных областях, включая производство аккумуляторов и поглощение водорода.
Однако, взаимодействие водорода с легкими металлами также может иметь отрицательные последствия. Например, повышенная активность водорода может привести к коррозии металла или вызвать его растрескивание. Поэтому, в контексте использования водорода с легкими металлами в индустрии и других областях, необходимо учитывать все особенности данного взаимодействия и применять соответствующие меры предосторожности.
Ковалентные связи с водородом
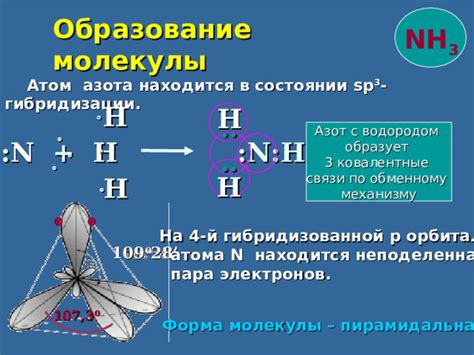
Ковалентные связи - это вид химической связи между атомами, при котором электроны распределены между ними общим образом. Водород образует ковалентные связи с различными металлами, что позволяет образованию соединений с различными свойствами.
Одним из примеров ковалентных связей с водородом является соединение между водородом и металлом натрием. В этом случае водород образует связь с натрием, в результате которой образуется соединение NaH. Эта связь является ковалентной, так как электроны в этой связи распределены между атомами общим образом, создавая стабильное соединение.
Ковалентные связи с водородом также характерны для соединений с металлами более высокого порядка. Например, при взаимодействии водорода с атомами магния образуется соединение MgH2. В этом случае два атома водорода образуют ковалентные связи с атомом магния, обеспечивая стабильность соединения.
Ковалентные связи с водородом играют важную роль в различных процессах, таких как каталитические реакции и производство аммиака. Благодаря этому типу связи возможно образование различных соединений с металлами, что расширяет возможности использования водорода в различных областях науки и техники.
Вопрос-ответ

Как водород взаимодействует с металлами?
Водород может взаимодействовать с металлами различными способами, включая адсорбцию, абсорбцию и десорбцию.
Какие металлы способны адсорбировать водород?
Многие металлы могут адсорбировать водород, включая платину, никель, палладий, радий и др.
Что происходит при абсорбции водорода металлом?
При абсорбции водорода металлом происходит проникновение молекул водорода во внутреннюю структуру металла.
Какие металлы способны абсорбировать водород?
Металлы, способные абсорбировать водород, включают титан, цирконий, цирий, магний и другие.
Как водород взаимодействует с алюминием?
Водород может реагировать с алюминием, образуя алюминиевые гидриды, которые используются, например, в батареях.
