Соляная кислота (хлороводородная кислота) HCl - одна из самых распространенных и знакомых нам кислот. Ее отношение к железу – тема, заслуживающая особого внимания. Железо Fe, находящееся в контакте с соляной кислотой, может вызывать различные реакции, обладает интересными свойствами и широко применяется в различных областях жизни.
Соляная кислота обладает резким запахом, она является сильным водяным растворителем и носителями H+ (водородных ионов). При контакте с железом соляная кислота вызывает реакцию. Железо при этом проявляет свою активность и способность образовывать соединения с различными веществами.
При контакте соляной кислоты с железом, происходит реакция образования хлорида железа FeCl2 (железо хлорид) и выделения водорода H2.
Эта реакция является типичной реакцией железа с соляной кислотой. Полученный хлорид железа часто используется в распространенных процессах, таких как производство железных материалов, медицина, пищевая промышленность и другие сферы деятельности, благодаря своим уникальным свойствам и сильной способности образовывать соединения с различными веществами.
Таким образом, отношение соляной кислоты к железу является одной из важных тем для изучения в области химии и технологии. Знание реакции и свойств соляной кислоты и железа позволяет проникнуть в тайны их взаимодействия и применить полученные знания в различных сферах жизни и науки.
Воздействие соляной кислоты на железо

Соляная кислота (хлороводородная кислота) – кислотное вещество, которое может сильно воздействовать на железо. При взаимодействии соляной кислоты с железом происходит химическая реакция, в результате которой образуется соль – хлорид железа и выделяется водород.
Соляная кислота, будучи сильным окислителем, может вызывать коррозию металла. При этом на поверхности железа образуется слой оксидов железа, который может затем растворяться в соляной кислоте. Таким образом, воздействие соляной кислоты может вызывать разрушение поверхности железа.
Реакция соляной кислоты с железом сопровождается выделением водорода. Взаимодействие металла с кислотой протекает в две стадии: вначале образуется хлорид железа, а затем под действием кислоты выпускаются пузырьки водорода. Это явление можно наблюдать, если поместить кусочек железа в раствор соляной кислоты.
Воздействие соляной кислоты на железо находит множество применений в различных отраслях промышленности и научных исследованиях. Например, соляная кислота используется для удаления ржавчины с поверхностей из железа или стали. Она также применяется для очистки трубопроводов и наладки химических реакций в лабораториях.
Химические свойства соляной кислоты

Соляная кислота, или хлороводородная кислота (HCl), является одной из наиболее важных и распространенных кислот в химии. Она обладает рядом уникальных химических свойств, которые делают ее эффективным реагентом и широко используемым в различных отраслях промышленности.
Одним из основных свойств соляной кислоты является ее высокая реакционная активность. HCl с легкостью взаимодействует с большинством металлов, образуя соли и выделяя водород. Например, соляная кислота реагирует с железом, образуя хлорид железа и выделяя молекулы водорода: 2HCl + Fe -> FeCl2 + H2.
Кроме того, соляная кислота проявляет свойства окисляющего агента в ряде реакций. Она способна окислить определенные вещества, например, восстановить йодид калия до йода, выделив молекулы хлора: 6HCl + 2KI -> 2KCl + I2 + 4H2O + 3Cl2.
Другой важной свойство соляной кислоты является ее способность к диссоциации в растворе. HCl эффективно диссоциирует на ионы водорода (H+) и ионы хлора (Cl-), что делает ее кислотной. Это свойство позволяет соляной кислоте служить катализатором различных химических реакций, а также использоваться в аналитической химии для определения pH растворов.
И, наконец, соляная кислота находит применение во многих отраслях промышленности. Она используется для очистки и обработки металлов, производства пластмасс, производства удобрений, а также в медицине и лабораторных исследованиях. Ее высокая растворимость и химическая активность делают ее эффективным и универсальным реагентом.
Реакция соляной кислоты с железом

Соляная кислота, химическая соединение с формулой HCl, особенно активно взаимодействует с железом. Эта реакция является одной из наиболее известных и часто используемых химических реакций.
При взаимодействии соляной кислоты с железом, образуется солюбильная соль железа и выделяется молекулярный водород. Это реакция обмена, которая соответствует общему химическому уравнению: Fe + 2HCl → FeCl2 + H2.
Реакция между соляной кислотой и железом происходит при обычных температурах и обычном давлении. Она сопровождается выделением газа (водорода) и образованием соли железа (хлорида железа(II)). Соляная кислота является сильным окислителем, поэтому железо обесцвечивается и превращается в ион железа с двойным положительным зарядом (Fe2+).
Эта реакция сольватируется, поэтому соляная кислота вступает в химическую реакцию с железом, разрушая его структуру. Результатом этой реакции является образование водорода, который выделяется в виде газа.
Коррозия железа под воздействием соляной кислоты
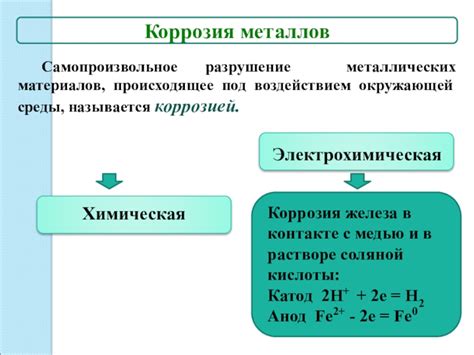
Соляная кислота (HCl) является одной из самых распространенных кислот и часто применяется в различных сферах промышленности и в быту. Эта кислота обладает высокой коррозионной активностью, поэтому ее воздействие на металлы, включая железо, вызывает неконтролируемый процесс разрушения материала.
Под воздействием соляной кислоты железо подвергается химическому окислению и образованию соответствующих солей. Коррозия вызывает выщелачивание металла и образование пузырчатых отложений, которые затем превращаются в ржавчину. Соляная кислота нарушает защитную пленку оксида железа (Fe2O3), которая обычно предохраняет металл от окисления.
Хотя железо и может быть устойчивым к окислению на воздухе при комнатной температуре, взаимодействие с соляной кислотой вызывает акцерецию процессов коррозии. Реакция протекает с выделением водорода, что приводит к образованию пузырьков на поверхности металла и образованию пористых структур.
Поэтому при работе с соляной кислотой важно принимать меры предосторожности и использовать специальные защитные средства. Также широко применяются различные покрытия или защитные слои для предотвращения коррозии, особенно при контакте с соляной кислотой.
Применение соляной кислоты в промышленности

Соляная кислота (HCl) является одним из наиболее важных химических соединений, применяемых в промышленности. Ее используют в различных отраслях, благодаря ее уникальным свойствам и высокой активности. Рассмотрим некоторые из областей ее применения.
1. Производство пластмасс и полимеров. Соляная кислота является одним из ключевых ингредиентов в производстве пластмасс и полимеров. Она используется для очистки и обработки сырья, а также в качестве катализатора при полимеризации различных веществ. Благодаря своей кислотности она способствует получению высококачественных и устойчивых материалов.
2. Металлургическая промышленность. Соляная кислота широко применяется в металлургии. Она используется для очистки металлов от органических и неорганических загрязнений, а также для удаления ржавчины и окислов. Кроме того, она применяется при процессах гальванизации, а также для обработки металлических поверхностей перед нанесением защитного покрытия.
3. Производство хлора и его производных. Соль натрия (NaCl) является основным сырьем для производства хлора (Cl2) и его производных, таких как гидрохлоридная кислота, хлориды металлов и др. Соляная кислота применяется в процессе электролиза солевых растворов для разложения соли натрия на хлор и каустическую соду. Таким образом, соляная кислота играет важную роль в химической промышленности.
4. Очистка воды и обработка сточных вод. Соляная кислота применяется для регулирования рН воды, а также для удаления железа, марганца и других загрязнений. Она эффективно удаляет ржавчину и осадки с трубопроводов и оборудования, а также помогает предотвратить образование накипи.
5. Производство удобрений. Соляная кислота используется в производстве удобрений, таких как аммиачная селитра и аммиачный нитрат. Она служит источником азота для растений, способствуя их росту и развитию.
Таким образом, соляная кислота широко применяется в различных сферах промышленности благодаря своим уникальным свойствам и реактивности. Ее использование позволяет получать высококачественные продукты, обеспечивать чистоту и эффективность производственных процессов, а также способствует улучшению экологической безопасности и эффективности использования ресурсов.
Опасности использования соляной кислоты
Соляная кислота, также известная как хлороводород, представляет собой одну из наиболее опасных химических веществ. Она может причинить серьезный вред здоровью и окружающей среде.
Вещество является сильным ожоговым агентом. При попадании на кожу или слизистые оболочки соляная кислота вызывает ожоги и воспаление. Пострадавший может испытывать острую боль, отек, язвы и рубцы. Для предотвращения контакта с кожей необходимо использовать соответствующую защитную экипировку, такую как резиновые перчатки и защитные очки.
Соляная кислота является агрессивным окислителем. Она может вызывать реакцию с горючими веществами, такими как определенные виды органических материалов, бумага или дерево, что может привести к возгоранию или даже пожару. Поэтому необходимо хранить соляную кислоту в отдельно стоящем хранилище и избегать контакта с воспламеняющимися материалами.
Длительное вдыхание паров соляной кислоты может вызвать серьезные проблемы с дыхательной системой. Она может вызывать ожоги и раздражение слизистой оболочки носа, горла, легких, что может привести к проблемам с дыханием, кашлю, затруднению глотания и даже хроническим заболеваниям легких.
Соляная кислота может вызвать загрязнение окружающей среды. При попадании в водные среды, она может привести к увеличению кислотности и разрушению экосистем. Она также может загрязнять почву и поверхности, ведя к деградации почвенного покрова и влиянию на растительный и животный мир.
Исходя из вышеизложенного, необходимо соблюдать все меры предосторожности при работе с соляной кислотой и следовать правилам безопасности, чтобы минимизировать риски и предотвратить негативные последствия для здоровья и окружающей среды.
Меры безопасности при работе с соляной кислотой

При работе с соляной кислотой необходимо соблюдать определенные меры безопасности, чтобы предотвратить возможные травмы и отравления. Во-первых, следует надевать защитные средства, такие как халат, перчатки, респиратор и защитные очки. Это позволит предотвратить попадание кислоты на кожу, в глаза и дыхательные пути.
Во-вторых, необходимо работать с соляной кислотой в хорошо проветриваемом помещении или под вытяжкой. Кислотные пары могут быть ядовитыми и вызвать раздражение дыхательных путей. Кроме того, следует избегать вдыхания паров кислоты, так как это может привести к ожогам гортани и легких.
Если при работе с соляной кислотой произошло разливание или попадание кислоты на кожу или одежду, необходимо немедленно промыть место попадания большим количеством воды и обратиться за медицинской помощью. Кислота может вызвать глубокие ожоги и повреждение тканей.
Кроме того, при хранении соляной кислоты необходимо соблюдать все требования безопасности. Кислоту не следует хранить рядом с горючими материалами или продуктами питания, а также избегать контакта с другими химическими веществами, которые могут привести к нестабильности и возможному выпуску опасных газов.
В целом, работа с соляной кислотой требует внимательности и ответственности. Соблюдение правил безопасности поможет избежать возможных опасностей и обеспечить безопасность при работе с этой химической веществом.
Вопрос-ответ

Какое отношение соляной кислоты к железу?
Соляная кислота (HCl) взаимодействует с железом (Fe) с образованием водорода (H2) и соли железа (FeCl2 или FeCl3), в зависимости от концентрации кислоты и условий реакции.
Какими свойствами обладает соляная кислота при взаимодействии с железом?
При взаимодействии соляной кислоты с железом образуется водород и соли железа. Кроме того, такая реакция может сопровождаться выделением тепла и образованием пены.
В каких случаях применяют соляную кислоту в отношении к железу?
Соляную кислоту можно использовать для удаления окиси железа с поверхности металла, а также для очистки и обработки железных изделий. Она также применяется в лабораторных условиях для проведения химических реакций и анализа образцов, содержащих железо.
