Соляная кислота (хлороводородная кислота) – одна из наиболее распространенных и известных кислот. Она широко используется в промышленности и в нашей повседневной жизни. Сталкнувшись с металлами, соляная кислота вызывает различные типы реакций в зависимости от их химических свойств и степени активности.
Одним из наиболее распространенных типов реакций с металлами является образование солей. В данной реакции, соляная кислота обменивает ион водорода (H+) на ион металла и образует соль и воду. Образовавшиеся соли проявляют различные химические и физические свойства, и могут использоваться в различных сферах промышленности.
Другим типом реакций, которые могут происходить между соляной кислотой и металлами, является выделение водорода. В этом случае, соляная кислота окисляет металл и образует соль, одновременно выделяя молекулы водорода. Эта реакция особенно активна с металлами, такими как цинк и железо.
Также возможно реагирование соляной кислоты с активными металлами при высоких концентрациях или высоких температурах, что может привести к более сложным реакциям, таким как образование сульфатов металлов или выделение самого хлора. Эти реакции требуют более жестких условий и обладают повышенной опасностью.
Реакции соляной кислоты с металлами

Соляная кислота (хлороводородная кислота) является сильным минеральным кислотным соединением, состоящим из водорода и хлора. Она обладает высокой реакционной активностью и способна взаимодействовать с многими металлами, образуя различные типы реакций.
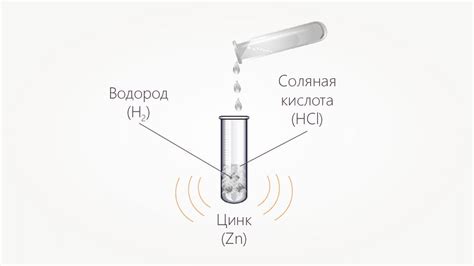
Одним из типов реакций соляной кислоты с металлами является реакция образования солянокислого металла. В ходе этой реакции атом водорода кислоты замещается металлическим катионом, образуя соль и выделяяся молекулярный водород. Примером такой реакции является взаимодействие соляной кислоты с цинком, при котором образуется хлорид цинка и выделяется водород: Zn + 2HCl → ZnCl2 + H2.
Другим типом реакции является реакция нейтрализации, при которой соляная кислота образует соль и воду. В данном случае, водородные ионы H+ в кислоте реагируют с гидроксидными ионами OH- в основании, образуя воду H2O. Примером такой реакции может быть взаимодействие соляной кислоты с натрием, при котором образуется хлорид натрия и вода: HCl + NaOH → NaCl + H2O.
Также, соляная кислота может взаимодействовать с активными металлами, такими как натрий, калий и литий, с образованием водорода и соли. Взаимодействие соляной кислоты с натрием может протекать взрывоопасным образом, и поэтому требует особой осторожности.
Реакция соляной кислоты с щелочными металлами
Соляная кислота – одна из наиболее распространенных и активных кислот, которая образуется при взаимодействии воды с хлоридом водорода. Она характеризуется высокой степенью диссоциации и является сильным окислителем. Из-за этих свойств соляная кислота способна взаимодействовать с различными соединениями, в том числе с металлами, в том числе с щелочными металлами.
При взаимодействии соляной кислоты с щелочными металлами происходит химическая реакция. Щелочные металлы (например, натрий, калий, литий) реагируют с кислотой, образуя соли иводород газ. Реакция протекает с выделением тепла. Щелочные металлы, как сильные восстановители, реагируют с соляной кислотой, окисляясь и передавая свои электроны кислоте. Формирующийся иодид металла, растворяясь в воде, приводит к образованию иона металла и хлороводорода.
В ходе реакции соляной кислоты с щелочными металлами также выделяются газы водорода и хлороводорода. Они образуют пузырьки, благодаря чему реакция хорошо наблюдается. При проведении эксперимента рекомендуется использовать соляную кислоту и металл в равных молярных пропорциях, чтобы обеспечить оптимальное протекание реакции.
Реакция соляной кислоты с переходными металлами

Переходные металлы являются широко распространенными элементами в химических соединениях и металлических сплавах. Реакция соляной кислоты с переходными металлами приводит к образованию солей и выделению водорода.
Типичным представителем переходных металлов является железо. При взаимодействии соляной кислоты с железом происходит реакция, в результате которой образуется феррохлорид FeCl2 или железо(II) хлорид. Реакция протекает по следующему уравнению:
Fe + 2HCl → FeCl2 + H2
Аналогичным образом происходит реакция соляной кислоты с медью, в результате которой образуется хлорид меди(II) или медь(II) хлорид. Уравнение реакции выглядит следующим образом:
Cu + 2HCl → CuCl2 + H2
Соляная кислота также реагирует с кобальтом, образуя хлорид кобальта(II) или кобальт(II) хлорид. Реакция протекает по следующему уравнению:
Co + 2HCl → CoCl2 + H2
Другими примерами реакции соляной кислоты с переходными металлами могут быть взаимодействия с никелем, цинком и марганцем, приводящие к образованию соответствующих хлоридов:
- Ni + 2HCl → NiCl2 + H2
- Zn + 2HCl → ZnCl2 + H2
- Mn + 2HCl → MnCl2 + H2
Таким образом, реакция соляной кислоты с переходными металлами приводит к образованию соответствующих хлоридов и выделению водорода.
Вопрос-ответ

Какие типы реакций возможны при взаимодействии соляной кислоты с металлами?
При взаимодействии соляной кислоты с металлами могут происходить следующие типы реакций: образование солей, выделение водорода и окисление металла.
Какую роль играет соляная кислота в реакции с металлами?
Соляная кислота является окислителем в реакции с металлами. Она отбирает электроны от металла, что приводит к окислению металла.
