Щелочные металлы - это элементы периодической системы, которые реактивны и имеют низкую плотность. К этой группе относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они характеризуются высокой электроотрицательностью и способностью образовывать ионы с однозарядным положительным зарядом.
Взаимодействие щелочных металлов с водородом является интересным исследовательским объектом в химии. Щелочные металлы могут реагировать с водородом и образовывать гидриды. Например, натрий реагирует с водородом и образует натриевый гидрид (NaH). Эта реакция может протекать при нагревании или в присутствии катализаторов.
Гидриды щелочных металлов могут быть использованы в различных промышленных процессах. Они могут быть использованы в качестве водородного носителя или катализаторов. Благодаря способности образовывать ионы с положительным зарядом, гидриды щелочных металлов могут быть также использованы в электрохимических процессах, таких как производство водорода или энергетических батарей.
Что такое щелочные металлы?
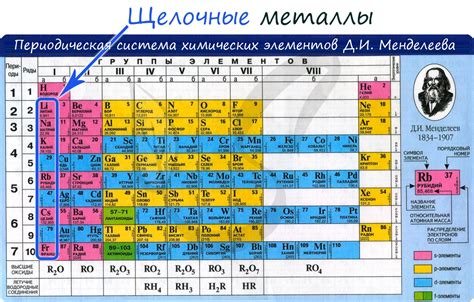
Щелочные металлы - это элементы первой группы периодической таблицы Менделеева, которые характеризуются низкой плотностью, низкой температурой плавления и химической активностью. Их атомы обладают одной валентной электронной оболочкой, что делает их очень реакционноспособными.
В группе щелочных металлов включены следующие элементы: литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они обладают металлическим блеском и хорошей электропроводностью.
Щелочные металлы легко реагируют с водой, образуя щелочи и выделяя водород. Они также могут реагировать с кислородом воздуха, образуя оксиды. Кроме того, они обладают способностью образовывать сплавы с другими металлами и растворяться в аммиаке.
Элементы группы щелочных металлов имеют широкое применение в различных отраслях промышленности и науки. Например, натрий используется в производстве щелочей, стекла, пластика и шампуней. Калий применяется в удобрениях и в производстве бытовых моющих средств. Литий используется в производстве литий-ионных аккумуляторов, а рубидий и цезий применяются в научных исследованиях и атомных часах.
Состав и основные свойства
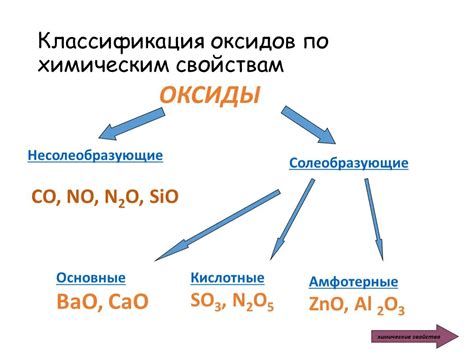
Щелочные металлы — это элементы периодической системы, включающие литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они относятся к первой группе и характеризуются высокой активностью и реакционностью.
Основной химической особенностью щелочных металлов является их способность образовывать сильные щелочные растворы, реагируя с водой. При контакте с водой они образуют гидроксид, сопровождаемый выделением водорода. Реакция щелочных металлов с водой является экзотермической и является одним из составляющих показателей их активности.
Щелочные металлы обладают низкими температурами плавления и кипения, что делает их хорошими теплоносителями. Они также обладают низкой плотностью и легкостью обработки, что делает их ценными материалами в различных отраслях промышленности.
Щелочные металлы оказывают сильное влияние на физиологические процессы в организмах. Витамины и минералы, содержащиеся в щелочных металлах, необходимы для правильного функционирования организма. Они также используются в медицинских препаратах и в качестве катализаторов в химической промышленности.
Применение щелочных металлов в различных отраслях

Щелочные металлы, такие как литий, натрий и калий, широко применяются в различных отраслях благодаря своим уникальным химическим свойствам.
1. Энергетика: Литий используется в производстве аккумуляторов для электромобилей, так как он обладает высокой энергоемкостью и небольшим весом. Калий используется в топливных элементах, которые могут быть использованы для получения электроэнергии из химической энергии.
2. Фармакология: Натрий используется в производстве растворов для инъекций, так как он обладает свойством поддерживать баланс электролитов в организме человека. Литий используется в лекарствах для лечения биполярного аффективного расстройства и депрессии.
3. Металлургия: Натрий и калий используются в процессах получения алюминия из руды. Щелочные металлы используются в сплавах для повышения прочности и коррозионной стойкости металлических материалов.
4. Химическая промышленность: Калий используется в производстве удобрений, так как он содержит много необходимых растениям питательных веществ. Литий используется в производстве литиевых греющих элементов, таких как батарейки и аккумуляторы.
5. Фотоника: Щелочные металлы используются в производстве оптических стекол и волокон для создания оптических волоконных световодов, которые используются в телекоммуникационных системах и лазерных устройствах.
Таким образом, щелочные металлы находят применение во многих отраслях, благодаря своим полезным свойствам и химическим характеристикам.
Взаимодействие щелочных металлов с водородом

Щелочные металлы - это элементы, расположенные в первой группе периодической таблицы: литий (Li), натрий (Na), калий (K), рубидий (Rb) и цезий (Cs). Они легко взаимодействуют с водородом, образуя соединения, называемые гидридами. Гидриды щелочных металлов являются сильными веществами, способными выделять водород при контакте с водой или кислородом.
Взаимодействие щелочных металлов с водородом происходит по принципу образования ионных связей. Щелочные металлы имеют одну электронную оболочку, которая легко отдается, образуя положительный ион. Водород, в свою очередь, имеет одну электрону на своей единственной оболочке, и может легко принять электрон, образуя отрицательный ион.
Таким образом, при взаимодействии щелочных металлов с водородом образуются ионные соединения металла и водорода. Примерами таких соединений являются литийгидрид (LiH), натрийгидрид (NaH) и калийгидрид (KH).
Образование гидридов щелочных металлов является не только академическим интересом, но и имеет практическое применение. Гидриды щелочных металлов используются в качестве химических реагентов, сырья для производства водорода и в различных промышленных процессах.
Взаимодействие щелочных металлов с водородом является важной областью научных исследований, которая позволяет лучше понять структуру и свойства этих элементов. Изучение таких взаимодействий может привести к разработке новых материалов и технологий с использованием водорода в различных сферах, включая энергетику и транспорт.
Вопрос-ответ

Какие щелочные металлы взаимодействуют с водородом?
Все щелочные металлы (литий, натрий, калий, рубидий, цезий) могут взаимодействовать с водородом.
В чем заключается взаимодействие щелочных металлов с водородом?
Взаимодействие щелочных металлов с водородом происходит через образование солей гидридов щелочных металлов и выделения водородного газа.
