Реакция щелочных металлов с водой - это процесс, который может протекать с невероятной энергией и вызывать впечатляющие последствия. Щелочные металлы, такие как натрий, калий и литий, легко реагируют с водой, образуя горючие газы, щелочные растворы и даже взрывы.
Когда щелочный металл погружается в воду, происходит сильное выделение водорода. Реакция проходит настолько быстро, что вода начинает кипеть и испаряться. Этот процесс сопровождается высвобождением большого количества тепла, что вызывает возгорание горячего водяного пара и образует яркий пламя.
Интересно, что щелочные металлы также реагируют с влажным воздухом, образуя щелочные растворы. К примеру, металл калий покрывается липкой, гелеподобной массой, состоящей из щелочи. Это связано с тем, что металлы реагируют не только с водой, но и с влагой из воздуха, образуя щелочные растворы, которые после окисления становятся еще более опасными.
Необычайная реакция щелочных металлов с водой привлекает внимание не только ученых, но и широкой общественности. Разрушительная сила, отважность и даже красота этого процесса заставляют нас восхищаться силой природы и обращать внимание на опасности, связанные с неправильной обработкой этих металлов.
Исторический обзор: первые открытия и открытия в настоящее время

Первые открытия
Изучение реакции щелочных металлов с водой началось задолго до нашей эры. В Древнем Египте и Древней Греции наблюдались первые проявления данной реакции. Однако, первым ученым, который систематически исследовал это явление, был арабский химик и алхимик Джабир ибн Хайян, живший в VIII веке. В своих трудах он описал, что реакция щелочных металлов с водой сопровождается появлением пламени и образованием щелочи.
Открытия в настоящее время
С развитием науки и технологий открытия в области реакции щелочных металлов с водой продолжаются в настоящее время. Современные исследования позволяют подробно изучать механизмы данной реакции и выявлять дополнительные аспекты. Например, в 1807 году был открыт газ, выделяющийся при взаимодействии щелочных металлов с водой - это водород. Это было сделано английским химиком и физиком Вильямом Николсоном.
Позднее, в начале XX века, реакция щелочных металлов с водой стала активно изучаться в рамках разработки водородных двигателей. Явление высокотемпературного взрыва при соприкосновении щелочных металлов с водой привело к опасениям и необходимости разработки безопасных технологий. Современные исследования в этой области ведутся в целях улучшения эффективности процесса и минимизации возможных взрывов.
Свойства щелочных металлов и их взаимодействие с водой
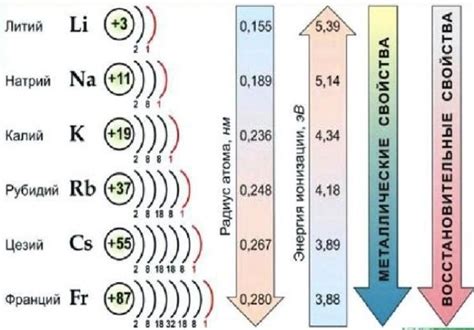
Щелочные металлы – это группа элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb) и цезий (Cs). Эти металлы характеризуются уникальными физическими и химическими свойствами.
Щелочные металлы обладают низкой плотностью и низкой температурой плавления, что делает их мягкими и легко обрабатываемыми. Они являются отличными проводниками электричества и тепла, а также обладают металлическим блеском.
Водородное взаимодействие щелочных металлов с водой чрезвычайно активно. Комбинируясь с молекулами воды, эти металлы выделяют водород и образуют гидроксиды, известные как щелочи. Это происходит вследствие высокой реакционной способности и низкой ионизационной энергии щелочных металлов.
Взаимодействие щелочных металлов с водой сопровождается химической реакцией и выделением значительного количества тепла. В некоторых случаях может возникнуть взрыв из-за образования водорода и его смешивания с кислородом из воздуха. Поэтому реакция щелочных металлов с водой требует особой осторожности и проводится в специальных условиях.
Для наглядности можно представить таблицу с данными о реакции щелочных металлов с водой. В данной таблице будут указаны металлы, химические уравнения реакций и основные свойства образовавшихся гидроксидов.
Физические процессы, происходящие во время реакции
Во время реакции щелочных металлов с водой происходят различные физические процессы, которые сопровождаются выделением тепла, образованием щелочной растворимой соли и выделением газа в виде пузырьков.
Уже с самого начала реакции можно наблюдать интенсивное выделение тепла. Данный физический процесс связан с термической реакцией между водой и щелочным металлом. Обычно такая реакция протекает очень быстро, за несколько секунд, и довольно интенсивно, что создает ощущение жара и появление пара вокруг реагирующих веществ.
Также в результате данной реакции образуется щелочная растворимая соль. При растворении щелочного металла в воде, образуется гидроксид металла, который является щелочью. Этот процесс сопровождается растворением и ионизацией молекул щелочи, что приводит к образованию гидроксид-ионов OH- в растворе.
Также во время реакции происходит выделение газа в виде пузырьков. Этот процесс связан с образованием водорода H2 в результате реакции между щелочным металлом и водой. Образовавшийся водород, не растворяясь в воде, образует пузырьки, которые поднимаются к поверхности и выделяются в атмосферу.
Эффекты реакции: образование гидроксидов и оснований
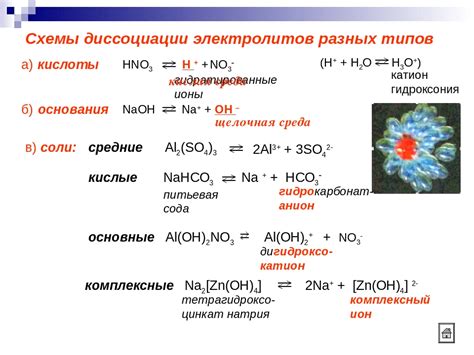
Реакция щелочных металлов с водой приводит к образованию гидроксидов и оснований, что является характерным эффектом данного процесса.
В результате реакции, металлические щелочные элементы, такие как натрий (Na), калий (K) и литий (Li), вступают в химическую реакцию с молекулами воды. Гибридизация этих металлов образует гидроксид щелочного металла, который является основанием.
Гидроксиды являются особой формой оснований, которые обладают щелочными свойствами. Они растворяются в воде, образуя щелочные растворы. Гидроксид натрия обозначается формулой NaOH, гидроксид калия - KOH, гидроксид лития - LiOH. Все они представляют собой сильные основания и способны нейтрализовать кислоты.
Образование гидроксидов и оснований при реакции щелочных металлов с водой объясняет резкое повышение pH раствора. При этом наблюдаются характерные изменения, такие как образование бурых отложений в виде осадка и возникновение пузырьков газа, состоящее из водорода, который выделяется во время реакции.
Особенности реакции лития, натрия, калия и других щелочных металлов
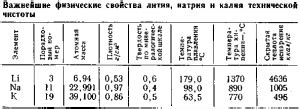
Литий, натрий и калий относятся к щелочным металлам, характеризующимся высокой реакционной способностью и активностью. Они имеют низкую плотность и мягкую текстуру, легко резаться ножом, а также отличаются низкой температурой плавления и кипения.
При контакте с водой щелочные металлы реагируют, образуют щелочные гидроксиды и выделяются водород. Эта реакция сопровождается высвобождением тепла и повышением температуры реакционной смеси.
Реакция с водой лития протекает медленно, но при этом наблюдается выделение пламени. Натрий, калий и другие щелочные металлы реагируют намного быстрее, при этом пламя яркое и интенсивное.
Реакция щелочных металлов с водой осуществляется следующим образом: металл реагирует с молекулой воды, образуя щелочный гидроксид и выделяя водород. Причиной выделения водорода является эндотермическая реакция, основная причина выделения тепла.
- Литий реагирует со водой медленно, выделяет наименьшее количество водорода и образует гидроксид лития.
- Натрий реагирует более интенсивно, выделяется больше водорода и образуется гидроксид натрия. При этом пламя может быть ярким и красным.
- Калий реагирует очень активно, пламя яркое и фиолетовое, выделяется много водорода и образуется гидроксид калия.
Реакция щелочных металлов с водой имеет практическое применение в различных сферах, таких как производство водорода, производство химических реактивов и взрывчатых веществ.
Опасности при обращении с щелочными металлами

Щелочные металлы, такие как литий, натрий и калий, представляют опасность при обращении с ними из-за их высокой реактивности. При контакте с водой или влажным воздухом эти металлы могут вызывать сильные взрывы, возгорания и образование едкой щелочи.
Взрывоопасность щелочных металлов обусловлена их способностью быстро реагировать с водой. При этом выделяется водород, который в присутствии металла может воспламениться. Взрывы могут быть настолько сильными, что могут привести к разрушению зданий и травмированию людей.
Одна из наиболее опасных особенностей щелочных металлов - образование едкой щелочи. При реакции с водой металлы образуют оксиды, которые растворяются в воде и образуют щелочные растворы. Эти растворы могут вызывать ожоги при контакте с кожей, а также приводить к повреждению глаз и дыхательных путей.
Безопасность при обращении с щелочными металлами требует строгого соблюдения предосторожностей. Необходимо использовать защитную экипировку, включающую перчатки, средства защиты глаз и дыхания. Также важно осуществлять работу в хорошо проветриваемом помещении и избегать контакта с водой или другими веществами, которые могут способствовать возникновению реакции.
В случае аварийного сползания щелочного металла необходимо немедленно принять меры по его удалению, используя специальную оборудование и средства защиты. Также следует ограничить доступ в зону возможной опасности и обратиться за помощью к специалистам.
Возможности применения реакции в научных и технических целях

1. Поступательное движение: Реакция щелочных металлов с водой может использоваться для создания поступательного движения. Например, в научных экспериментах можно использовать реакцию натрия с водой для создания движущегося робота или механизма. Щелочные металлы могут служить топливом для таких устройств.
2. Генерация энергии: Реакция щелочных металлов с водой может быть использована для генерации энергии. Например, водород, выделяющийся в результате этой реакции, можно использовать как источник энергии для работы двигателей. Это может быть особенно полезно в ситуациях, где нет доступа к другим источникам энергии.
3. Химические реакции: Реакция щелочных металлов с водой может быть использована для проведения различных химических реакций. При этом могут образовываться различные соединения, которые могут быть использованы в научных исследованиях или в технических процессах. Например, получение гидроксида натрия или гидроксида калия может быть полезно для производства мыла или других химических продуктов.
4. Очистка воды: Реакцию щелочных металлов с водой можно использовать для очистки воды от различных примесей. Щелочные металлы могут образовывать соли с различными загрязнителями, которые затем можно отфильтровать или удалить другими методами. Это может быть полезно для очистки питьевой воды или удаления загрязнений из сточных вод.
Вопрос-ответ

Что происходит, когда щелочной металл реагирует с водой?
При реакции щелочных металлов с водой происходит выделение водорода, образование щелочи и выделение тепла. Эта реакция может быть сопровождена жаром и даже взрывами.
Почему щелочные металлы реагируют с водой?
Щелочные металлы реагируют с водой из-за высокой реакционной способности своих атомов кискалия, аталлия и других.
Каковы последствия реакции щелочных металлов с водой?
Последствия реакции щелочных металлов с водой могут быть разными. В некоторых случаях реакция может протекать с жаром и образованием щелочи. В более сильных случаях может произойти взрыв.
Каким образом происходят взрывы при реакции щелочных металлов с водой?
Взрывы при реакции щелочных металлов с водой происходят из-за высокого уровня энергии, выделяющейся при реакции. Энергия может накапливаться в водороде, который образуется в результате реакции, что приводит к взрыву.
