Щелочные металлы - группа химических элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они отличаются высокой химической активностью и способностью взаимодействовать с водой. При взаимодействии с водой щелочные металлы образуют гидроксиды, которые являются сильными щелочами и имеют широкое применение в различных отраслях промышленности и научных исследованиях.
Взаимодействие щелочных металлов с водой происходит следующим образом. Когда металлический элемент погружается в воду, происходит распад молекулы воды на ионы водорода (H+) и гидроксид-ионов (OH-). Поскольку щелочные металлы обладают высокой химической активностью, взаимодействие с водой происходит интенсивно и с выделением большого количества тепла.
Такое реактивное взаимодействие обусловлено электрохимическими свойствами щелочных металлов. Они имеют низкую электроотрицательность и, соответственно, высокую электроотрицательность, что усиливает их способность притягивать ионы воды и активно взаимодействовать с ними.
В результате взаимодействия щелочных металлов с водой образуются гидроксиды. Например, литий взаимодействует с водой, образуя гидроксид лития (LiOH). Натрий взаимодействует с водой, образуя гидроксид натрия (NaOH). Калий, рубидий, цезий и франций также образуют соответствующие гидроксиды при взаимодействии с водой.
Взаимодействие щелочных металлов с водой

Взаимодействие щелочных металлов с водой – процесс, давно известный ученым. Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, обладают способностью реагировать с водой, образуя гидроксиды.
Это явление происходит при обычных условиях, без необходимости применения высоких температур или давления. В результате взаимодействия щелочных металлов с водой образуются гидроксиды, которые являются щелочными растворами.
Щелочные металлы взаимодействуют с водой, так как они обладают высокой активностью и электроотрицательностью. Во время реакции происходит выделение водорода и образование гидроксидов металлов.
При этом реакция взаимодействия может быть сопровождена выделением большого количества теплоты и образованием пламени. Это связано с высокой реактивностью щелочных металлов и их способностью быстро реагировать с водой.
Реакция взаимодействия щелочных металлов с водой является универсальной и может применяться для идентификации данных металлов. В ходе эксперимента можно наблюдать, как металл трещит и плавится в результате реакции с водой, а также как образуется щелочной раствор.
Стоит отметить, что реактивность щелочных металлов с водой возрастает по мере движения в периодической системе элементов от лития к цезию. Натрий и калий реагируют с водой менее активно, чем литий, а рубидий и цезий – более активно.
Образование гидроксидов при обычных условиях

Гидроксиды – это соединения, образующиеся при взаимодействии щелочных металлов с водой при обычных условиях. Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, обладают сильной щелочной реакцией и легко реагируют с водой.
Схема реакции растворения щелочного металла в воде следующая:
- Металл вступает в контакт с водой;
- Происходит реакция, в ходе которой образуется гидроксид металла и выделяется водородный газ;
- Гидроксид металла растворяется в воде, образуя щелочной раствор.
Например, реакция лития с водой протекает следующим образом:
- 2Li + 2H2O → 2LiOH + H2↑
Также важно отметить, что при реакции с водой образуется гидроксид металла в осадке. Например, если кусочек натрия положить в стакан с водой, на поверхности образуется белый осадок натриевого гидроксида.
Образование гидроксидов при обычных условиях имеет практическое значение. Гидроксиды щелочных металлов используются в различных отраслях промышленности, в том числе в производстве щелочей и мыла, водоочистке и производстве химических реактивов.
Химические реакции в присутствии щелочных металлов и воды
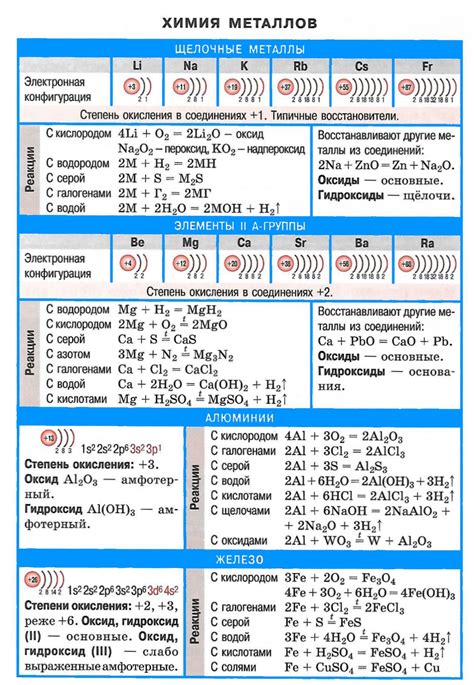
Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, обладают способностью взаимодействовать с водой при обычных условиях. При этом происходят химические реакции, в результате которых образуются гидроксиды этих металлов и выделяется водород.
Процесс взаимодействия щелочных металлов с водой может быть представлен следующим уравнением реакции:
2M + 2H2O -> 2M(OH) + H2
Где M - символ щелочного металла.
Вода обеспечивает необходимую среду для взаимодействия металлов и их окислительных свойств. В процессе реакции ионы щелочного металла обмениваются электронами с водой, что приводит к образованию гидроксидов. Выделение водорода является побочным продуктом реакции.
Щелочные металлы обладают большой активностью и образуют самые легко растворимые гидроксиды. Гидроксиды этих металлов обладают щелочными свойствами и широко используются в различных областях, включая промышленность, медицину и быт.
Химические реакции щелочных металлов с водой проходят со значительным выделением тепла и сопровождаются образованием пузырьков водорода. Данное свойство можно использовать для определения наличия щелочного металла в образце или для получения водорода в лабораторных условиях.
Влияние взаимодействия щелочных металлов с водой на окружающую среду

Гидроксиды щелочных металлов, образующиеся в результате взаимодействия металлов этой группы с водой, представляют собой сильные щелочные соединения. Они могут оказывать значительное влияние на окружающую среду.
Во-первых, гидроксиды щелочных металлов обладают свойством растворяться в воде, образуя сильно щелочные растворы. При попадании этих растворов в почву они могут негативно повлиять на ее качество, увеличивая ее щелочность и нарушая химический баланс.
Во-вторых, гидроксиды щелочных металлов могут вызывать коррозию металлических конструкций. Вода, насыщенная этими соединениями, может разрушать покрытия и приводить к выравниванию исходных металлов. Это может привести к серьезным повреждениям инфраструктуры и созданию опасных ситуаций.
В-третьих, гидроксиды щелочных металлов могут вызывать токсическое воздействие на растительный и животный мир. Высокая щелочность этих соединений может оказывать вредное воздействие на растения, приводя к нарушению физиологических процессов и ослаблению роста. Водные организмы также могут страдать от влияния гидроксидов, что приводит к изменению экосистем и ухудшению биологического разнообразия.
В-четвертых, гидроксиды щелочных металлов могут нанести вред здоровью человека. При попадании воды, насыщенной этими соединениями, на кожу или слизистые оболочки они могут вызывать ожоги и раздражение. Поэтому необходимо соблюдать меры предосторожности и обратить особое внимание на безопасное использование и хранение гидроксидов щелочных металлов.
Вопрос-ответ

Какие металлы взаимодействуют с водой при обычных условиях?
Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, взаимодействуют с водой при обычных условиях, образуя гидроксиды и выделяя водород.
Что происходит при взаимодействии щелочных металлов с водой?
При взаимодействии щелочных металлов с водой происходит химическая реакция, в результате которой образуются гидроксиды металлов и выделяется водородный газ. Интенсивность реакции зависит от активности металла и температуры воды.
