Серная кислота (H2SO4) – одна из самых распространенных и важных неорганических кислот. У нее широкий спектр применения в различных отраслях промышленности и научных исследованиях. Одной из важных особенностей серной кислоты является ее способность взаимодействовать с различными соединениями, такими как оксиды металлов, основания и соли. Такие реакции позволяют получать новые соединения, изменять их физико-химические свойства и применять их в различных промышленных процессах.
Взаимодействие серной кислоты с оксидами металлов происходит в результате образования соответствующих солей. Для этого необходимо добавить оксид металла к серной кислоте и провести реакцию, которая приводит к образованию водорастворимого соединения между серной кислотой и металлом. Таким образом, возможно получение новых соединений с определенными химическими и физическими свойствами.
Основания - это вещества, которые могут принимать протоны от кислоты. Взаимодействие серной кислоты с основаниями приводит к образованию солей и воды. Как и в случае с оксидами металлов, реакция происходит путем добавления основания к серной кислоте и образования ионов соли. Эта реакция широко применяется в различных химических процессах и может изменяться в зависимости от используемых веществ и условий проведения реакции.
Соли - это соединения, образованные в результате взаимодействия кислот и оснований. Взаимодействие серной кислоты с солями может привести к образованию новых соединений с различными свойствами. В зависимости от реакционных условий и используемых веществ, эта реакция может протекать по-разному и приводить к образованию соединений с различными степенями окисления серы.
Реакция серной кислоты с оксидами металлов
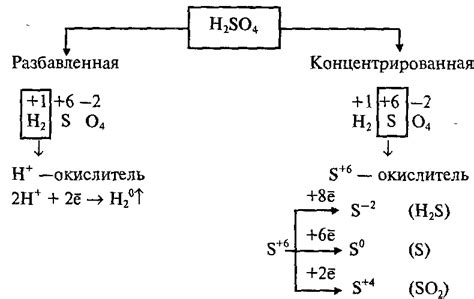
Серная кислота – это одна из наиболее распространенных неорганических кислот. Она обладает сильными окислительными свойствами и образует соединения с различными веществами, в том числе с оксидами металлов. Реакция серной кислоты с оксидами металлов является типичным примером подстановочной реакции.
При взаимодействии серной кислоты с оксидами металлов образуются соли серной кислоты и вода. Эта реакция происходит обычно с выделением тепла. Оксид металла действует в данной реакции как основание, а серная кислота – как кислота. В реакции нейтрализации образуется соль, которая может быть растворимой или нерастворимой в воде.
Некоторые оксиды металлов, такие как оксиды металлов переходных групп, способны образовывать растворимые соли с серной кислотой. В этом случае реакция протекает полностью и возможна образование цветных растворов. Например, при реакции серной кислоты с оксидом железа (III) образуется соль серной кислоты – серный ангидрид.
Однако, некоторые оксиды, такие как оксиды щелочных металлов (например, оксид натрия) или оксид алюминия, не реагируют с серной кислотой. Это связано с тем, что соли, образующиеся при взаимодействии, нерастворимы в воде и не могут образовать растворы.
Влияние оснований на серную кислоту

Серная кислота - это неорганическое соединение, которое взаимодействует с различными основаниями. Изучение этого взаимодействия позволяет понять, как основания могут влиять на свойства серной кислоты.
Основания реагируют с серной кислотой, образуя соли и воду. При этом происходит протекание химической реакции, участвующие в которой ионы H+ из серной кислоты и OH- из основания образуют воду.
Характер реакции между основаниями и серной кислотой зависит от свойств обоих соединений. Сильные основания, такие как гидроксид натрия (NaOH) или гидроксид калия (KOH), полностью реагируют с серной кислотой, образуя соли с положительными ионами металлов.
У слабых оснований, например, гидроксида алюминия (Al(OH)3) или гидроксида магния (Mg(OH)2), реакция с серной кислотой происходит лишь частично. Образуются соединения, которые называют алюминатами или магниятами, и они остаются растворимыми в воде.
Влияние оснований на серную кислоту проявляется не только в химических реакциях, но и в изменении свойств серной кислоты. Например, добавление основания может снизить кислотность серной кислоты и повысить ее растворимость в воде.
Таким образом, взаимодействие серной кислоты с основаниями играет важную роль в химии и может быть использовано для повышения эффективности многих процессов, например, в производстве удобрений или очистке промышленных сточных вод.
Химические свойства солей серной кислоты
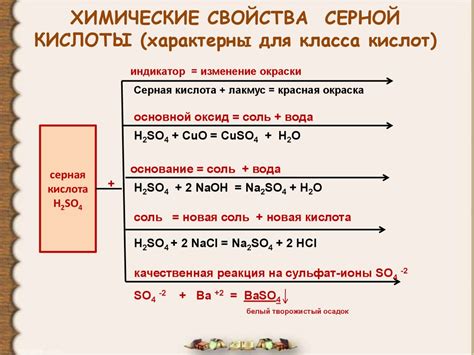
Соли серной кислоты являются соединениями, образующимися при реакции серной кислоты с основаниями или металлами. Они обладают рядом химических свойств, которые определяют их использование в различных сферах промышленности и науки.
Прежде всего, соли серной кислоты обладают гидратацией - способностью связываться с молекулами воды. Некоторые соли способны образовывать гидраты с определенным количеством молекул воды, что влияет на их физические свойства, например на температуру плавления или растворимость.
Соли серной кислоты также проявляют свои кислотные свойства при реакции с основаниями. При этом происходит нейтрализационная реакция, в результате которой образуется соль и вода. Важно отметить, что при реакции сильного основания с серной кислотой образуется соль, которая может быть растворима или нерастворима в воде.
Другим важным химическим свойством солей серной кислоты является их способность образовывать комплексные соединения. Комплексные соединения с образованием координационных связей возникают при взаимодействии солей серной кислоты с соответствующими лигандами, такими как аммиак или водородсульфид.
Соли серной кислоты находят широкое применение в промышленности, фармакологии, сельском хозяйстве и других отраслях. Они используются в производстве удобрений, стекла, подкрасочных и строительных материалов, а также в медицине, для создания препаратов и реагентов.
Применение серной кислоты и ее соединений
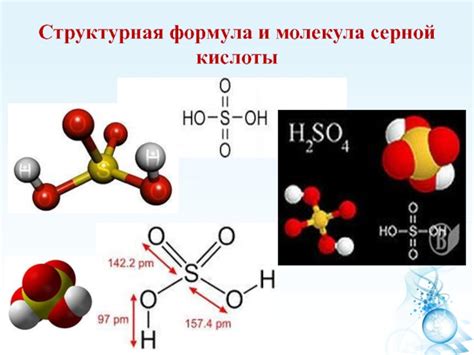
Серная кислота (H2SO4) — широко используемое химическое соединение с множеством применений.
Производство удобрений: серная кислота используется для получения фосфорных удобрений из фосфатных руд. Она является ключевым компонентом в процессе получения аммофоса и суперфосфата. Также серная кислота применяется для производства других удобрений, включая аммиачную селитру и селитру натрия.
Производство органических соединений: серная кислота играет важную роль в химической промышленности и используется для получения различных органических соединений. Например, она является важным компонентом в процессе получения спирта этилового, винилового хлорида и многих других органических соединений.
Гальваническая отрасль: серная кислота используется в процессе металлообработки. Она применяется для очистки металлов от загрязнений, удаления оксидных пленок и образования слоев защитных покрытий на металлических поверхностях.
Производство бумаги: серная кислота используется в процессе производства целлюлозы для бумаги. Она применяется для обработки древесной массы, что позволяет удалить неклетчатые вещества и получить чистую целлюлозу.
Производство жидкого топлива: серная кислота используется в процессе конверсии биомассы или углеводородных сырьевых материалов в жидкое топливо. Она служит катализатором реакции конверсии и позволяет получать различные виды топлива.
Применение других соединений серной кислоты: помимо самой серной кислоты, ее соединения, такие как сульфаты металлов и серные кислотные соли, также находят различные применения. Например, сульфат магния используется в производстве удобрений, сульфат алюминия применяется в процессе коагуляции воды, а серные кислотные соли являются важными промышленными химическими соединениями.
Вопрос-ответ

Что такое серная кислота и как она взаимодействует с оксидами металлов?
Серная кислота (H₂SO₄) - это одна из наиболее распространенных кислот в химии. Она хорошо растворяется в воде и образует соединения с различными веществами. Оксиды металлов - это химические соединения, состоящие из кислорода и металла. При взаимодействии серной кислоты с оксидами металлов образуется соль и вода. Например, при реакции серной кислоты с оксидом железа (Fe₂O₃) образуется соль - сульфат железа (Fe₂(SO₄)₃) и вода (H₂O).
Как серная кислота взаимодействует с основаниями?
Серная кислота - это кислота, а основания - это вещества, способные протекать слабую кислотно-щелочную реакцию. При взаимодействии серной кислоты с основаниями происходит нейтрализационная реакция, в результате которой образуется соль и вода. Например, при взаимодействии серной кислоты (H₂SO₄) с гидроксидом натрия (NaOH) образуется соль - сульфат натрия (Na₂SO₄) и вода (H₂O).
Какова реакция между серной кислотой и солями?
Серная кислота может взаимодействовать с солями и образовывать другие соли. Реакция зависит от конкретной соли и может быть разной. Например, при взаимодействии серной кислоты (H₂SO₄) со солями железа (FeCl₃) образуется соль - сульфат железа (Fe₂(SO₄)₃) и соль - хлорид водорода (HCl). Реакция между серной кислотой и солями может происходить под воздействием тепла или при нагревании и обычно сопровождается выделением газов или образованием осадка.
Какие продукты образуются при взаимодействии серной кислоты с алюминием?
При взаимодействии серной кислоты (H₂SO₄) с алюминием (Al) образуется соль - сульфат алюминия (Al₂(SO₄)₃) и высвобождается водородный газ. Реакция описывается следующим уравнением: 2Al + 3H₂SO₄ → Al₂(SO₄)₃ + 3H₂.
