Серная кислота (H2SO4) является одной из самых распространенных и важных химических соединений. Она широко используется в промышленности, научных исследованиях и в повседневной жизни. Кроме того, серная кислота активно взаимодействует с металлами, порождая различные процессы и реакции.
Взаимодействие серной кислоты с металлами осуществляется по механизму, называемому окислением-восстановлением. В данной реакции серная кислота действует в качестве окислителя, передавая электроны металлу и саморегенерируясь. Это позволяет металлу окислиться и образовать ион металла с положительным зарядом.
Серная кислота обладает высокой кислотностью и агрессивностью. Ее молекула содержит две группы -OH, способные взаимодействовать с металлами. Это свойство определяет способность серной кислоты к различным химическим реакциям с металлическими поверхностями.
При взаимодействии металла с серной кислотой происходит образование солей и выделение водорода. Водородные ионы H+ образуются вследствие диссоциации серной кислоты. В результате образованию соли металла с серной кислотой, например, сульфата металла. Образование солей металлов происходит с выделением объемов водорода, что часто сопровождается пузырьковой эффектом.
Важно отметить, что некоторые металлы, например, никель и алюминий, обладают пассивностью перед серной кислотой. Данное явление связано с образованием на поверхности металла защитной пленки оксида или металлического сульфата, которая предотвращает дальнейшее взаимодействие серной кислоты с металлом. Такая пассивность защищает металл от коррозии и разрушения.
Все вышеописанные особенности взаимодействия серной кислоты с металлами свидетельствуют о сложности процессов, которые происходят при контакте между ними. Изучение данных реакций нашло широкое применение в различных областях, от производства и технологии до научных исследований в химии и физике. Это позволяет лучше понять и контролировать взаимодействия серной кислоты и металлов, а также использовать их в различных технических и химических процессах.
Механизм взаимодействия серной кислоты с металлами
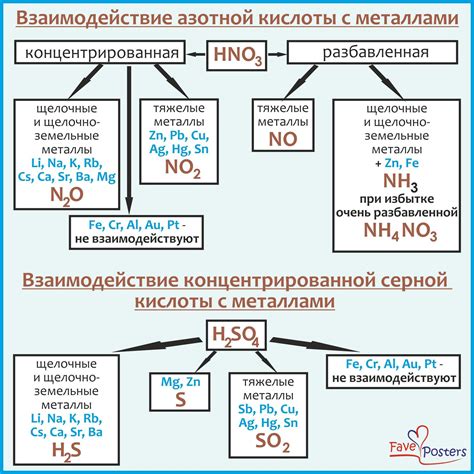
Взаимодействие серной кислоты с металлами осуществляется через процесс окисления и образования соответствующих солей. Этот процесс происходит в несколько этапов.
На первом этапе происходит диссоциация серной кислоты в водном растворе, образуя положительные и отрицательные ионы. Вода служит хорошим растворителем для серной кислоты, что усиливает ее реакционную способность.
На следующем этапе металл вступает в реакцию с отрицательными ионами серной кислоты. Металл окисляется, отдавая электроны, в результате образуется положительный ион металла. Этот процесс называется окислительным взаимодействием.
Образование соответствующих солей происходит благодаря образованию химической связи между положительными и отрицательными ионами. Благодаря этому механизму взаимодействия серной кислоты с металлами возникают серные соли.
Взаимодействие серной кислоты с металлами обладает не только окислительными свойствами, но и является причиной образования водорода. Отдавая электроны, металл способствует редокс-реакции, в результате чего образуется газ водород.
Механизм взаимодействия серной кислоты с металлами является основой для ряда практических применений, например, в процессах гальванического покрытия, где происходит образование покрытия металлом, а также в химическом анализе для определения содержания металлов в различных материалах.
Причины
Серная кислота (H2SO4) является сильной кислотой, и ее взаимодействие с металлами обусловлено рядом причин. Основной причиной этого взаимодействия является способность серной кислоты к диссоциации на ионы в водном растворе.
В результате диссоциации, серная кислота образует положительные ионы водорода (H+) и отрицательные ионы сульфата (SO42-). Ионы водорода обладают сильно кислотными свойствами и могут реагировать с металлами, образуя соли.
Второй причиной взаимодействия серной кислоты с металлами является окислительное действие кислоты. В процессе реакции серной кислоты с металлом, электротонный перенос происходит с металла на ионы водорода, что приводит к окислению металла и понижению его степени окисления.
Третьей причиной взаимодействия серной кислоты с металлами является более высокая энергетическая стойкость ионной связи в сульфатах по сравнению с металлической связью. В результате этого, ионы металла вступают в реакцию с ионами сульфата, образуя стабильные соли металлосульфатов.
Таким образом, взаимодействие серной кислоты с металлами основано на диссоциации кислоты, окислительном действии и преимуществе ионной связи в сульфатах перед металлической связью.
Влияние серной кислоты на металлы

Серная кислота - активное химическое соединение, которое способно взаимодействовать с различными металлами. Ее воздействие может привести к различным реакциям, включая окисление, растворение или образование защитной пленки.
Одной из основных реакций, которые происходят при взаимодействии серной кислоты с металлами, является окисление. При этом металл постепенно окисляется и образует оксиды, которые часто являются неактивными и защищают поверхность металла от дальнейшего воздействия кислоты.
Некоторые металлы, такие как железо и цинк, образуют растворимые соли с серной кислотой. Это значит, что они растворяются в кислоте и образуют ионы, которые могут вступать в дальнейшие химические реакции. Такой процесс может привести к образованию пузырьков газа или выделению тепла.
Однако не все металлы реагируют с серной кислотой. Некоторые металлы, такие как золото и платина, являются химически инертными и не реагируют с кислотой. Они обладают высокой стойкостью к окислению и растворению.
Взаимодействие серной кислоты с металлами имеет важное применение в различных областях. Например, оно используется в гальванических элементах и аккумуляторах, где металлы окисляются и восстанавливаются при прохождении электрического тока.
Таким образом, взаимодействие серной кислоты с металлами является сложным процессом, обусловленным свойствами как кислоты, так и металлов. Оно может приводить как к химическим реакциям, так и к образованию защитных пленок, и способно найти применение в различных технических и химических процессах.
Химические реакции

Химическая реакция – это процесс, в результате которого происходит превращение исходных веществ, называемых реагентами, в новые вещества, которые называются продуктами реакции. Взаимодействие серной кислоты с металлами является одной из таких химических реакций.
Чаще всего при взаимодействии серной кислоты с металлами происходит образование солей. В данной реакции серная кислота выступает в роли окислителя, а металл – в роли восстановителя. При этом серная кислота окисляет металл, передавая ему свои электроны, а сама восстанавливается. Такая реакция часто сопровождается выделением газов, в том числе водорода.
При взаимодействии серной кислоты с металлами образующиеся соли называются сернокислыми солями. Например, при реакции меди с серной кислотой образуется сульфат меди (II). Это вещество имеет формулу CuSO4. Чтобы произвести данную реакцию, нужно добавить медную фольгу (или порошок) в серную кислоту, что вызовет пузырьковое выделение серно-водородного газа и образование сульфата меди (II).
Такие реакции между серной кислотой и металлами обладают большой практической значимостью и широко используются в промышленности для получения различных солей и других химических соединений.
Особенности взаимодействия различных металлов с серной кислотой
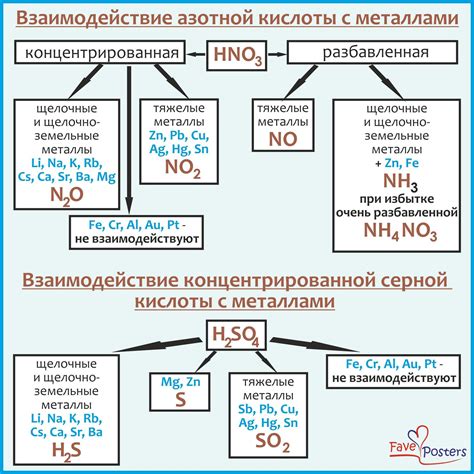
1. Чувствительность активных металлов к серной кислоте: Активные металлы, такие как натрий и калий, реагируют с серной кислотой интенсивно и быстро. При этом наблюдается выделение газа и образование солей серной кислоты.
2. Нейтральные и пассивные металлы: Нейтральные металлы, такие как железо и алюминий, образуют защитную пленку оксида на поверхности, которая препятствует дальнейшему взаимодействию с серной кислотой. Однако, в присутствии катализаторов, таких как пероксид водорода или Фентонова реагенты, взаимодействие может продолжаться.
3. Реакция с платиновыми металлами: Платиновые металлы, такие как платина, палладий и родий, обладают высокой химической инертностью и поэтому не реагируют с серной кислотой при обычных условиях. Однако, при высоких температурах и в присутствии сильных окислителей, таких как концентрированный пероксид водорода, они могут подвергаться химическому разложению.
4. Легированные металлы: Легирование металлов, например, добавление хрома к стали, может повышать их устойчивость к серной кислоте. Хром образует защитную оксидную пленку на поверхности металла, которая предотвращает его дальнейшее коррозионное взаимодействие с серной кислотой.
5. Взаимодействие с щелочными растворами: Некоторые металлы, такие как алюминий и цинк, могут реагировать с серной кислотой только в присутствии щелочных растворов. При этом образуются соли серной кислоты и соли щелочного металла.
Вопрос-ответ

Каким образом серная кислота реагирует с металлами?
Серная кислота может реагировать с металлами, образуя соответствующие соли и выделяя водород. Реакция происходит при контакте металла с серной кислотой, в результате чего металл происходит окисление, а серная кислота восстанавливается.
Почему серная кислота реагирует с металлами?
Серная кислота реагирует с металлами из-за своих окислительных свойств. Она имеет большую аффинность к электронам, что позволяет ей окислять металлы. Кроме того, реакция серной кислоты с металлами является экзотермической, то есть сопровождается выделением энергии в виде тепла.
Каков механизм взаимодействия серной кислоты с металлами?
Механизм взаимодействия серной кислоты с металлами включает несколько стадий. Сначала происходит диссоциация серной кислоты на ионы водорода и сульфатные ионы. Затем металл реагирует с ионами водорода, образуя водород газ и ион металла. Это последующая реакция металла с сульфатными ионами, образуя соответствующую соль и выделяя дополнительный водород.
