Серная кислота является одним из наиболее распространенных и важных химических соединений, которое обладает широким спектром применения в различных отраслях промышленности. Однако, ее взаимодействие с металлами после водорода сопровождается рядом особенностей, которые нуждаются в подробном исследовании.
При взаимодействии серной кислоты с металлами после водорода происходят реакции окисления-восстановления, при которых серная кислота окисляет металлы, а последние восстанавливают серную кислоту до серы или сульфидов. Эти реакции могут протекать с различной интенсивностью, зависящей от вида металла, его концентрации и температуры.
Одной из особенностей взаимодействия серной кислоты с металлами является образование сульфата металла. Это ионное соединение, обладающее высокой стабильностью, что обуславливает его широкое использование в промышленности, особенно в качестве сырья для производства удобрений.
Однако, при взаимодействии некоторых металлов с серной кислотой после водорода могут возникать и нежелательные последствия. В частности, это может быть образование сульфидов металлов, которые обладают низкой растворимостью и могут осаждаться на поверхности или внутри металлических конструкций, приводя к их коррозии и разрушению.
Таким образом, взаимодействие серной кислоты с металлами после водорода имеет свои особенности, которые нуждаются в дальнейшем исследовании и учете при проектировании и эксплуатации различных объектов. Наличие такого знания позволяет предотвратить нежелательные последствия и эффективно использовать серную кислоту в различных отраслях промышленности.
Серная кислота: взаимодействие с металлами
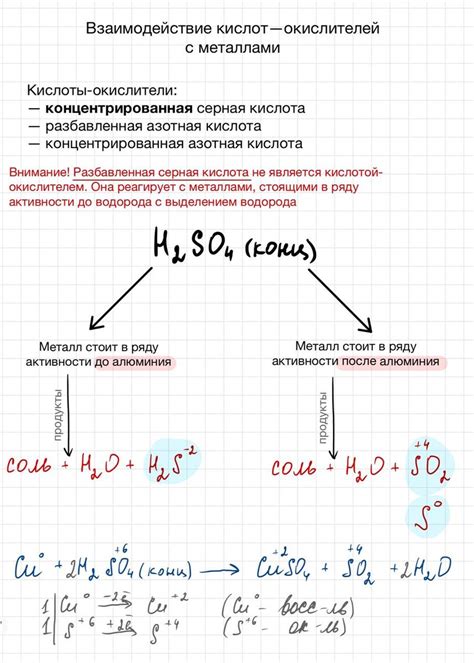
Серная кислота (H2SO4) – одно из наиболее распространенных химических соединений, которое имеет широкий спектр применения в различных отраслях. При контакте серной кислоты с металлами происходят химические реакции, которые могут иметь как полезные, так и негативные последствия.
Взаимодействие серной кислоты с металлами основано на ее способности выступать в роли окислителя. Серная кислота может окислять металлы, выделяя при этом водород. Некоторые металлы, такие как цинк или алюминий, способны реагировать с серной кислотой достаточно интенсивно, с выделением значительного количества водорода.
Например, при взаимодействии алюминия с серной кислотой, образуется сернокислый алюминий и выделяется водород:
- Al + H2SO4 → Al2(SO4)3 + H2
Однако взаимодействие серной кислоты с некоторыми металлами может привести к негативным последствиям, таким как коррозия металлических поверхностей. Например, при контакте железа с серной кислотой, образуется сернокислое железо и выделяется водород:
- Fe + H2SO4 → FeSO4 + H2
Сернокислое железо (FeSO4) может дальше реагировать с кислородом из воздуха и превращаться в гидроксид железа, причиняя поверхности железа значительный вред.
Таким образом, взаимодействие серной кислоты с металлами может иметь как полезные, так и негативные последствия в зависимости от конкретного случая и условий проведения реакции.
Влияние водорода на реакцию
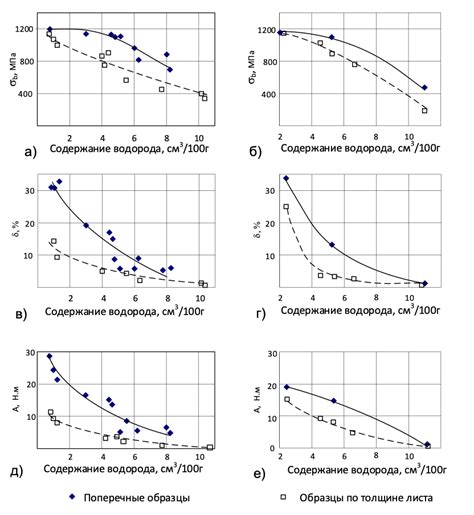
Взаимодействие серной кислоты с металлами может значительно измениться после взаимодействия с водородом. Водород обладает особым эффектом на реакции, вызывающими диспропорцию серной кислоты.
Один из причин такого изменения заключается в формировании газового барьера между металлом и кислотой. Водород, выделяющийся в результате реакции, стремится заполнить пространство между поверхностью металла и окружающей средой. Это приводит к уменьшению контакта между серной кислотой и металлом, что может замедлить или полностью остановить реакцию.
Кроме того, водород может действовать как ингибитор реакции, то есть вещество, которое замедляет или предотвращает химическую реакцию. Водород может образовывать пассивные слои на поверхности металла, что снижает его активность и увеличивает стабильность.
- Формирование газового барьера между металлом и кислотой.
- Действие водорода как ингибитора реакции.
В целом, водород может играть важную роль в изменении характера реакции между серной кислотой и металлами. Понимание влияния водорода на реакцию может помочь улучшить процессы, связанные с обработкой металлов и разработкой новых материалов.
Причины и механизм взаимодействия
Взаимодействие серной кислоты с металлами после водорода обусловлено рядом факторов. Одной из причин этого является высокая активность серной кислоты, которая может реагировать с различными веществами, включая металлы. Относительно легкое взаимодействие кислоты с металлами после водорода объясняется изменением условий, в том числе pH и концентрации серной кислоты в реакционной среде.
Механизм взаимодействия между серной кислотой и металлами, происходящий после выделения водорода, может быть различным и зависит от специфики конкретных реагентов. Одним из возможных механизмов является реакция между металлом и серной кислотой, в которой происходит образование соли металла и освобождение водорода.
Серная кислота, будучи сильным окислителем, способна окислить металлы, что также может быть причиной их взаимодействия. В этом случае происходит передача электронов от металла к серной кислоте, что приводит к образованию соответствующих оксидов металлов и серы.
Иногда взаимодействие между серной кислотой и металлами после выделения водорода сопровождается образованием сульфатных соединений. Это обусловлено тем, что серная кислота обладает способностью образовывать соли, называемые сульфатами. Такие соединения могут обладать высокой стойкостью и использоваться в различных отраслях промышленности.
Физические и химические последствия
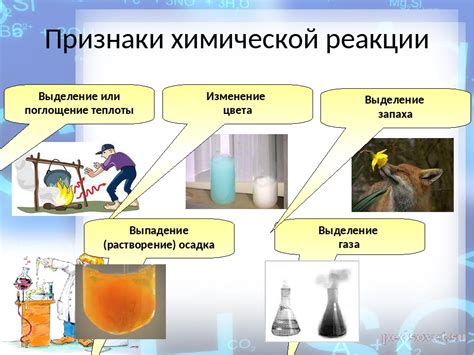
Физические последствия:
- При взаимодействии серной кислоты с металлами после водорода может наблюдаться выделение тепла. Это явление носит название экзотермической реакции.
- Под действием кислоты может происходить изменение цвета металлической поверхности. Например, при реакции серной кислоты с железом образуется окись железа, имеющая красно-коричневый цвет.
- Взаимодействие серной кислоты с металлами может приводить к выделению газов. Например, при реакции с цинком образуется сульфид цинка, при этом выделяется сероводородный газ.
Химические последствия:
- В результате реакции серной кислоты с металлами образуются соли серной кислоты. Например, при взаимодействии с железом формируется сульфат железа (II) FeSO4.
- В процессе реакции металл может окисляться, а серная кислота – восстанавливаться. Это значит, что происходит передача электронов между металлом и кислотой.
- Взаимодействие серной кислоты с металлами может приводить к коррозии металлов, так как кислота способна разрушать металлическую поверхность, образуя оксиды и соли.
Роль серной кислоты в промышленности

Серная кислота - одно из основных веществ, широко применяемых в промышленности. Ее уникальные свойства и возможности обладают огромным значением для множества отраслей.
Применение серной кислоты начинается еще на стадии получения различных видов удобрений. Благодаря своим кислотным свойствам она помогает конвертировать фосфатные сырья в растворимые вещества, которые могут быть эффективно использованы в сельском хозяйстве. Также серная кислота широко используется в производстве минеральных удобрений, таких как аммиачная селитра и суперфосфаты.
Кроме того, серная кислота играет важную роль в производстве бумаги и целлюлозы. Она используется для обработки древесных волокон, позволяя получить белую, чистую массу, необходимую для изготовления качественной бумаги. Благодаря своим окислительным свойствам серная кислота также применяется в процессе отбеливания бумаги.
Еще одна важная сфера применения серной кислоты - гальваническое производство. Она используется в электрохимических процессах, позволяющих получать различные виды металлических покрытий. При этом серная кислота выполняет функцию электролита, обеспечивая электрохимическую реакцию между металлом и раствором.
В промышленности также активно применяется серную кислоту для очистки различного оборудования и трубопроводов от накипи и отложений. Она эффективно растворяет нежелательные отложения и позволяет восстановить исходную работоспособность оборудования. Более того, серная кислота может быть использована для очистки бассейнов, резервуаров и систем водоснабжения.
Таким образом, серная кислота является неотъемлемым компонентом для множества процессов и отраслей промышленности. Ее уникальные свойства и возможности делают ее незаменимым средством в производстве различных продуктов, качество которых напрямую зависит от ее использования.
Вопрос-ответ

Что происходит при взаимодействии серной кислоты с металлами?
При взаимодействии серной кислоты с металлами происходит реакция, в результате которой образуется соль и выделяется водородный газ. Серная кислота отдает протоны металлу, образуя соль металла и воду.
Какие металлы реагируют с серной кислотой?
С серной кислотой реагируют многие металлы, включая щелочные металлы, такие как натрий и калий, а также щелочноземельные металлы, такие как магний и алюминий. Реакция может происходить и с другими металлами, но скорость и интенсивность зависят от их активности и структурных особенностей.
Каковы последствия взаимодействия серной кислоты с металлами?
Последствия взаимодействия серной кислоты с металлами могут быть различными. Как правило, при этой реакции образуется соль металла и выделяется водородный газ. В зависимости от условий реакции, могут образовываться различные продукты, такие как сульфаты или сульфиты. Также возможно выделение тепла или образование осадка. Важно контролировать процесс реакции, чтобы избежать возможных опасных последствий, таких как выделение токсичных газов или разрушение реакционной смеси.
Почему происходит реакция между серной кислотой и металлами?
Реакция между серной кислотой и металлами происходит из-за различных химических свойств этих веществ. Серная кислота является сильным окислителем и имеет высокую кислотность, благодаря чему может отдавать протоны металлу. Металлы, в свою очередь, способны давать электроны, что позволяет им участвовать в реакции взаимодействия. Такое взаимодействие происходит в результате стремления системы достичь более низкой энергии и более стабильного состояния.
