Серная кислота – это химическое соединение, которое широко используется в промышленности и в нашей повседневной жизни. Ее применение связано с ее высокой реактивностью и кислотностью. Вместе с тем, серная кислота имеет сильное влияние на металлы, вызывая различные химические и физические изменения.
Взаимодействие металлов с серной кислотой провоцирует реакцию окисления, в результате которой образуется соответствующий солевой комплекс. Например, железо реагирует с серной кислотой, образуя сульфат железа и выделяяся водород. Такие реакции придают металлам новые физические свойства и могут привести к их коррозии или разрушению.
Многие металлы способны реагировать с серной кислотой, однако их реакции могут различаться в зависимости от их свойств и степени чистоты. Так, некоторые металлы, например, медь и свинец, могут растворяться в серной кислоте, образуя соответствующие соли. Другие металлы, например, алюминий и цинк, образуют защитную пленку оксида, которая предотвращает продолжение реакции.
Наблюдения за взаимодействием металлов с серной кислотой являются важными в химических исследованиях и применяются для определения характеристик и свойств металлов, а также для разработки новых материалов и технологий. Например, особенности реакции металлов с серной кислотой могут быть использованы для создания катодов и анодов в электрохимических аккумуляторах.
Взаимодействие серной кислоты с металлами
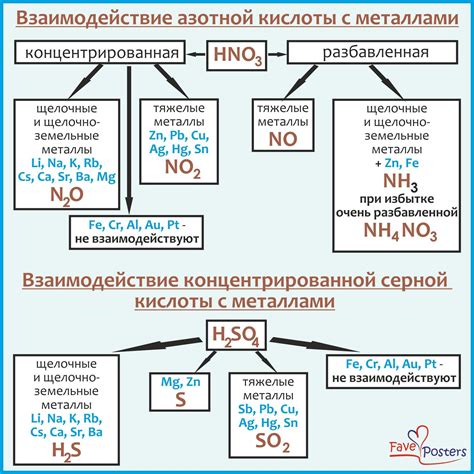
Серная кислота является одним из наиболее распространенных неорганических кислот и сильным окислителем, поэтому ее взаимодействие с различными металлами имеет свои особенности.
Когда серная кислота взаимодействует с металлами, происходит реакция окисления металла с образованием сульфата соответствующего металла и выделением водорода. Данная реакция является одной из самых характерных реакций взаимодействия кислоты и металла.
Особенности взаимодействия серной кислоты с металлами определяются рядом факторов, включая активность металла, концентрацию и температуру серной кислоты. Некоторые металлы, такие как натрий и калий, активно реагируют с серной кислотой, причиной этого является их высокая химическая активность.
Реакция взаимодействия серной кислоты с железом является одной из важнейших, так как она используется в промышленности для получения сульфата железа. Данная реакция является экзотермической, то есть сопровождается выделением тепла.
- Выводы:
- Серная кислота взаимодействует с металлами, образуя соответствующие сульфаты и выделяя водород.
- Особенности взаимодействия зависят от активности металла, концентрации и температуры кислоты.
- Реакция взаимодействия серной кислоты с железом является важной в промышленности.
Основные принципы химической реакции
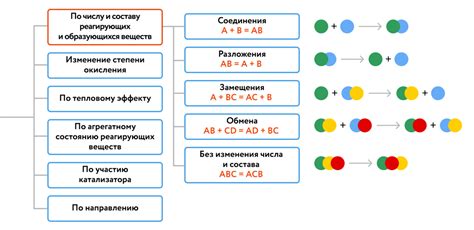
Химическая реакция - это процесс взаимодействия химических веществ, в результате которого происходит образование новых веществ с изменением их состава и свойств. Основные принципы химической реакции можно разделить на следующие:
- Закон сохранения массы: Масса реагирующих веществ должна быть равна массе образовавшихся продуктов реакции. В процессе химической реакции атомы не могут исчезать или появляться из ниоткуда, а только переходить из одних соединений в другие.
- Закон постоянства состава: Количество и типы атомов, входящих в молекулы реагирующих веществ и продуктов реакции, должны быть одинаковыми. То есть, вещества соединяются и разделяются в строго определенных пропорциях.
- Закон действующих масс: Скорость химической реакции пропорциональна концентрации реагирующих веществ. Скорость реакции может быть увеличена путем увеличения концентрации веществ, увеличения поверхности, повышения температуры или добавления катализатора.
- Принципы взаимодействия: Химическая реакция может происходить путем обмена ионами, образования связей между атомами, перестройки молекулярной структуры и других процессов, что определяет характер и результат реакции.
Понимание этих принципов позволяет анализировать и предсказывать результаты химических реакций, что имеет большое значение как в научных исследованиях, так и в различных промышленных и технологических процессах.
Факторы, влияющие на скорость реакции

Скорость реакции – важный показатель химической процесса, который может быть изменен разными факторами. Они могут оказывать как положительное, так и отрицательное влияние на скорость химической реакции.
1. Концентрация веществ
Концентрация реагентов является одним из основных факторов, влияющих на скорость реакции. Чем выше концентрация веществ, тем больше вероятность их столкновения и образования активированного комплекса. Это приводит к увеличению скорости реакции.
2. Температура
Температура также оказывает значительное влияние на скорость химической реакции. При повышении температуры, скорость реакции возрастает, так как реакции происходят с большей энергией. Повышение температуры приводит к увеличению скорости коллизий молекул и активации химической реакции.
3. Площадь поверхности
Площадь поверхности вещества играет важную роль в реакциях. Чем больше поверхность вещества, тем больше возможностей для взаимодействия молекул и, следовательно, происходит увеличение количества реакций и скорости химической реакции.
4. Катализаторы
Использование катализаторов позволяет ускорить реакцию, уменьшив энергетический барьер. Катализаторы активируют реагенты и облегчают сближение молекул для успешной реакции. Это позволяет реакциям протекать при более низких температурах и повышает их скорость.
Все эти факторы могут влиять на скорость химической реакции, что делает их очень важными при изучении химических процессов и их оптимизации.
Образование сульфатов и сульфатных отложений

Воздействие серной кислоты на металлы может приводить к образованию сульфатных соединений, которые являются основными продуктами реакции. Сульфаты образуются в результате окисления металлов, при этом серная кислота действует в качестве окислителя, передавая кислородные радикалы металлу.
Сульфатные соединения обладают разнообразными свойствами и широко применяются в различных отраслях промышленности. Некоторые из них имеют важное значение для сельского хозяйства, так как могут использоваться в качестве удобрений. Например, медный сульфат применяется в качестве фунгицида для борьбы с грибковыми заболеваниями растений.
Образование сульфатных отложений может быть проблемой в различных технических системах, таких как трубопроводы, паровые котлы и системы охлаждения. Это происходит из-за того, что сульфаты образуют твердые осадки, которые могут забивать трубы и препятствовать нормальному функционированию системы.
Для предотвращения образования сульфатных отложений могут применяться различные методы, такие как использование ингибиторов коррозии, фильтрация и реагентная обработка. Кроме того, регулярная очистка и поддержание оптимальных условий работы системы также помогают минимизировать образование отложений.
Таким образом, образование сульфатов и сульфатных отложений при воздействии серной кислоты на металлы является распространенным явлением, которое может иметь как положительные, так и отрицательные последствия в зависимости от контекста и условий применения.
Коррозия и разрушение металлических поверхностей

Коррозия - это процесс разрушения металлических поверхностей вследствие взаимодействия с окружающей средой. Основным фактором, вызывающим коррозию, являются химические реакции, происходящие между металлом и веществами в окружающей среде. Одним из наиболее распространенных веществ, вызывающих коррозию, является серная кислота.
Серная кислота проявляет сильное окислительное действие на металлы. При контакте с серной кислотой, металлическая поверхность может претерпеть различные изменения. Например, на поверхности железа происходит образование коррозионных пятен, которые с течением времени могут превратиться в язвенные повреждения. Латунные поверхности при взаимодействии с серной кислотой образуют темно-зеленую коррозию, в то время как на алюминиевой поверхности могут появляться белые пятна.
Коррозия серной кислотой происходит не только на поверхности металла, но и внутри его структуры. Это может привести к образованию трещин, пузырьков и других повреждений, которые снижают прочность и долговечность металлических конструкций. Кроме того, коррозия может приводить к нарушению нормального функционирования технических устройств и систем.
Для защиты металлических поверхностей от коррозии, используют различные методы и материалы. Возможными способами защиты являются нанесение защитных покрытий, применение антикоррозионных покрытий или использование специальных материалов, реагирующих с серной кислотой и предотвращающих ее дальнейшее воздействие на металлическую поверхность.
Химические свойства растворов серной кислоты

Серная кислота – это один из наиболее распространенных химических реагентов, используемых в лабораторных и промышленных целях. Она обладает рядом характерных химических свойств, которые определяют ее способность взаимодействовать с различными соединениями.
Первое заметное свойство растворов серной кислоты – их кислотность. Серная кислота является сильным кислотным соединением и проявляет свою кислотность при контакте с водой. Она способна отдавать протоны, что приводит к увеличению концентрации ионов водорода в растворе.
Второе важное свойство серной кислоты – она является окислителем. Она способна окислять множество веществ, в том числе металлы. Взаимодействие растворов серной кислоты с металлами приводит к образованию солей и выделению водорода. Некоторые металлы, такие как цинк и железо, активно реагируют с серной кислотой, при этом образуется солевой осадок и выделяется газ водород.
Также важно отметить, что растворы серной кислоты обладают сильной коррозионной активностью. Они способны разрушать металлы и многие органические соединения. При этом образуются новые вещества, которые могут иметь токсическое действие.
Однако не все металлы взаимодействуют с серной кислотой так активно. Например, металлы, образующие пассивные пленки оксида на поверхности, такие как алюминий или хром, могут быть устойчивы к взаимодействию с серной кислотой.
Наблюдения и эксперименты с серной кислотой и металлами

Серная кислота (H2SO4) является одним из наиболее распространенных и активных химических соединений. Она имеет сильно коррозионные свойства и способна вступать в реакцию с различными металлами. В ходе экспериментов было обнаружено, что некоторые металлы проявляют активную реакцию с серной кислотой, тогда как другие металлы практически не реагируют.
Одним из ярких примеров активной реакции металлов с серной кислотой является реакция соединения меди (Cu) с серной кислотой. При взаимодействии меди с серной кислотой происходит выделение газа и изменение цвета раствора. Сначала раствор приобретает зеленовато-голубой оттенок, затем становится синим. Результатом реакции является образование сульфата меди (CuSO4) и диоксида серы (SO2).
Кроме того, эксперименты показали, что серная кислота также может реагировать с железом (Fe). В результате взаимодействия железа с серной кислотой образуется сульфат железа (FeSO4) и выделяется газ. Наблюдается покраска раствора в зеленовато-желтый цвет, который со временем становится коричневым.
С другой стороны, некоторые металлы практически не реагируют с серной кислотой. Например, при взаимодействии серебра (Ag) с серной кислотой не наблюдается значительного изменения. Реакция между ними медленная и практически не приводит к образованию новых соединений.
Таким образом, эксперименты с серной кислотой и металлами позволяют наблюдать различные реакции и изменения, происходящие при взаимодействии этих веществ. Это свидетельствует о разной степени активности металлов и их способности реагировать с серной кислотой.
Вопрос-ответ

Каково влияние серной кислоты на металлы?
Серная кислота может реагировать с некоторыми металлами, образуя соли и выделяя водород. В результате этой реакции металл может корродироваться и разрушаться.
Какие металлы взаимодействуют с серной кислотой?
Взаимодействие серной кислоты происходит с различными металлами, включая алюминий, цинк, железо, никель и многие другие. Однако реакция может происходить в разной степени, в зависимости от концентрации и температуры кислоты.
