Серная кислота – это одно из наиболее распространенных и важных неорганических кислот. Она широко используется в различных отраслях промышленности и научных исследованиях, в том числе в химической промышленности, металлургии, электролитическом производстве и обработке материалов.
Одним из интересных и важных аспектов взаимодействия серной кислоты с металлами является возможность образования сульфатов металлов. Это особенно важно в тех случаях, когда требуется получить стойкие и прочные соединения для различных целей.
Сульфаты металлов, образующиеся при взаимодействии серной кислоты с металлами, имеют широкий спектр применений. Они могут использоваться в качестве катализаторов, красителей, коагулянтов и других веществ в различных отраслях промышленности. Кроме того, сульфаты металлов используются для производства удобрений, лекарственных препаратов и в других сферах человеческой деятельности.
Химические свойства серной кислоты при взаимодействии с металлами
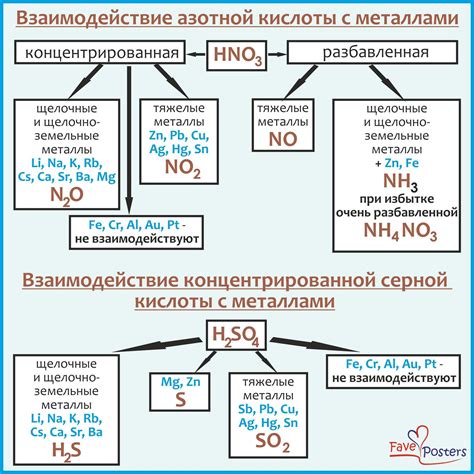
Серная кислота (H2SO4) является одним из наиболее распространенных и важных химических соединений. Она обладает высокой кислотностью и широко используется в различных отраслях промышленности.
Серная кислота взаимодействует с металлами, образуя соответствующие соли (сульфаты). При этом происходит реакция нейтрализации, в результате которой происходит образование воды и соли.
Взаимодействие серной кислоты с металлами происходит следующим образом: серная кислота отдает два протона, которые реагируют с металлом, образуя соответствующие ионы металла и водород. Например, при взаимодействии серной кислоты с цинком образуются сульфат цинка и молекулы воды:
H2SO4 + Zn → ZnSO4 + H2O
Реакция между серной кислотой и металлами характеризуется выделением водорода и образованием солей.
Применение данной реакции находит в различных областях промышленности, например, в гальваническом производстве, при производстве удобрений, в процессах очистки и обработки металлов и других применениях, где требуется получение солей металла.
Окислительные реакции серной кислоты и их значимость

Серная кислота (H2SO4) является одним из наиболее сильных окислителей и широко используется в различных химических процессах. Окислительные свойства серной кислоты обусловлены наличием в ее молекуле двух атомов кислорода, которые могут служить активными центрами для окисления различных веществ.
Взаимодействие серной кислоты с металлами является одним из основных процессов, при котором происходят окислительные реакции. При этом металлы могут быть окислены серной кислотой, а сами она восстанавливается. Такие реакции играют важную роль в производстве и электрохимии, а также находят применение в аналитической химии.
Одним из примеров таких реакций является окисление металлического железа серной кислотой. При этом происходит образование соли серной кислоты (сернокислого железа) и образование газообразного вещества – диоксида серы (SO2). Данная реакция используется, например, при производстве железосодержащих красителей, а также при получении серы из железа.
Окислительные реакции серной кислоты имеют большое значение в химической промышленности. Серная кислота широко применяется в процессах окисления органических веществ, получении красителей, удобрений и других продуктов химической промышленности. Также эти реакции широко применяются в аналитической химии для определения содержания различных веществ.
Коррозия металлов под воздействием серной кислоты

Серная кислота является одним из наиболее распространенных и агрессивных химических веществ, которые способны вызывать коррозию на металлических поверхностях. Наиболее часто подвержены коррозии металлы, такие как железо, алюминий, цинк и никель.
Коррозия металлов под воздействием серной кислоты происходит в результате реакции агрессивного кислотного окружения с металлом. В процессе этой реакции происходит образование сульфатов металлов, а металл сам постепенно разрушается.
Образовавшиеся при коррозии сульфаты могут затруднить эксплуатацию различных устройств, в том числе в области металлургии, нефтегазовой промышленности и производства химических веществ. Это связано с тем, что сульфаты образуют осадки и отложения на поверхности металла, что ведет к его дополнительному разрушению.
Для защиты металлов от коррозии под воздействием серной кислоты используются различные методы и материалы. Одним из таких методов является нанесение защитных покрытий на поверхность металла, которые предотвращают проникновение кислоты и контакт с металлом. Также используются специальные смазки и растворы, которые создают защитную пленку на поверхности металла.
Исследования в области взаимодействия серной кислоты с металлами по-прежнему актуальны. Они позволяют разрабатывать новые методы защиты металлов от коррозии, а также улучшать уже существующие способы и материалы, применяемые в различных отраслях промышленности.
Вопрос-ответ

Какие металлы взаимодействуют с серной кислотой?
Серная кислота может реагировать с различными металлами, включая железо, цинк, алюминий, медь и т.д. Взаимодействие металла с серной кислотой может привести к образованию солей серной кислоты и выделению водорода.
Каковы особенности взаимодействия серной кислоты с металлами?
Основная особенность взаимодействия серной кислоты с металлами заключается в том, что металл постепенно растворяется в серной кислоте, образуя соответствующие соли. При этом происходит выделение водорода и возникает химическая реакция, которая может идти с выделением тепла.
В каких сферах применяется взаимодействие серной кислоты с металлами?
Взаимодействие серной кислоты с металлами имеет широкое применение в различных сферах. Оно используется в процессе очистки металлических поверхностей от ржавчины или загрязнений. Также это взаимодействие может быть использовано в процессе производства батарей, аккумуляторов и других электрохимических устройств.
