Азотная кислота (HNO3) – одно из наиболее распространенных и активных окислителей, используемых в химической промышленности и лабораторных исследованиях. Ее разбавленный раствор представляет собой сильный окислитель, способный прореагировать с многими металлами. Взаимодействие разбавленной азотной кислоты с металлами может происходить по реакции окисления, образуя соответствующие нитраты.
В процессе реакции окисления азотная кислота (HNO3) отдаёт свои атомы кислорода, в результате чего происходит окисление металла. При этом образуются продукты реакции – нитраты металлов и выделяется оксид азота, который обычно присутствует в виде характерного желтого газа. Реакция окисления может происходить довольно интенсивно и взрывоопасно в зависимости от концентрации и условий обработки.
Пример уравнения реакции взаимодействия разбавленной азотной кислоты с металлом может быть следующим:
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Это уравнение показывает, что 3 молекулы меди (Cu) реагируют с 8 молекулами азотной кислоты (HNO3), образуя 3 молекулы нитрата меди (Cu(NO3)2), 2 молекулы оксида азота (NO) и 4 молекулы воды (H2O).
Таким образом, взаимодействие разбавленной азотной кислоты с металлами может привести к образованию соответствующих нитратов металлов, освобождению оксида азота и выделению воды. Эта реакция может применяться для получения нитратов металлов и в других химических процессах, требующих окисления металлических соединений.
Взаимодействие разбавленной азотной кислоты с металлами
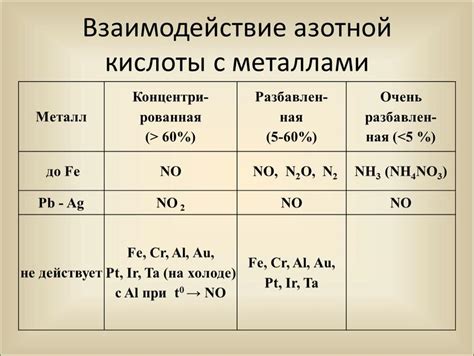
Азотная кислота (HNO3) является одной из самых сильных кислот и может взаимодействовать с различными металлами. В результате таких реакций образуются соответствующие соли и выделяется диоксид азота и вода. При этом металл может быть полностью растворен или реагировать только поверхностно.
Реакция взаимодействия азотной кислоты с металлом происходит в несколько этапов. Сначала происходит окисление металла, в результате которого образуется оксид металла и образующиеся нитраты. Затем образовавшиеся нитраты, благодаря своей растворимости, постепенно вымываются из металлической поверхности. Данный процесс может продолжаться до полного растворения металла или до достижения равновесия, при котором скорость вымывания нитратов равна их скорости образования.
Важно отметить, что взаимодействие азотной кислоты с металлами может протекать только при наличии воды и только в разбавленной форме кислоты. Концентрированная азотная кислота способна атаковать пассивные слои оксида на поверхности металла, что приводит к его пассивации. Поэтому для безопасного проведения реакций с металлами рекомендуется использовать разбавленные растворы азотной кислоты.
В результате взаимодействия разбавленной азотной кислоты с металлами могут образовываться разнообразные нитраты, такие как нитрат железа (III), нитрат меди (II), нитрат свинца (II) и т.д. Такие реакции находят широкое применение в химической промышленности и научных исследованиях.
Реакция между разбавленной азотной кислотой и металлическими элементами

Азотная кислота (HNO3) - это кислотное вещество, которое образуется при смешивании азотного ангидрида и воды. Когда разбавленная азотная кислота взаимодействует с металлическими элементами, возникает химическая реакция, в результате которой происходит образование нитратов и освобождение газа - диоксида азота.
Реакция азотной кислоты с металлами происходит по следующему уравнению: 2HNO3 + M → M(NO3)2 + H2O + NO2, где M - металлический элемент.
При этой реакции азотная кислота окисляет металл, тогда как сами нитраты являются окислителями. Газ - диоксид азота (NO2) имеет красно-коричневый цвет и характерный запах. Он образуется в результате разложения азотной кислоты при высоких температурах и имеет высокую токсичность.
Реакция разбавленной азотной кислоты с металлическими элементами используется в различных химических процессах, включая производство удобрений и нитратов для применения в сельском хозяйстве, а также в лабораторных условиях для синтеза различных соединений.
Важно отметить, что реакция между азотной кислотой и металлами является экзотермической, то есть сопровождается выделением тепла. При обработке металлов азотной кислотой необходимо соблюдать предосторожность и использовать защитное снаряжение, так как она является коррозионно активным веществом.
Уравнение реакции между азотной кислотой и металлами
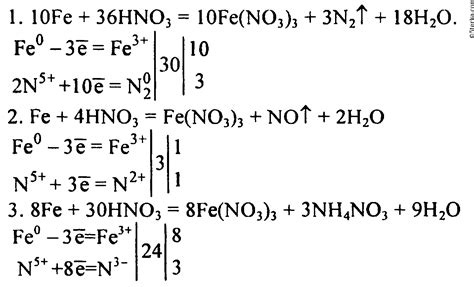
Азотная кислота (HNO3) является одной из самых сильных кислот и обладает выраженными окислительными свойствами. Это делает ее хорошим агентом для окисления металлов. Когда азотная кислота взаимодействует с металлом, образуется соль и выделяется оксид азота.
Уравнение реакции между азотной кислотой и металлами можно представить следующим образом:
- Азотная кислота + Металл → Соль + Оксид азота
Например, при взаимодействии азотной кислоты с медью (Cu), образуется нитрат меди (Cu(NO3)2) и оксид азота NO2.
| Реагенты | Продукты |
|---|---|
| HNO3 + Cu | Cu(NO3)2 + NO2 |
Реакция азотной кислоты с металлами протекает с выделением газообразного оксида азота, который может проявлять себя в виде ярко-красной или коричневой вспышки. Данная реакция является опасной и требует соблюдения мер безопасности.
Итак, уравнение реакции между азотной кислотой и металлами может быть представлено как простое химическое уравнение, в котором азотная кислота окисляет металл, образуя соль и выделяя оксид азота. Оксид азота проявляется в виде газообразного вещества, обладающего ярким цветом.
Вопрос-ответ

Какие металлы могут реагировать с разбавленной азотной кислотой?
Металлы, которые могут реагировать с разбавленной азотной кислотой, включают цинк (Zn), железо (Fe), алюминий (Al), медь (Cu) и свинец (Pb).
Какая реакция происходит между разбавленной азотной кислотой и металлами?
Реакция между разбавленной азотной кислотой и металлами приводит к образованию соответствующих нитратов металлов и выделению диоксида азота и воды.
Как можно описать уравнение реакции между разбавленной азотной кислотой и цинком?
Уравнение реакции между разбавленной азотной кислотой и цинком можно описать как: 2HNO3 + Zn -> Zn(NO3)2 + 2NO2 + H2O.
Какой продукт образуется при взаимодействии разбавленной азотной кислоты с медью?
При взаимодействии разбавленной азотной кислоты с медью образуется нитрат меди (Cu(NO3)2) и выделяется диоксид азота и вода.
