Растворы щелочей – это важный класс химических соединений, которые обладают высокой щелочностью и активно взаимодействуют с металлами. Этот процесс может привести к различным последствиям, включая образование гидроксидов металлов, выделение водорода и, в некоторых случаях, реакции горения. В данной статье мы рассмотрим основные аспекты взаимодействия растворов щелочей с металлами и его применение в различных областях.
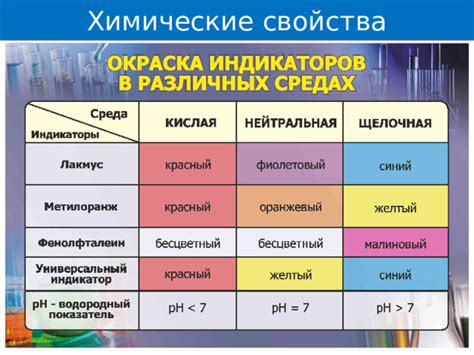
Одной из основных характеристик растворов щелочей является их pH-значение, которое говорит о концентрации гидроксидных ионов в растворе. Щелочные растворы обладают высоким pH-значением (от 7 до 14) и отличаются высокой щелочностью. Именно благодаря этой химической активности, они способны взаимодействовать с металлами и вызывать различные химические реакции.
Взаимодействие растворов щелочей с металлами может привести к образованию гидроксидов, которые играют важную роль в промышленности и медицине. Гидроксиды металлов широко применяются в качестве катализаторов, осадков для очистки сточных вод, а также в процессе производства электролитических растворов.
Взаимодействие растворов щелочей с металлами

Растворы щелочей являются сильными щелочными растворителями и активно взаимодействуют с металлами. Это происходит из-за высокой активности гидроксидов щелочей, которые вызывают окисление металлов и образуют соли и воду.
Взаимодействие растворов щелочей с металлами может протекать различными способами в зависимости от свойств металла и концентрации раствора щелочи. Например, некоторые металлы, такие как натрий и калий, реагируют с водой из раствора щелочи, образуя гидроксиды и выделяя водород. Другие металлы, такие как цинк и алюминий, реагируют соединениями щелочей, образуя соответствующие соли и выделяя водород.
Реакция взаимодействия растворов щелочей с металлами может проходить с выделением тепла. Если раствор щелочи содержит металл с низкой активностью, то реакция будет протекать медленно и незаметно. Однако растворы щелочей с металлами с высокой активностью могут даже вызвать воспламенение.
Важно отметить, что взаимодействие растворов щелочей с металлами может быть опасным, так как может привести к образованию вредных газов или коррозии металла. Поэтому необходимо соблюдать меры предосторожности при работе с растворами щелочей, такие как использование защитных очков и перчаток.
Свойства растворов щелочей
Растворы щелочей обладают рядом особых свойств, которые делают их полезными в различных промышленных процессах и химических реакциях.
Каустический эффект: Растворы щелочей обладают способностью вызывать каустический или жжение эффект при контакте с кожей или слизистыми оболочками. Это связано с высокой концентрацией гидроксидных ионов в щелочных растворах. Каустический эффект позволяет использовать растворы щелочей для удаления загрязнений, очистки поверхностей и дезинфекции.
Базические свойства: Растворы щелочей являются базами и обладают способностью отщелачивать или нейтрализовать кислоты. Это делает их важными компонентами в процессе регулирования pH, а также в реакциях, где требуется получение нейтрального или слабощелочного окружения.
Растворимость и проводимость: Растворы щелочей обычно хорошо растворяются в воде и имеют высокую электролитическую проводимость. Это связано с наличием ионов гидроксида (OH-) в растворе, которые являются электролитами. Высокая проводимость растворов щелочей делает их эффективными в использовании в электрохимических процессах и как электролиты в батареях.
Коррозионное воздействие: Растворы щелочей могут быть коррозивными для многих металлических материалов, особенно при высоких концентрациях и повышенных температурах. Это обусловлено их агрессивными свойствами и способностью реагировать с металлами, вызывая образование оксидов или гидроксидов металлов.
В целом, свойства растворов щелочей определяют их широкое применение в различных отраслях промышленности, медицине и быту. Важно учитывать их особенности и использовать с осторожностью, соблюдая меры безопасности при работе с ними.
Эффекты взаимодействия
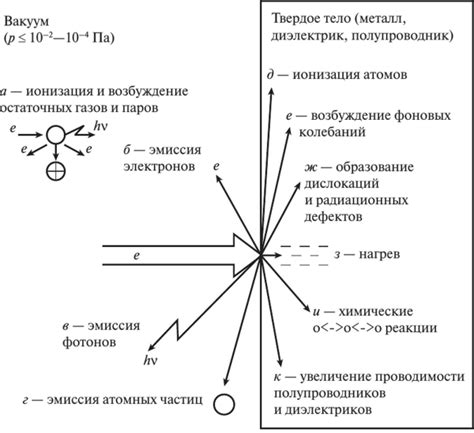
Взаимодействие растворов щелочей с металлами может приводить к различным эффектам, в зависимости от свойств самого металла и состава щелочного раствора.
Один из наиболее распространенных эффектов – образование газа. При взаимодействии щелочи с некоторыми металлами (например, алюминием, цинком или магнием) возникает химическая реакция, в результате которой выделяется водородный газ. Этот процесс часто сопровождается пузырьковым шипением и живым испарением металла.
Кроме образования газа, могут наблюдаться и другие эффекты. Например, при взаимодействии щелочных растворов с железом, может происходить окисление металла. В результате реакции образуется ржавчина или осаждается темно-синий оттенок оксида железа.
Другой интересный эффект – растворение металла в щелочном растворе. Некоторые металлы, такие как алюминий или цинк, могут растворяться в алкалиях, образуя соединения с щелочью, например, алюминаты или гидроксиды. Этот процесс может быть наблюдаемым визуально, так как металл постепенно исчезает, а раствор меняет цвет благодаря образованию соединений с металлом.
Взаимодействие растворов щелочей с металлами – это важный процесс в химии и может быть использован в различных областях, например, в производстве водорода или при создании защитных покрытий на металлических поверхностях.
Влияние металлов на растворы щелочей

Металлы играют важную роль во взаимодействии с растворами щелочей, так как они могут вызывать различные химические реакции и изменять свойства растворов. Прежде всего, металлы могут реагировать с щелочными растворами, образуя соли. Это происходит путем обмена ионами, при котором металлы отдают свои ионы катионым группам радикалов щелочных растворов.
Влияние металлов на растворы щелочей может также проявляться в изменении pH-значения раствора. Некоторые металлы могут вызывать щелочную реакцию, увеличивая концентрацию гидроксидных ионов. Другие металлы могут, напротив, вызывать кислотную реакцию, снижая концентрацию щелочных ионов.
Особый эффект имеет растворение металлов в щелочных растворах. При этом образуются комплексы, которые могут иметь различные свойства и применения. Например, растворение алюминия в щелочи приводит к образованию алюминатов, которые обладают высокой помехостойкостью и используются в производстве керамики и стекла.
Также важно отметить, что явление пассивации металлов может влиять на их взаимодействие с растворами щелочей. Пассивация - это процесс образования плотной защитной пленки на поверхности металла, которая предотвращает дальнейшее реагирование с окружающей средой. Возможность пассивации зависит от свойств металла и условий окружающей среды.
В целом, влияние металлов на растворы щелочей комплексное и зависит от множества факторов, таких как тип и концентрация металла, pH-значение раствора, присутствие других веществ и т. д. Понимание этих взаимодействий позволяет оптимизировать процессы химической обработки и разработать новые способы использования металлов и щелочных растворов в различных областях промышленности и научных исследований.
Практическое применение

Взаимодействие растворов щелочей с металлами находит широкое применение в различных областях, включая промышленность, науку и бытовую сферу.
Одним из главных практических применений этого процесса является промышленное получение металлов. Растворы щелочей, такие как гидроксид натрия или гидроксид калия, используются для растворения металлических руд, что позволяет извлекать металлы из земной коры. Такой процесс широко применяется в добыче алюминия, цинка, магния и других металлов.
Другим практическим применением взаимодействия растворов щелочей с металлами является использование этого процесса в гальванической обработке поверхностей. Растворы щелочей, например, гидроксид натрия, используются для очистки металлических поверхностей от загрязнений, окислов и других нежелательных веществ. Это позволяет получить чистую и гладкую поверхность металла, что в свою очередь улучшает сцепление с другими материалами, а также может применяться в декоративном покрытии металлических изделий.
В бытовой сфере взаимодействие растворов щелочей с металлами используется при очистке различных поверхностей и инструментов. Например, вы можете использовать раствор гидроксида натрия или гидроксида калия для удаления ржавчины с металлических поверхностей или очистки посуды от остатков пищи и отложений.
Таким образом, взаимодействие растворов щелочей с металлами имеет множество практических применений, от получения металлов до очистки поверхностей и предметов. Это делает этот процесс важным и неотъемлемым в различных областях деятельности человека.
Вопрос-ответ

Что такое щелочь и какие они бывают?
Щелочи - это химические вещества, обладающие щелочной реакцией. Щелочи могут быть разных типов, например, гидроксиды щелочных металлов (натрия, калия, лития и др.), аммиак и некоторые другие соединения. Они отличаются своими свойствами и применением.
Каким образом растворы щелочей взаимодействуют с металлами?
Растворы щелочей могут реагировать с металлами, образуя соли и выделяя водород. Эта реакция происходит за счет обмена ионами: щелочь отдает гидроксидные ионы OH-, а металл принимает ион водорода H+. Также металл может раствориться в щелочи с образованием соединений-гидроксидов металлов.
