Переходные металлы являются одной из наиболее интересных и важных групп элементов в таблице химических элементов. Они отличаются особыми свойствами и имеют широкий спектр применения в различных областях науки и техники. Еще одной особенностью переходных металлов является их способность взаимодействовать с водой. В данной статье мы рассмотрим особенности этого взаимодействия и роль, которую переходные металлы играют в процессах, связанных с водой.
Переходные металлы обладают уникальными электронными структурами, что позволяет им образовывать сложные соединения с водой. Одной из основных особенностей взаимодействия переходных металлов с водой является их способность вступать в реакцию с молекулами воды и образовывать гидроксиды. Гидроксиды переходных металлов являются важными компонентами в различных химических процессах и имеют широкое применение в промышленности.
Взаимодействие переходных металлов с водой также может сопровождаться образованием комплексных соединений. Комплексные соединения переходных металлов с водой обладают уникальными физическими и химическими свойствами, что делает их важными объектами исследования. Благодаря этим свойствам комплексные соединения находят широкое применение в катализе, металлургии, фармацевтике и других отраслях промышленности.
Взаимодействие переходных металлов с водой является активной областью исследований в химии и материаловедении. Понимание особенностей этого взаимодействия позволяет разрабатывать новые материалы с улучшенными свойствами и создавать новые технологии. Таким образом, изучение взаимодействия переходных металлов с водой имеет большую практическую значимость и способствует развитию науки и технологий.
Роль переходных металлов в процессе взаимодействия с водой
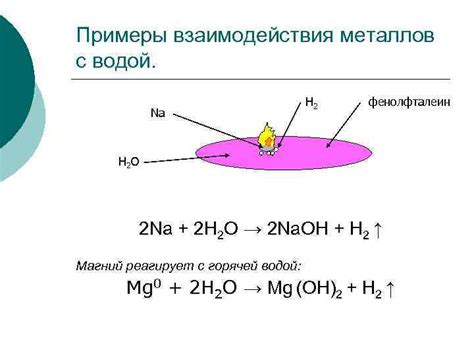
Переходные металлы играют важную роль в процессе взаимодействия с водой благодаря своим уникальным химическим свойствам. Они способны образовывать разнообразные соединения с водой, включая ионы и комплексы. Это обусловлено наличием их электронных оболочек, которые позволяют им проводить электрический ток и участвовать в различных реакциях.
Взаимодействие переходных металлов с водой происходит через процесс гидратации, когда ионы металла образуют соединения с молекулами воды. Этот процесс может быть различным в зависимости от характеристик самого металла, его окислительного состояния и условий реакции.
Одним из наиболее известных примеров взаимодействия переходных металлов с водой является реакция железа с водой, которая приводит к образованию гидроксида железа и выделению водорода. Эта реакция широко используется в промышленности для очистки воды от загрязнений и в процессе получения водорода.
Переходные металлы также активно применяются в качестве катализаторов в химических реакциях с участием воды. Например, комплексы платины и родия могут ускорять реакции окисления воды, превращая ее в кислород. Это имеет применение в производстве водорода, солнечных батарей и других энергетических систем.
В целом, взаимодействие переходных металлов с водой является активной областью исследований и имеет большое практическое значение в различных областях науки и технологий.
Особенности химического взаимодействия переходных металлов с водой

Переходные металлы обладают уникальными свойствами взаимодействия с водой, которые определяются их электронной структурой и возможностью образования ионов различной валентности.
Одной из особенностей взаимодействия переходных металлов с водой является их способность окислять воду, образуя катионы с положительными зарядами. Этот процесс происходит в присутствии кислорода и обеспечивает обратимость реакции, что делает переходные металлы важными катализаторами в таких процессах, как электролиз воды.
Другой особенностью взаимодействия переходных металлов с водой является их способность образовывать комплексные соединения с водой. Комплексные ионы переходных металлов с водой могут иметь различную степень гидратации, что зависит от координационного числа и вида переходного металла.
Вода также может влиять на степень окисления переходных металлов. Например, вода может помочь восстановить переходный металл из более высокого окисления в более низкое, если имеется подходящий снижающий агент. Это может быть использовано в различных процессах, включая очистку воды.
Применение переходных металлов в различных сферах

Переходные металлы - это группа элементов, которые находят широкое применение в различных сферах человеческой деятельности.
В катализе переходные металлы играют важную роль. Они способны ускорить химические реакции, увеличивая скорость образования продуктов или снижая энергию активации. Например, платина и родий используются в автомобильных катализаторах для превращения вредных газов в безопасные продукты.
Переходные металлы также используются в процессах окисления и восстановления. Они могут быть использованы для очистки загрязненных веществ, а также для получения высокоочищенных продуктов. Например, железо используется в процессе водоподготовки для удаления из воды избыточного количества органических веществ и металлов.
Кроме того, переходные металлы используются в электронике. Они могут быть использованы для создания проводников, транзисторов, конденсаторов и других электронных компонентов. Например, медь используется в электрических проводах и кабелях, так как она обладает хорошей проводимостью и стабильностью.
Переходные металлы также применяются в производстве стали, сплавов и магнитов. Например, железо, хром и никель используются для создания прочной и устойчивой к коррозии стали, которая применяется в строительстве и машиностроении.
Использование переходных металлов в различных сферах позволяет значительно расширить возможности человеческой деятельности, придавая материалам и веществам новые свойства и позволяя выполнять различные функции.
Потенциал переходных металлов для создания новых материалов и технологий

Переходные металлы представляют собой группу элементов, которые обладают уникальными свойствами и высокой активностью в химических реакциях. Именно благодаря этим особенностям они имеют огромный потенциал для создания новых материалов и технологий.
Одним из главных направлений исследований в области переходных металлов является их взаимодействие с водой. Вода является доступным и широко распространенным растворителем, поэтому изучение реакции переходных металлов с водой позволяет выявить новые свойства и возможности данных элементов.
Важным результатом таких исследований является разработка новых материалов и технологий на основе переходных металлов. Например, использование переходных металлов в катализаторах позволяет значительно увеличить скорость химических реакций и повысить эффективность процессов.
Переходные металлы также применяются при создании новых электронных материалов. Они обладают высокой проводимостью и магнитными свойствами, что делает их идеальными кандидатами для использования в различных электронных устройствах.
Кроме того, переходные металлы могут быть использованы в процессах очистки воды и воздуха. Их способность образовывать стабильные соединения с различными загрязняющими веществами позволяет эффективно удалять их из окружающей среды и снижать уровень загрязнения.
Таким образом, переходные металлы представляют огромный потенциал для создания новых материалов и технологий в различных сферах. Их уникальные свойства и активность открывают новые горизонты в науке и промышленности, способствуя развитию новых и инновационных решений.
Вопрос-ответ

В чем заключается особенность взаимодействия переходных металлов с водой?
Особенностью взаимодействия переходных металлов с водой является их способность образовывать ионы различной степени окисления и обладать разной активностью. Это обусловлено наличием внутренней электронной оболочки, которая позволяет переходным металлам легко изменять свою окисленность и образовывать соединения с разными степенями окисления.
Какие переходные металлы проявляют особую активность при взаимодействии с водой?
Некоторые переходные металлы, такие как натрий, калий и литий, проявляют особую активность при взаимодействии с водой. Они образуют гидроксиды, которые обладают щелочными свойствами. Это значит, что они способны образовывать растворы с щелочной реакцией, способные изменять pH-значение водных растворов.
