Реакции металлических оксидов с водородом представляют собой важный процесс, который приводит к образованию соответствующих гидридов. Этот тип реакций включает в себя сочетание металла с водородом, что приводит к выделению тепла и образованию структуры гидрида.
Уравнение такой реакции может быть представлено следующим образом: Металл + Водород → Гидрид. В этом уравнении металл обозначается символом M, а гидрид - символом MH. В процессе реакции металлических оксидов с водородом происходит уменьшение оксидационного состояния металла и окисление водорода.
Одной из особенностей взаимодействия оксида металла с водородом является его способность образовывать гидриды различной структуры. Некоторые металлы могут образовывать простые гидриды, в которых металл связан непосредственно с водородом.
Важно отметить, что реакция металлических оксидов с водородом имеет большое практическое значение. Например, такой процесс широко используется в промышленности при получении водорода. Кроме того, изучение взаимодействия оксида металла с водородом позволяет более глубоко разобраться в химических свойствах и поведении этих веществ.
Уравнение реакции оксида металла с водородом

Реакция оксида металла с водородом представляет собой процесс, при котором оксид металла вступает в химическую реакцию с молекулами водорода, образуя соответствующий металл и воду. Уравнение реакции можно записать следующим образом:
МО + H2 → М + H2О
Где МО обозначает оксид металла, М - металл, H2 - молекула водорода, H2О - молекула воды.
Уравнение реакции оксида металла с водородом отражает основную химическую превращение, происходящее в данной системе. В процессе реакции оксид металла вступает в контакт с молекулами водорода, что приводит к образованию металла и воды. В данном уравнении принимаются во внимание только основные реагенты и продукты реакции, без учета промежуточных стадий.
Уравнение реакции оксида металла с водородом является основой для объяснения процессов взаимодействия металлов с водородом, а также может быть использовано в химических расчетах и предсказании результатов реакций. Однако следует отметить, что реакция оксида металла с водородом может иметь дополнительные сложности и особенности, в зависимости от конкретного оксида металла и условий проведения реакции.
Физические особенности реакции оксида металла с водородом

Реакция оксида металла с водородом является химической реакцией, при которой происходит образование соединения металла с водородом. Эта реакция может протекать как при комнатной температуре, так и при повышенных температурах.
Одной из особенностей этой реакции является образование воды в результате соединения водорода с кислородом из оксида металла. При этом оксид металла сокращается, а водород окисляется. Реакция может проходить медленно или быстро в зависимости от конкретных условий, таких как температура, давление и наличие катализаторов.
Следует отметить, что окисление металла в реакции оксида металла с водородом может привести к образованию оксида металла с различной степенью окисления. Например, если металл имеет несколько степеней окисления, то при реакции с водородом может образоваться не только один оксид, но и другие соединения с различными степенями окисления металла.
В зависимости от специфики реакции оксида металла с водородом, может образовываться и другие продукты, помимо воды. Например, может происходить выделение газов, таких как аммиак или кислотные газы. Кроме того, в некоторых случаях возможно образование осадков в виде металлических частиц или металлосодержащих соединений.
Химические особенности реакции оксида металла с водородом
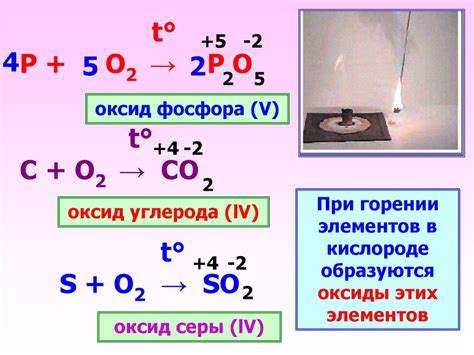
Реакция между оксидом металла и водородом является одной из важных химических реакций, которые имеют множество особенностей.
Во-первых, реакция оксида металла с водородом происходит с образованием воды. Это связано с тем, что водород и оксид металла обладают высокой активностью, их атомы обмениваются электронами, образуя ковалентную связь между атомами водорода и кислорода.
Во-вторых, при взаимодействии оксида металла с водородом может образовываться не только вода, но и характерные продукты реакции, такие как металлический гидрид, метанол или азотистая кислота. Это связано с тем, что оксиды металлов имеют различную химическую активность и способны образовывать различные продукты взаимодействия с водородом.
В-третьих, реакция оксида металла с водородом может происходить при различных условиях, включая различную температуру, давление и наличие катализаторов. Например, при нагревании оксида металла с водородом до определенной температуры может происходить спонтанное горение, сопровождающееся выделением тепла и света.
В заключение, реакция оксида металла с водородом является важным химическим процессом, который имеет свои особенности. Понимание этих особенностей позволяет более глубоко изучать и использовать данную реакцию в научных и промышленных целях.
Избирательность взаимодействия оксида металла с водородом

Взаимодействие оксида металла с водородом является сложным процессом, который подчиняется ряду особенностей. Одной из таких особенностей является избирательность взаимодействия, то есть способность оксида металла взаимодействовать только с определенными видами водорода.
Избирательность взаимодействия может быть обусловлена различными факторами, такими как размеры частиц оксида металла и водорода, а также их электрохимические свойства. Например, некоторые виды оксида металла могут образовывать стабильные соединения только с дейтерием, тяжелым изотопом водорода, в то время как другие могут образовывать соединения с обычным водородом.
Избирательность взаимодействия также может быть связана с тем, что разные виды оксида металла имеют разную аффинность к водороду. Некоторые оксиды металла могут активно взаимодействовать с водородом, образуя стабильные соединения, в то время как другие могут быть менее реактивными и мало взаимодействовать с водородом.
Избирательность взаимодействия оксида металла с водородом имеет важное практическое значение. Например, некоторые виды оксида металла используются в катализаторах для различных процессов в промышленности, связанных с водородом. При выборе катализатора необходимо учесть его способность взаимодействовать с водородом и выбрать оптимальный соединитель, который обеспечит нужное химическое превращение.
Влияние температуры на взаимодействие оксида металла с водородом
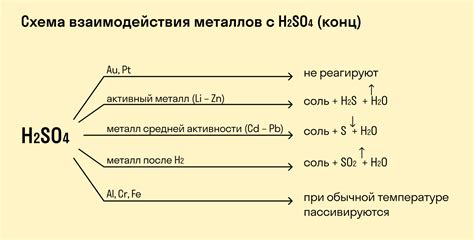
Температура является одним из ключевых факторов, влияющих на процесс взаимодействия оксида металла с водородом. При перегреве оксида металла происходит активационная энергия, что способствует более интенсивному процессу реакции.
При повышении температуры, скорость образования водорода становится выше, что может привести к ускоренному разложению оксида металла. Также следует отметить, что температура может влиять на степень окисления металла, что может приводить к обратимости реакции.
Исследования показывают, что при низких температурах, оксид металла может не взаимодействовать с водородом или процесс может протекать очень медленно. Однако с увеличением температуры, снижается энергия активации, что способствует более быстрому взаимодействию.
Необходимо отметить, что влияние температуры на взаимодействие оксида металла с водородом может быть различным в зависимости от конкретного металла и его оксида. Одни металлы могут показывать более высокую активность взаимодействия при повышении температуры, в то время как у других это взаимодействие может быть незначительным или отсутствующим.
Возможные побочные реакции взаимодействия оксида металла с водородом

Взаимодействие оксида металла с водородом может привести к возникновению различных побочных реакций, которые могут препятствовать или изменить основное химическое преобразование. Одной из возможных реакций является образование отложений металла на поверхности оксида. Это может привести к снижению эффективности реакции и образованию нежелательного катализатора.
Другой возможной побочной реакцией является окисление водорода, что может привести к образованию воды и других окислителей. Такое окисление может происходить как на поверхности оксида, так и внутри материала. В результате этого процесса может измениться состав и свойства исходного материала.
Кроме того, при взаимодействии оксида металла с водородом могут образовываться различные продукты газообразной и жидкой фазы. Например, в результате реакции может образоваться вода, оксид металла или его гидрид. Это может быть полезным, если целью реакции является получение данных продуктов, однако такие побочные реакции могут оказать негативное влияние на целевую химическую реакцию.
Таким образом, взаимодействие оксида металла с водородом может вызывать различные побочные реакции, которые нужно учитывать при планировании и проведении химических преобразований. Необходимо учитывать возможность образования отложений металла, окисления водорода, а также образования различных продуктов газообразной и жидкой фазы.
Применение реакции оксидов металлов с водородом в промышленности
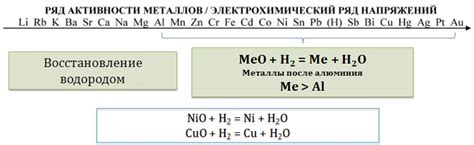
Реакция оксидов металлов с водородом активно применяется в промышленности для производства различных химических соединений и веществ. Эта реакция является одной из основных методов получения чистого металла из его оксида.
Оксиды металлов могут быть в виде руды или естественного минерала, и для получения металла из них необходимо провести процесс восстановления. Восстановление оксидов металлов с помощью водорода позволяет получить металлы высокой чистоты.
Промышленность использует реакцию оксидов металлов с водородом для производства таких веществ, как железо, никель, медь и алюминий. Например, при производстве железа из железной руды сначала выполняется реакция восстановления оксида железа (III) путем подачи водорода. Результатом этой реакции является получение чистого железа и отделение от него оксидов других примесей.
Кроме того, реакция оксидов металлов с водородом применяется в химической промышленности для получения различных химических соединений. Например, при производстве аммиака используется реакция восстановления оксида азота (III) водородом. Полученный аммиак широко применяется в производстве удобрений и других химических соединений.
Важно отметить, что реакция оксидов металлов с водородом является эндотермической и требует подачи тепла для ее осуществления. Это учитывается при проектировании и установке соответствующей оборудования в промышленности.
Взаимодействие оксида металла с водородом: потенциальные направления исследований

1. Изучение кинетики взаимодействия
Одним из потенциальных направлений исследований является изучение кинетики взаимодействия оксида металла с водородом. Изучение этого процесса позволит понять, как быстро и эффективно происходит реакция между оксидом металла и водородом. Такие исследования могут быть полезными при разработке катализаторов для химических процессов, связанных с водородом.
2. Роль оксида металла в присутствии водорода
Другим интересным направлением исследований является исследование роли оксида металла в присутствии водорода. Водород может взаимодействовать с оксидом металла, образуя новые соединения или меняя свойства существующих. Понимание этих процессов позволит разработать новые материалы с улучшенными свойствами и применением в различных сферах, включая энергетику и катализ.
3. Особенности реакции оксида металла с водородом
Одной из интересных особенностей реакции между оксидом металла и водородом является возможность образования воды. Вода может образовываться в результате реакции оксида металла с водородом, что может иметь важное практическое применение, например, при производстве водородного топлива. Исследования этой реакции позволят разработать эффективные методы получения водорода из оксида металла.
4. Влияние условий на взаимодействие
Исследование влияния различных условий на взаимодействие оксида металла с водородом также представляет интерес. Можно изучать, как температура, давление и концентрация веществ влияют на скорость и эффективность реакции. Эти исследования помогут определить оптимальные условия для получения желаемого продукта в реакции между оксидом металла и водородом.
Вопрос-ответ

Какую роль играет оксид металла при взаимодействии с водородом?
Оксид металла играет роль катализатора при взаимодействии с водородом. Он облегчает процесс реакции, снижая энергию активации и ускоряя образование новых соединений.
Какие особенности уравнения взаимодействия оксида металла с водородом?
Уравнение взаимодействия оксида металла с водородом имеет особенности в виде термодинамических и кинетических факторов. Например, термодинамические факторы могут определять, насколько сильно происходит реакция, а кинетические факторы могут влиять на скорость реакции.
Какие продукты образуются при взаимодействии оксида металла с водородом?
При взаимодействии оксида металла с водородом образуются вода и металл в основном в виде соответствующих гидридов. Например, оксид алюминия взаимодействует с водородом, образуя алюминиевый гидрид и воду.
Какова роль водорода при взаимодействии с оксидом металла?
Водород играет роль реагента при взаимодействии с оксидом металла. Он обеспечивает атомы водорода, которые реагируют с атомами кислорода в оксиде металла, образуя воду и освобождая металлические ионы.
