Металлы - это важная группа химических элементов, обладающих высокой электропроводностью, пластичностью и теплоотдачей. Они широко используются в промышленности, строительстве и производстве различных изделий. Взаимодействие металлов с другими веществами приводит к химическим реакциям, которые можно описать с помощью химических уравнений.
Одним из примеров взаимодействия металлов является реакция железа с кислородом. При нагревании железо окисляется, образуется оксид железа. Химическое уравнение данной реакции выглядит следующим образом:
4 Fe + 3 O2 → 2 Fe2O3
Другим примером реакции металлов является взаимодействие алюминия с хлором. При нагревании алюминий реагирует с хлором и образуется хлорид алюминия. Уравнение данной реакции:
2 Al + 3 Cl2 → 2 AlCl3
Таким образом, взаимодействие металлов с другими веществами является важным процессом в химии. Химические уравнения позволяют описать эти реакции и получить полное представление о протекающих процессах.
Взаимодействие металлов с водой: химические реакции и уравнения

Металлы могут взаимодействовать с водой, образуя химические реакции и оставляя следы процесса. Процесс взаимодействия между металлом и водой называется гидролизом. Он может протекать с различной интенсивностью и приводить к различным результатам.
Некоторые металлы, например, натрий и калий, очень активно реагируют с водой. При этом образуются соответствующие основания и выделяется водород. Реакция взаимодействия натрия с водой выглядит следующим образом:
2Na + 2H2O → 2NaOH + H2
В результате такой реакции образуется гидроксид натрия (NaOH) и выделяется водород (H2). При этом происходит горение водорода с искрой. Реакция между калием и водой происходит подобным образом.
Другие металлы, например, цинк или алюминий, реагируют с водой медленнее и менее интенсивно. Реакция взаимодействия цинка с водой можно представить следующим уравнением:
Zn + 2H2O → Zn(OH)2 + H2
В результате происходит образование гидроксида цинка (Zn(OH)2) и выделение молекул водорода (H2). Аналогичные реакции между водой и алюминием также приводят к образованию соответствующих гидроксидов и выделению водорода.
Следует отметить, что взаимодействие металлов с водой может быть использовано в различных практических целях. Например, водород, выделяемый при реакции металлов с водой, может использоваться в производстве водородных топливных элементов или в качестве энергоносителя.
Взаимодействие металлов с кислородом: примеры и химические уравнения

Взаимодействие металлов с кислородом является одной из основных химических реакций, которые происходят в природе. Кислород может оказывать влияние на металлы, вызывая их окисление и образование оксидов. Примеры таких реакций включают ржавление железа, окисление магния и алюминия.
Одним из наиболее распространенных примеров взаимодействия металлов с кислородом является ржавление железа. Когда железо взаимодействует с кислородом влажного воздуха или воды, образуется оксид железа (III), который имеет красно-коричневый цвет и называется ржавчиной. Химическое уравнение для этой реакции выглядит следующим образом:
4Fe + 3O2 → 2Fe2O3
Другим примером взаимодействия металла с кислородом является окисление магния. При нагревании магний реагирует с кислородом и образует оксид магния, который имеет белый цвет и называется магний оксидом. Химическое уравнение для этой реакции можно записать так:
2Mg + O2 → 2MgO
Взаимодействие металлов с кислородом имеет широкое применение в промышленности и быту. Окислительные свойства кислорода используются, например, при сварке и горениии. Знание химических реакций и уравнений, связанных с этими процессами, позволяет контролировать их и использовать в различных технологических процессах.
Реакция металлов с кислотами: примеры и уравнения
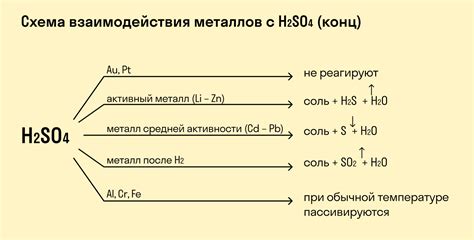
Реакция металлов с кислотами является одним из основных примеров химических реакций, которые могут происходить между различными веществами. Это взаимодействие обусловлено способностью кислот разрушать металлы и образовывать соли.
Одним из классических примеров реакции металлов с кислотами является реакция цинка с серной кислотой. При этом образуется соль цинка и водород. Уравнение этой реакции можно записать следующим образом:
Zn + H2SO4 → ZnSO4 + H2
Еще одним примером является реакция железа с соляной кислотой. В результате происходит образование соли железа и освобождение водорода. Уравнение этой реакции выглядит следующим образом:
Fe + 2HCl → FeCl2 + H2
На основе этих примеров можно сделать общий вывод о реакции металлов с кислотами: металл замещает водород в кислоте и образует соль. При этом в результате образуется водород, который можно наблюдать в виде пузырьков.
Взаимодействие металлов с солями: химические реакции и их уравнения

Взаимодействие металлов с солями может протекать различными способами, в зависимости от их электрохимических свойств. В химических реакциях между металлами и солями происходит обмен ионов, что приводит к образованию новых веществ.
К таким реакциям относятся реакции дисплейсмента, в которых один металл вытесняет из соли другой металл. Например, при взаимодействии меди и серной кислоты образуется сера и соль меди:
- Сu + H₂SO₄ → СuSO₄ + H₂S
Также металлы могут образовывать комплексы с солями, в которых металл координируется с частицами соли. Например, при взаимодействии меди и нитрата серебра образуется комплексное соединение:
- 2Cu + 2AgNO₃ → 2Ag + Cu(NO₃)₂
Реакции взаимодействия металлов с солями имеют большое практическое значение, так как могут использоваться в процессах получения металлов из руд, а также в производстве различных химических соединений. Такое взаимодействие может быть использовано для очистки воды от металлических загрязнений или для получения электрической энергии в гальванических элементах.
Реакция металлов с основаниями: примеры и уравнения
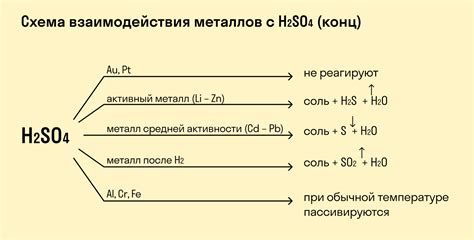
Взаимодействие металлов с основаниями является одним из важных процессов в химии. При этом происходит образование солей и выделение водорода. Результатом такой реакции является образование солей и выделение водорода. Например, реакция натрия с гидроксидом натрия выглядит следующим образом:
2Na + 2NaOH —> 2Na2O + H2
В данной реакции металл натрий вступает в реакцию с основанием гидроксид натрия, что приводит к образованию основы оксид натрия и выделению молекул водорода. Это явление можно наблюдать в виде пузырей, образующихся на поверхности металла во время реакции.
Также реакция алюминия с гидроксидом натрия является примером реакции металла с основанием. Ее уравнение выражается следующим образом:
2Al + 6NaOH —> 2Na3AlO3 + 3H2
В результате этой реакции образуется соль алюмината натрия и выделяется водород. В данной реакции металл алюминий реагирует с основанием гидроксид натрия, что приводит к образованию соли алюмината натрия и выделению водорода. Такие реакции имеют важное практическое значение и широко используются в различных сферах промышленности.
Взаимодействие металлов с неорганическими соединениями: примеры и химические уравнения

Металлы, как основные элементы химии, вступают во взаимодействие с различными неорганическими соединениями. При этом происходят химические реакции, которые характеризуются различными химическими уравнениями. Эти реакции задаются законами химии и могут быть использованы для получения новых веществ или промышленных процессов.
Одним из примеров взаимодействия металлов с неорганическими соединениями является реакция между металлом калием (K) и водой (H2O). В результате такой реакции образуется щелочь – гидроксид калия (KOH) и выделяется водород (H2). Химическое уравнение реакции будет выглядеть следующим образом:
2K + 2H2O → 2KOH + H2
Другим интересным примером является взаимодействие металла железа (Fe) с кислородом (O2) из воздуха. В результате такой реакции образуется оксид железа (Fe2O3), который называется ржавчиной. Химическое уравнение реакции имеет вид:
4Fe + 3O2 → 2Fe2O3
Также можно рассмотреть реакцию между металлом медью (Cu) и серной кислотой (H2SO4). В результате такой реакции образуется сульфат меди (CuSO4) и выделяется сероводород (H2S). Химическое уравнение реакции будет иметь следующий вид:
Cu + H2SO4 → CuSO4 + H2S
Таким образом, взаимодействие металлов с неорганическими соединениями является важным аспектом химии и позволяет исследовать свойства различных веществ, разрабатывать новые материалы и оптимизировать промышленные процессы.
Реакция металлов с органическими соединениями: примеры и уравнения
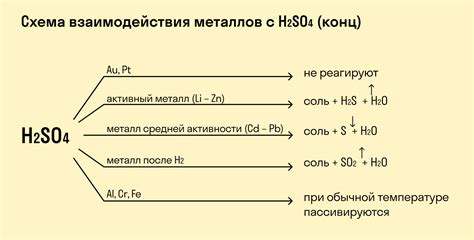
Металлы могут вступать в химические реакции с органическими соединениями, образуя различные продукты. Такие реакции имеют большое значение в синтезе органических соединений и представляют собой важный инструмент в органической химии.
Активные металлы, такие как натрий, калий или магний, могут реагировать с органическими соединениями, содержащими функциональные группы, такие как галогены, гидроксильные группы и амины. Например, реакция натрия с галогенированным углеводородом может привести к образованию соединения с новой C-N связью.
Ароматические соединения, такие как бензол, также могут реагировать с металлами, образуя соединения, называемые ареными комплексами. Например, взаимодействие бензола с алюминием может привести к образованию комплекса, в котором алюминий связан с ароматическим кольцом через π-связь.
Реакции металлов с органическими соединениями могут иметь как синтетическое, так и деструктивное значение. Например, взаимодействие металлов с органическими кислотами может привести к образованию солей металлов, которые могут использоваться в различных процессах синтеза. С другой стороны, реакции металлов с некоторыми органическими соединениями могут приводить к разрушению структуры молекулы, что может быть полезно в некоторых процессах очистки или переработки органических отходов.
В целом, реакции металлов с органическими соединениями представляют собой важный аспект органической химии, который позволяет образовывать новые соединения, изменять их свойства и использовать их в различных сферах промышленности и научных исследований.
Вопрос-ответ

Какие реакции могут происходить между металлами и кислородом?
Реакцией между металлами и кислородом является окисление металлов. К примеру, реакция между железом и кислородом приводит к образованию ржавчины - гидроксида железа(III) Fe(OH)3. Реакция между медью и кислородом приводит к образованию оксида меди(II) CuO. Реакция между алюминием и кислородом приводит к образованию оксида алюминия(III) Al2O3.
Какие еще реакции могут происходить между металлами и другими веществами?
Между металлами и кислотами может происходить реакция образования соли и выделения водорода. К примеру, реакция между цинком и серной кислотой приводит к образованию сульфата цинка и выделению водорода. Реакция между магнием и соляной кислотой приводит к образованию хлорида магния и выделению водорода. Между металлами и щелочами может происходить реакция образования соли и выделения водорода. К примеру, реакция между натрием и гидроксидом калия приводит к образованию соли НаK и выделению водорода.
Какая реакция происходит между алюминием и йодом?
Между алюминием и йодом происходит реакция образования тройного полиодида. В результате образуются кристаллы салетры - AlI3.
