Таблица Менделеева — это систематическое представление элементов, разделенных по группам и периодам в зависимости от их атомных свойств. Среди элементов таблицы особое место занимают металлы, которые составляют большую часть периодической системы. Металлы обладают рядом характерных свойств, таких как хорошая теплопроводность, высокая пластичность и электропроводность.
Металлы таблицы Менделеева взаимодействуют между собой, образуя различные соединения. Одним из наиболее распространенных типов взаимодействия металлов является сплавление. Сплавы представляют собой смеси двух или более металлов, которые обладают новыми свойствами в сравнении с их исходными компонентами. Сплавы применяются в различных отраслях промышленности, таких как машиностроение, химическая и энергетическая промышленность.
Металлы таблицы Менделеева также могут образовывать соединения с неметаллами. Например, соединения меди и серы образуют медные сульфиды, которые имеют важное применение в производстве меди и латуни. Также металлы могут реагировать с кислородом, образуя оксиды, которые являются основными компонентами многих металлических руд. Взаимодействие металлов с неметаллами позволяет создавать различные материалы с желаемыми свойствами для различных применений.
Металлы таблицы Менделеева и их химические свойства
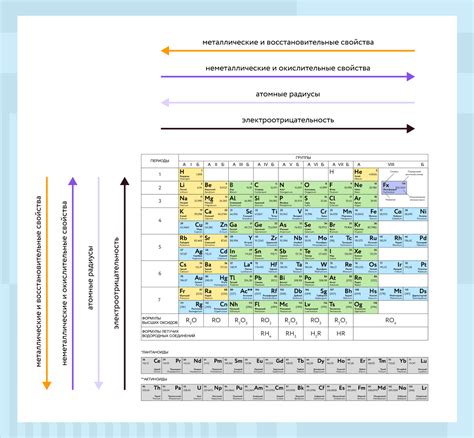
Металлы таблицы Менделеева - это элементы, обладающие определенными химическими свойствами. Они находятся слева от линии разделения в периодической системе и включают такие элементы, как железо, алюминий, медь и др.
Одним из основных химических свойств металлов является их способность образования ионов с положительным зарядом. Также металлы обладают высокой тепло- и электропроводностью, благодаря чему они широко используются в электротехнике и металлообработке.
Металлы также обладают характерной металлической блеской и свойством отбиваться. Они имеют высокую пластичность и деформируются без разрушения. Большинство металлов также являются твердыми при комнатной температуре, за исключением ртути.
Кроме того, металлы имеют различные химические реакции. Они могут образовывать соединения с не металлами и другими металлами, обладают способностью окисляться при взаимодействии с кислородом и растворяются в кислотах. Некоторые металлы обладают коррозионной стойкостью и используются в производстве специальных сплавов и материалов для работы в агрессивных средах.
Серебро, его химические свойства

Серебро (Ag) является мягким, блестящим металлом с высокой теплопроводностью и электропроводностью. Оно имеет атомный номер 47 в таблице Менделеева и химический символ Ag.
Одной из главных характеристик серебра является его устойчивость к окислению и коррозии. Это позволяет использовать его в ювелирной и медицинской промышленности.
Серебро также известно своей высокой рефлективностью света. Благодаря этому свойству, его широко используют для создания зеркал, фотографических пленок и оптических устройств.
Серебро может взаимодействовать с другими элементами и образовывать различные соединения. Некоторые из наиболее известных соединений серебра включают серебряные соли, такие как серебро нитрат (AgNO3) и серебро хлорид (AgCl), которые обладают антисептическими и противогрибковыми свойствами. Они широко используются в медицине и фармацевтике.
Серебро также имеет антимикробные свойства, что означает, что оно может убивать бактерии и другие микроорганизмы. Из-за этого свойства, его используют в производстве антимикробных поверхностей, медицинских препаратов и ортопедических имплантатов.
Золото, его реакции с другими веществами

Золото - благородный металл, отличающийся высокой устойчивостью к реакциям с другими химическими веществами. Однако, в некоторых условиях, оно все же может образовывать реактивные соединения.
Одной из наиболее известных реакций золота является его растворение в растворах цианида натрия. Эта реакция широко используется в золотодобывающей промышленности при обработке золотосодержащих руд. В результате реакции образуется комплексное ионное соединение, которое легко растворяется в воде.
Золото также может реагировать с хлоридами, образуя хлоридные соли. Например, реакция золота с хлоридом железа(III) приводит к образованию золотистого цвета, позволяя использовать этот тест для обнаружения примесей золота в различных образцах. Другой известной реакцией является взаимодействие золота с хлоридом серебра, при котором образуется черный осадок.
Аммиак также образует соединения с золотом. При действии аммиака на раствор золотих хлоридов, образуется так называемый аммиачный комплекс. Этот процесс используется в минералогии для выделения золота из минеральных образцов.
Таким образом, несмотря на общее низкое взаимодействие с другими веществами, золото способно образовывать реактивные соединения с цианидами, хлоридами и аммиаком.
Железо и его влияние на окружающую среду

Железо - один из самых распространенных металлов на Земле, которое широко используется в промышленности и строительстве. Однако, его взаимодействие с окружающей средой может оказывать отрицательное влияние на экосистему.
Одной из проблем, связанных с присутствием железа в окружающей среде, является его окисление при воздействии влаги и кислорода. Это приводит к образованию ржавчины, которая может проникать в почву и воду и загрязнять их.
Кроме того, промышленное использование железа может приводить к выбросам вредных веществ в атмосферу, таких как оксиды железа, которые взаимодействуют с другими веществами и образуют аэрозоли. Эти аэрозоли могут влиять на качество воздуха и вызывать проблемы с дыханием у людей.
Также, железо может оказывать негативное влияние на водные экосистемы. Повышенное содержание железа в воде может привести к образованию отложений, которые загрязняют водные ресурсы и могут навредить рыбам и другим водным организмам.
Разумное использование и утилизация железа и его соединений в промышленности и быту является важным фактором для снижения его негативного воздействия на окружающую среду. Необходимо соблюдать стандарты экологической безопасности и использовать современные технологии, чтобы минимизировать негативное влияние железа на окружающую среду и сохранить ее природные ресурсы.
Алюминий и его применение в промышленности

Алюминий является легким металлом, который обладает высокой прочностью, стойкостью к коррозии и хорошей проводимостью тепла и электричества. Благодаря этим свойствам, алюминий широко применяется в различных отраслях промышленности.
Одной из основных областей применения алюминия является авиационная промышленность. Легкость и прочность этого металла позволяют снижать вес самолетов, что приводит к уменьшению расходов топлива и экономии затрат. Алюминиевые сплавы также используются для производства крыльев, корпусов и других частей самолетов.
Алюминиевые сплавы широко применяются в производстве автомобилей. Они позволяют снизить вес автомобиля, улучшить топливную экономичность и обеспечить безопасность и комфорт вождения. Алюминиевые детали используются для производства кузовов, дверей, капотов, колесных дисков и других элементов автомобиля.
Алюминий также применяется в строительной промышленности. Он используется для производства оконных рам, дверей, фасадных систем, а также для создания легких и прочных конструкций. Кроме того, алюминиевые материалы широко применяются в производстве мебели и интерьерных деталей.
В электротехнике алюминий используется для производства проводов и кабелей. Он обладает хорошей электропроводностью и стойкостью к коррозии, что делает его незаменимым материалом для передачи электрической энергии.
Вполне очевидно, что алюминий имеет широкий спектр применения в различных отраслях промышленности. Его легкость, прочность и устойчивость к коррозии делают его незаменимым материалом для создания легких и надежных изделий.
Медь и ее электропроводность

Медь – один из самых известных и широко используемых металлов в мире. Она обладает высокой электропроводностью, что делает ее незаменимым материалом для проводников электрического тока.
Одной из причин высокой электропроводности меди является ее кристаллическая структура. Медь имеет упорядоченную решетку атомов, что способствует свободному перемещению электронов внутри материала. Благодаря этому, электроны легко передвигаются по проводнику, что обеспечивает высокую электропроводность.
Электропроводность меди также зависит от ее чистоты. Чем выше степень очистки меди от примесей и применяемых сплавов, тем выше будет электропроводность. Это объясняется тем, что примеси и сплавы ограничивают свободное движение электронов внутри материала.
Медь также обладает высокой теплопроводностью. Это делает ее подходящей для использования в множестве приложений, включая теплопроводящие трубы и радиаторы.
Как материал с высокой электропроводностью, медь находит широкое применение в электротехнике, электронике и промышленности. Она используется для изготовления проводов, кабелей, контактов, электронных компонентов и многого другого. Благодаря своим свойствам, медь продолжает оставаться одним из наиболее важных металлов в современном мире.
Никель и его применение в производстве сплавов

Никель – это d-блочный химический элемент с атомным номером 28 и символом Ni. Он обладает серебристым блеском и хорошей коррозионной стойкостью. Более половины всего производимого никеля в мире используется в производстве сплавов.
Никель является неотъемлемой частью нержавеющих сталей, которые широко применяются в различных отраслях, включая производство химических веществ, нефтепереработку, медицину и строительство. Нержавеющие сплавы обладают высокой прочностью, устойчивостью к высоким температурам и коррозии, что делает их незаменимыми материалами для производства различных компонентов, включая трубы, клапаны, котлы и сосуды.
Никелевые сплавы также нашли широкое применение в аэрокосмической, автомобильной и энергетической промышленности. Они используются для изготовления турбинных лопаток, пружин, валов и других деталей, работающих в экстремальных условиях. Никель обладает высокой устойчивостью к окислению и температуре, что делает его идеальным материалом для производства компонентов, работающих при высоких нагрузках и температурах.
Кроме того, никелевые сплавы также используются в производстве электрических проводов, батарей, монет и ювелирных изделий. Никель придает сплавам химическую стойкость, магнитные свойства и прочность, что делает его необходимым компонентом во многих промышленных и бытовых приложениях.
Титан и его устойчивость к коррозии

Титан - это легкий металл серебристо-серого цвета, который обладает высокой устойчивостью к коррозии. Это свойство делает титан одним из наиболее привлекательных материалов для использования в различных отраслях, в том числе в авиации, медицине и химической промышленности.
Титан образует защитную оксидную пленку на своей поверхности при контакте с кислородом из воздуха или водой. Эта пленка надежно защищает металл от дальнейшей коррозии и обеспечивает его устойчивость к агрессивным средам.
Защитная оксидная пленка особенно важна в морской среде, где титан используется в производстве кораблей и буровых платформ. Она позволяет титану противостоять соленой воде и другим вредным факторам, которые могут привести к быстрому разрушению других металлов.
Кроме того, титан имеет высокую стойкость к кислотам и щелочам, что делает его идеальным материалом для химической промышленности. Он не окисляется при контакте с агрессивными средами и сохраняет свои механические свойства в широком диапазоне рабочих температур.
В заключение, устойчивость титана к коррозии делает его незаменимым материалом во многих отраслях промышленности. Благодаря этому свойству титан может быть использован в условиях, где другие металлы быстро окисляются и разрушаются, обеспечивая при этом надежность и долговечность конструкций и изделий.
Вопрос-ответ

Что такое таблица Менделеева?
Таблица Менделеева - это систематическое представление химических элементов, разработанное русским химиком Дмитрием Ивановичем Менделеевым в 1869 году. Она упорядочена по возрастанию атомных номеров и группирует элементы по их свойствам и химическим реакциям.
Какие металлы входят в таблицу Менделеева?
В таблице Менделеева присутствует большое количество металлов, включая железо, алюминий, свинец, медь, цинк, серебро и золото, а также многие другие. Общее количество металлов в таблице составляет около 80 из 118 элементов.
Как взаимодействуют металлы в таблице Менделеева?
Металлы в таблице Менделеева взаимодействуют друг с другом и с другими элементами путем химических реакций. Они могут образовывать сплавы, соединения и агрегатные состояния с различными свойствами. Например, железо и медь могут соединяться для образования сплава бронзы.
Какое значение имеет взаимодействие металлов в таблице Менделеева?
Взаимодействие металлов в таблице Менделеева имеет большое значение для различных отраслей промышленности и науки. Металлы используются для производства различных материалов, оборудования и изделий. Они также играют важную роль в электротехнике, медицине и строительстве. Изучение взаимодействия металлов помогает развивать новые материалы и технологии.
