Металлы являются одними из наиболее распространенных материалов, которые мы используем в повседневной жизни. Вода, в свою очередь, является неотъемлемой частью нашей жизни. Поэтому важно изучать влияние взаимодействия металлов с водой и различные аспекты этого процесса.
Одним из факторов, влияющих на взаимодействие металлов с водой, является их ряд напряжений. Ряд напряжений металлов позволяет классифицировать металлы по их активности. Они классифицируются на основе их потенциала окисления в водных растворах. Металлы с более низким потенциалом окисления обладают большей активностью во взаимодействии с водой и могут проявлять различные химические и физические свойства.
Вода, как хороший растворитель, может взаимодействовать с различными металлами и вызывать разные реакции. Уровень реактивности металла соответствует его положению в ряду напряжений. Металлы с более высоким потенциалом окисления имеют большую тенденцию окисляться в водных средах. Взаимодействие металлов с водой может приводить к образованию окислов, гидроксидов, солей и других соединений, что влияет на их химические свойства и структуру.
Раздел 1. Исследования влияния напряжений на металлы

Влияние ряда напряжений на поведение металлов во взаимодействии с водой является важной исследовательской темой среди ученых и инженеров. Многие металлы могут быть подвержены коррозии под действием воды и влажной среды, и качество их поверхностей может сильно изменяться при различных видах напряжений. Поэтому для понимания и улучшения долговечности металлических конструкций и изделий необходимо изучить, как напряжения влияют на металлы в контакте с водой.
Одним из основных направлений исследований является изучение коррозии металлов под воздействием различных видов напряжений, таких как механическое, электрическое и термическое напряжения. Влияние механического напряжения на коррозию металлов хорошо изучено и подтверждено множеством экспериментов и наблюдений. Электрическое напряжение также играет важную роль в коррозии металлов, особенно в случаях гальванической коррозии при контакте разных металлов с водой. Термическое напряжение также может оказывать влияние на поведение металлов, особенно при обработке путем нагрева или охлаждения.
Другим важным аспектом исследований является анализ взаимодействия металлов с водой и образования оксидных пленок на их поверхности. Оксидные пленки играют важную роль в защите металлов от коррозии, и их формирование может быть различным в зависимости от вида напряжений, приложенных к металлу. Исследования позволяют определить, какие виды напряжений способствуют формированию эффективных защитных пленок, а какие, наоборот, усиливают процессы коррозии.
Итак, исследования влияния напряжений на металлы взаимодействующие с водой позволяют улучшить понимание процессов коррозии и формирования защитных оксидных пленок на металлических поверхностях. Эти исследования имеют большую практическую значимость для разработки новых материалов и технологий, повышающих долговечность и надежность металлических конструкций и изделий в условиях воздействия воды.
Положительное воздействие

Ряд напряжений металлов оказывает положительное воздействие на их взаимодействие с водой. Когда металлы находятся в различных электрохимических состояниях, они могут обладать различной активностью в реакциях с водой.
Например, металлы с более низкими значениями электродного потенциала, такие как магний и цинк, имеют большую активность в реакциях с водой. Они быстрее вступают в реакцию с водой и выделяют водородный газ.
Это положительное воздействие может быть использовано в различных приложениях. Например, водород, выделяющийся в результате реакции металла с водой, может быть использован как источник энергии или водородного топлива.
Кроме того, положительное воздействие напряжений металлов на их взаимодействие с водой может быть использовано для очистки воды от загрязнений. Некоторые металлы, взаимодействуя с водой, могут образовывать соединения, которые обладают свойствами сорбентов и способны поглощать различные загрязнители.
Таким образом, ряд напряжений металлов играет важную роль в их взаимодействии с водой, открывая новые возможности для использования этих процессов в различных областях, включая энергетику и очистку воды.
Отрицательное воздействие

Влияние ряда напряжений металлов на их взаимодействие с водой может иметь отрицательные последствия. При наличии напряжений, некоторые металлы могут выделяться из воды и образовывать токсичные соединения.
Один из негативных эффектов - коррозия металлов. Вода, особенно если она содержит соли, может привести к окислительно-восстановительным реакциям с поверхностью металла, что приводит к его разрушению и образованию коррозионных продуктов. Это может вызывать серьезные проблемы с инфраструктурой, например, повреждениями конструкций, трубопроводов и сооружений.
Некоторые металлы, особенно тяжелые металлы, могут иметь токсичное воздействие на организм человека и животных. Если металл попадает в воду, то оно может стать загрязненным и привести к серьезным заболеваниям. Например, свинец, марганец, ртуть и кадмий являются ядовитыми элементами, которые могут вызывать отравление и различные заболевания.
Влияние ряда напряжений металлов на воду также может негативно сказаться на экосистемах. Токсичные соединения, выделяющиеся из металлов, могут нанести ущерб растениям и животным, а также изменить биологическое разнообразие водных экосистем. Это может привести к нарушению природного равновесия и угрожать жизни многих организмов.
Раздел 2. Реакция металлов на взаимодействие с водой

Взаимодействие металлов с водой имеет важное значение для понимания их химических свойств и использования в различных областях науки и промышленности. При контакте с водой металлы могут проявлять разные реакции, включая растворение, образование газов и образование оксидов.
Наиболее активные металлы, такие как натрий и калий, реагируют с водой с выделением водорода и образованием щелочи. Натрий плавает на поверхности воды, при этом сильно шипит и образуется горячая водородная пленка. Калий также реагирует с водой с выделением водорода, но при этом может происходить самовоспламенение. Такие реакции обусловлены высокой активностью металлов и их способностью образовывать ионы гидроксида.
Менее активные металлы, такие как железо и алюминий, реагируют с водой медленнее. В случае железа, реакция происходит с образованием ржавчины, при этом выделяется водородный газ. Алюминий образует оксиды и гидроксиды, что делает его более устойчивым к взаимодействию с водой. Однако, при нагреве алюминий может реагировать с водой с образованием водорода.
Взаимодействие металлов с водой зависит также от их электрохимического потенциала. Металлы, имеющие более низкий потенциал, обычно менее активно реагируют с водой. Например, медь и серебро реагируют с водой очень медленно и требуют специальных условий для активации.
Таким образом, реакция металлов на взаимодействие с водой зависит от их активности и электрохимического потенциала. Понимание этих особенностей позволяет улучшить прогнозирование поведения металлов в различных условиях и использовать их эффективно в различных областях науки и промышленности.
Окисление металлов

Окисление металлов - это процесс, в ходе которого металлы взаимодействуют с водой или кислородом из воздуха и образуют оксиды. Данный процесс является важным в химии и имеет различные практические применения.
Окисление металлов является электрохимической реакцией, которая протекает при наличии электролита, такого как вода. В процессе окисления металлы теряют электроны и становятся положительно заряженными ионами.
Факторы, влияющие на скорость окисления металлов, включают концентрацию растворенного кислорода, присутствие других химических веществ, уровень pH и температуру окружающей среды. Некоторые металлы, такие как золото и платина, не подвержены окислению в обычных условиях, тогда как другие, например железо и алюминий, подвержены легкому окислению.
Окисление металлов играет важную роль в технологических процессах, таких как производство стали и алюминия. Оно также может быть причиной коррозии металлических поверхностей, что приводит к их разрушению. В пищевой промышленности окисление металлов может привести к изменению вкуса и качества продуктов.
Химические свойства металлов в воде
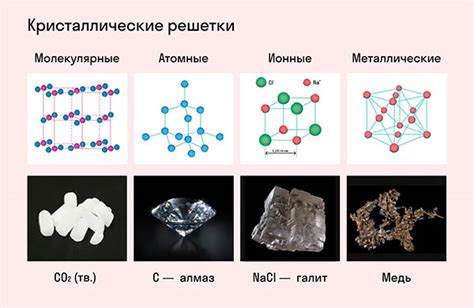
Металлы обладают различными химическими свойствами, включая взаимодействие с водой. Это взаимодействие может быть разнообразным и зависит от структуры и свойств конкретного металла.
Некоторые металлы, такие как литий и натрий, реагируют с водой очень активно, образуя водород и гидроксид металла. При этом происходит бурное окислительно-восстановительное взаимодействие, которое сопровождается выделением тепла и пузырьков газа.
Другие металлы, например серебро или золото, почти не реагируют с водой. Они обладают высокой химической инертностью и могут продолжать оставаться нереактивными при контакте со средой.
Некоторые металлы могут участвовать в реакциях окисления на воздухе, что в свою очередь может повлиять на реакцию с водой. Например, железо может реагировать с водой и окисляться, образуя гидроксид железа и выделяя водород.
Металлы могут иметь разную скорость реакции с водой. Например, некоторые металлы реагируют с водой медленно, постепенно образуя оксидные слои на поверхности металла. Эти оксидные слои могут предотвращать дальнейшую реакцию металла с водой.
Также важно отметить, что некоторые металлы могут реагировать с водой только при наличии дополнительных условий, например, при наличии кислорода или кислотных условиях. Это связано с тем, что реакция металлов с водой является сложным процессом, который зависит от множества факторов.
Физические свойства металлов в воде

Металлы обладают различными физическими свойствами во взаимодействии с водой, такими как растворимость и реактивность. Растворимость металлов в воде зависит от их химической природы и может быть разной для разных металлов.
Некоторые металлы, такие как натрий, калий и магний, растворяются в воде с образованием ионов, что делает их электролитами. Электролитические свойства этих металлов позволяют им проводить электрический ток в водном растворе.
Другие металлы, такие как железо и алюминий, не растворяются в воде, но могут реагировать с ней, образуя оксиды или гидроксиды. Взаимодействие этих металлов с водой зависит от pH раствора и присутствия окислителей или восстановителей.
Физические свойства металлов в воде также связаны с их электрохимическим поведением. Напряжения, которые развиваются на границе раздела металл-вода, можно использовать для определения активности металла и его способности корродировать в водной среде.
Исследование физических свойств металлов в воде имеет важное практическое значение, так как позволяет оценить их стойкость к коррозии и электролизу. Это важно для различных отраслей, включая строительство, энергетику и производство химических веществ.
Раздел 3. Роль напряжений во взаимодействии металлов с водой

Взаимодействие металлов с водой является сложным процессом, который может быть определен влиянием напряжений на данное взаимодействие. Когда металлы погружаются в воду, возникает электрохимическая реакция, в результате которой могут образовываться различные вещества.
Напряжения, возникающие при взаимодействии металлов с водой, могут влиять на скорость реакции, а также на тип и количество образовавшихся веществ. Некоторые металлы, такие как алюминий и цинк, при контакте с водой могут образовывать гидроксиды, которые являются основаниями и обычно растворяются в воде с образованием ионов гидроксида.
Другие металлы, например железо, могут образовывать оксидные пленки на своей поверхности при взаимодействии с водой. Эти пленки могут служить защитой от дальнейшего окисления металла. Однако, вносимые в воду напряжения могут приводить к разрушению пленки и продолжению окислительной реакции. В результате образуется ржавчина.
Изучение влияния напряжений на взаимодействие металлов с водой является важным фрагментом исследований в области коррозии и защиты металлов от окисления. Это позволяет лучше понять процессы, происходящие при контакте металлов с водой, и разработать специальные меры для защиты металлических конструкций от нежелательного воздействия окружающей среды.
Увеличение реактивности
Взаимодействие металлов с водой обусловлено их химической активностью. Изменение условий взаимодействия может привести к увеличению реактивности металлов.
Одним из факторов, влияющих на реактивность, является ряд напряжений металлов. Этот ряд представляет собой порядок, в котором металлы обладают различной способностью вступать в химические реакции с водой. Степень реактивности металла в значительной степени зависит от его положения в ряде напряжений. Так, металлы, находящиеся выше в ряде, обычно реагируют с водой более активно, чем металлы, находящиеся ниже.
Увеличение реактивности металлов может привести к ускоренному взаимодействию с водой и образованию соответствующих химических реакций. Например, некоторые металлы могут растворяться в воде с образованием соответствующих ионов. Другие металлы могут образовывать оксиды или гидроксиды при контакте с водой. Эти процессы могут привести к образованию химического движения или даже выбросу газов, что может быть опасным для окружающей среды и человеческого здоровья.
Поэтому, при изучении взаимодействия металлов с водой необходимо учитывать их реактивность и проводить соответствующие эксперименты и исследования для оценки влияния различных факторов, включая ряд напряжений металлов, на процессы, происходящие при контакте с водой.
Снижение стабильности
Эксперименты показали, что ряд напряжений металлов оказывает значительное влияние на их взаимодействие с водой. Одним из основных эффектов этого взаимодействия является снижение стабильности металлов.
Стабильность металлов обусловлена их способностью сохранять свои физико-химические свойства в определенных условиях. Однако при воздействии воды и присутствии определенных напряжений металлы могут изменять свою структуру и свойства, что приводит к снижению их стабильности.
Снижение стабильности металлов может проявляться в различных процессах, таких как коррозия, окисление и деградация структуры. Эти процессы могут быть вызваны как механическими воздействиями, так и химическими реакциями с водой.
Снижение стабильности металлов в результате их взаимодействия с водой имеет значительное значение как в научных исследованиях, так и в промышленности. Изучение этого явления позволяет более точно прогнозировать поведение металлов в различных условиях и разработать способы защиты от нежелательных последствий взаимодействия с водой.
Вопрос-ответ

Какие металлы оказывают наибольшее влияние на взаимодействие с водой?
Наибольшее влияние на взаимодействие с водой оказывают металлы с высокой электрохимической активностью, такие как калий, натрий и литий.
Как ряд напряжений металлов влияет на их способность реагировать с водой?
Ряд напряжений металлов показывает их способность реагировать с водой. Металлы с более высокими значениями в ряду будут более активно реагировать с водой, образуя гидроксиды и выделение водорода.
Какие результаты исследований говорят о влиянии ряда напряжений металлов на их реакцию с водой?
Результаты исследований показывают, что металлы с более высокими значениями в ряду напряжений, такие как алюминий и цинк, реагируют более активно с водой и способны образовывать более гидрофильные оксидные пленки.
Какие факторы влияют на взаимодействие металлов с водой помимо ряда напряжений?
Помимо ряда напряжений металлов, на взаимодействие с водой также влияют факторы, такие как концентрация раствора, температура и наличие примесей. Эти факторы могут ускорять или замедлять реакцию металлов с водой.
Каковы практические применения исследований влияния ряда напряжений металлов на их взаимодействие с водой?
Исследования влияния ряда напряжений металлов на их взаимодействие с водой имеют практические применения в различных областях, включая электрохимическую энергетику, коррозию и защиту металлов, производство водорода и использование его в топливных элементах.
