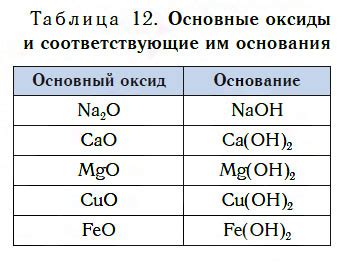
Вода – это химическое соединение, состоящее из двух атомов водорода и одного атома кислорода. Она является универсальным растворителем и важным компонентом для многих химических реакций. Некоторые металлы могут реагировать с водой, образуя оксиды – соединения, содержащие кислород. Эти реакции могут протекать с выделением газов и проявляться через изменение цвета или состояния металла.
В качестве примера можно привести металл натрия, который активно реагирует с водой. Когда металлонатрий погружается в воду, натрий окисляется, а вода восстанавливается. Результатом реакции является образование оксида натрия (Na2O) и выделение водорода (H2). При этом вода может производиться в невероятном количестве и может даже взорваться, если реакция протекает слишком интенсивно.
Также стоит упомянуть алюминий, который также реагирует с водой, образуя оксид алюминия (Al2O3). Однако, в отличие от натрия, реакция алюминия с водой проходит медленно из-за защитной оксидной пленки, которая образуется на его поверхности и замедляет процесс окисления. В результате реакции образуется водород газ, который выделяется в виде пузырьков, а поверхность алюминия покрывается тонкой пленкой оксида.
Металлы и оксиды
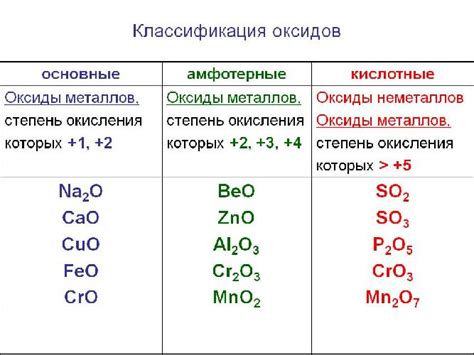
Металлы — это химические элементы, обладающие хорошей электропроводностью и способностью образовывать ионные связи. Многие металлы реагируют с водой, образуя оксиды.
Одним из примеров такой реакции является взаимодействие металла натрия с водой:
- Металл натрия хорошо растворяется в воде, образуя гидроксид натрия (NaOH) и выделяя водород (H2).
- Оксид натрия (Na2O) образуется только при реакции натрия с кислородом.
Другой пример реакции металла с водой — взаимодействие калия:
- Металл калия также реагирует с водой, приводя к образованию гидроксида калия (KOH) и выделению водорода.
- Оксид калия (K2O) образуется при нагревании калия с кислородом.
Таким образом, металлы, такие как натрий и калий, реагируют с водой, образуя оксиды только при взаимодействии с кислородом. Вода служит лишь промежуточным продуктом реакции, в которой образуются гидроксиды металлов и выделяется водород.
Реакция воды и металлов

Металлы различаются по своей реакционной способности с водой - некоторые из них реагируют с водой, образуя водородный газ и оксид металла. Это явление называется реакцией металла с водой.
Существуют две категории металлов в зависимости от скорости и интенсивности их реакции с водой:
- Активные металлы: натрий (Na), калий (K), магний (Mg), цезий (Cs) и другие. Они реагируют с водой очень быстро и под влиянием реакции происходит выброс пузырьков водорода.
- Малоактивные металлы: алюминий (Al), цинк (Zn), железо (Fe) и другие. Они реагируют с водой медленно и образуют металлический оксид и водородный газ.
В зависимости от химических свойств металла и условий реакции, оксид может иметь различную степень окисления и состав. Например, оксид алюминия (Al2O3) образуется при реакции алюминия с водой и является нерастворимым в воде.
Реакция металлов с водой имеет практическое значение и используется в различных отраслях, таких как производство водорода, генерация энергии и технологические процессы.
Следует отметить, что не все металлы реагируют с водой. Некоторые металлы, такие как серебро (Ag), золото (Au) и платина (Pt), не реагируют или реагируют только при наличии определенных условий, таких как повышенная температура или использование сильных окислителей.
Оксиды в результате реакции

Ряд металлов способен реагировать с водой, образуя оксиды. Оксиды имеют важное значение в химии и применяются в различных областях, таких как производство керамики и электроники.
Реакция металла с водой происходит с образованием оксида и выделением водорода. Оксиды образуются благодаря окислительной способности металлов, которые вступают в реакцию с кислородом из воды.
Одним из самых известных примеров такой реакции является реакция натрия с водой. В результате этой реакции образуется гидроксид натрия (NaOH) и выделяется водород. Реакция имеет значительную энергетическую характеристику и может протекать с большой интенсивностью.
Кроме натрия, с водой реагируют также другие щелочные металлы, такие как калий и литий. При реакции этих металлов с водой также образуются гидроксиды и выделяется водород. Эти металлы относятся к активным металлам и имеют высокую реакционную способность.
Среди дополнительных примеров можно привести магний и алюминий, которые также реагируют с водой. При этом образуются гидроксид магния (Mg(OH)2) и гидроксид алюминия (Al(OH)3). Эти металлы относятся к переходным металлам и обладают более низкой реакционной способностью по сравнению с щелочными металлами.
Таким образом, металлы реагируют с водой, образуя оксиды, которые имеют различные свойства и применения. Эта реакция играет важную роль в химической промышленности и научных исследованиях, а также имеет большое практическое значение в различных отраслях промышленности.
Вопрос-ответ

Какие металлы реагируют с водой?
Многие металлы способны реагировать с водой, образуя оксиды. Например, натрий (Na), калий (K), кальций (Ca) и магний (Mg) соответствуют активной серии металлов и реагируют с водой.
Какие оксиды образуются при реакции металлов с водой?
При реакции металлов с водой образуются соответствующие оксиды. Например, натрий (Na) образует оксид натрия (Na2O), калий (K) образует оксид калия (K2O), кальций (Ca) образует оксид кальция (CaO) и магний (Mg) образует оксид магния (MgO).
Какие металлы взаимодействуют с водой, образуя оксиды?
Взаимодействие металлов с водой и образование оксидов зависит от их активности. Металлы, находящиеся выше в активной серии, более активны и реагируют с водой. Например, натрий (Na), калий (K), кальций (Ca) и магний (Mg) реагируют с водой, образуя соответствующие оксиды.