Металлы и соли – это две группы химических соединений, взаимодействие которых наблюдается во многих естественных и технических процессах. Когда металлы контактируют с солями, возникают различные химические реакции, которые могут привести к образованию твердых соединений, включая соли металлов.
Один из примеров такого взаимодействия – реакция алюминия с хлоридом натрия (NaCl). В результате этой реакции образуется хлорид алюминия (AlCl3). Это соединение широко используется в промышленности, например, в качестве катализатора при производстве пластмасс и резин.
Еще один пример – реакция железа (Fe) с сульфатом меди (CuSO4). В результате образуется сульфат железа (FeSO4) и медь (Cu). Эта реакция позволяет получить медь при переработке медных руд, а также используется в лабораторных исследованиях для отделения меди от других металлов.
Взаимодействие металлов с солями формулы является сложным процессом, который зависит от многих факторов, включая концентрацию соли, температуру, растворимость и электрохимические свойства металла. Изучение этих реакций помогает понять особенности химического взаимодействия между различными веществами и применить их в различных сферах науки и промышленности.
Металлы и соли: общая информация

Металлы и соли – это два различных класса химических соединений, которые обладают разными свойствами и характерными особенностями. Металлы являются химическими элементами, которые обладают хорошей теплопроводностью, электропроводностью, блеском и способностью образовывать положительные ионы. В отличие от металлов, соли представляют собой химические соединения, состоящие из ионов металла и ионов кислоты или основания.
Металлы и соли играют важную роль в различных сферах человеческой жизни. Металлы широко применяются в промышленности, строительстве, электронике и других отраслях. Они используются для производства различных изделий, от автомобилей до бытовой техники. Популярные металлы включают железо, алюминий, медь и золото.
Соли также имеют широкое применение в промышленности и научных исследованиях. Они используются как катализаторы в химических процессах, добавки в пищу, компоненты удобрений и многое другое. Некоторые известные соли включают хлорид натрия (обычную кухонную соль), нитрат аммония (широко используется в сельском хозяйстве) и сульфат меди (применяется в производстве стекла и керамики).
Взаимодействие металлов с солями является одним из важных аспектов химических реакций. Благодаря этому взаимодействию металлы могут образовывать различные соединения с солями, в том числе оксиды, гидроксиды и хлориды. Эти соединения могут быть использованы в различных сферах, включая технологический процесс обработки поверхностей, электролиз и катализаторы.
Особенности реакций металлов с солями
1. Обменные реакции: Металлы могут образовывать соли путем обмена ионами с солями других металлов. Это основной механизм образования солей. Например, при реакции цинка с серной кислотой образуется сульфат цинка и выделяется водородный газ.
2. Образование осадков: Некоторые металлы образуют осадки при реакции с солями. Это происходит, когда ионы металла образуют нерастворимые вещества с ионами соли. Например, при реакции хлорида свинца с хлоридом натрия образуется нерастворимый осадок хлорида свинца.
3. Реакция с образованием газов: Некоторые металлы реагируют с солями, образуя газы. Например, металл алюминий может реагировать с хлоридами, образуя хлорид алюминия и выделяя хлор. Эта реакция имеет применение в промышленности для получения хлора.
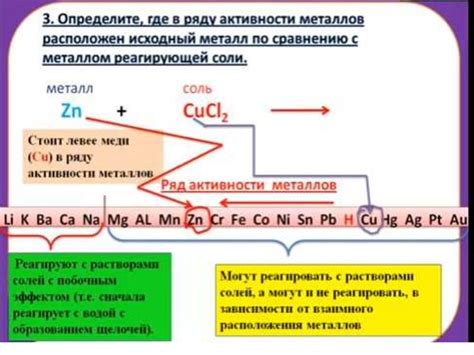
4. Замещение реакции: Некоторые металлы могут замещать другие металлы в солях. Например, цинк может замещать медь в сульфате меди, образуя сульфат цинка и освобождая медь. Это явление называется замещением.
5. Взаимодействие соляных растворов: Металлы могут реагировать не только с твердыми солями, но и с их водными растворами. Например, железо может реагировать с хлоридом железа, образуя хлориды железа различных степеней окисления.
Взаимодействие металлов с солями является основой многих химических реакций и имеет широкие применения в различных отраслях науки и технологий. Понимание особенностей этих реакций позволяет улучшить процессы синтеза, очистки и обработки металлов и их соединений.
Роль солей формулы в промышленных процессах

Соли формулы играют важную роль во многих промышленных процессах. Они используются для различных целей – от синтеза веществ до обработки материалов. В зависимости от своих химических свойств, соли могут быть использованы как реагенты, катализаторы или добавки для достижения определенных результатов.
Один из основных виов их применения – это использование солей в процессе обработки металлов. Соли могут служить для удаления окислов, включений и других примесей, улучшая качество и чистоту металлических изделий. Кроме того, соли могут быть использованы как загустители или смачиватели при нанесении защитных покрытий на металлы, что обеспечивает долговечность и стойкость к коррозии.
Соли также находят применение в процессах гальванизации и электролиза. Например, при гальваническом покрытии металлических изделий с использованием соляной кислоты, хлорида кобальта или никеля, соли обеспечивают равномерное и стойкое покрытие металла. При электролизе соли металлов, например цинка или меди, используются для получения соответствующих металлических осадков с высокой чистотой и поверхностной структурой.
В других областях промышленности соли формулы могут быть использованы для увеличения скорости реакции или улучшения качества продукции. Например, в пищевой промышленности соли формулы применяются как пищевые добавки, улучшающие вкус, текстуру или консистенцию продуктов. В текстильной промышленности соли формулы могут быть использованы для окрашивания и фиксации красителей на ткани, обеспечивая долговечность и стойкость к выцветанию.
Таким образом, соли формулы играют важную роль в различных процессах промышленности. Они являются неотъемлемой частью производства, позволяя достигать желаемых результатов, обеспечивая качество продукции и повышая эффективность процессов.
Вопрос-ответ

Какие металлы взаимодействуют с солями?
С растворимыми солями взаимодействуют многие металлы, например, железо, медь, цинк, свинец, никель и другие. Однако, не все металлы взаимодействуют с солями одинаково, так как у каждого металла свои особенности взаимодействия.
Какие особенности взаимодействия металлов с солями?
Особенности взаимодействия металлов с солями могут быть разными. Например, некоторые металлы могут образовывать нерастворимые осадки с определенными солями, что может приводить к выпадению осадков или изменению окраски раствора. Также, некоторые металлы могут взаимодействовать с солями с образованием характерных комплексных соединений. Кроме того, взаимодействие металлов с солями может приводить к реакциям окислительно-восстановительного типа, при которых меняется степень окисления металла.
