Серная кислота является одним из наиболее распространенных и активных химических веществ. Ее широко применяют в различных отраслях промышленности, в том числе и в металлургии. При разбавлении серной кислоты в воде происходят физические и химические процессы, которые могут существенно влиять на металлические вещества.
Физические процессы связаны с изменением свойств водного раствора серной кислоты. Разбавленная серная кислота обладает довольно высокой кислотностью и способна вызывать разрушение металлических поверхностей. При контакте с металлами происходит растворение и коррозия, что может привести к снижению прочности и долговечности металлических конструкций.
Химические процессы, происходящие при взаимодействии разбавленной серной кислоты с металлами, могут быть различными в зависимости от свойств и химической структуры металлических веществ. Некоторые металлы могут активно реагировать с серной кислотой и образовывать соли и газы, что может привести к образованию пассивной защитной пленки на поверхности металла. Другие металлы могут быть более устойчивы к взаимодействию с серной кислотой и не подвергаться коррозии.
Таким образом, взаимодействие металлических веществ с разбавленной серной кислотой имеет сложный характер и зависит от множества факторов. Знание и понимание этих процессов позволяет разрабатывать эффективные методы защиты металлов от коррозии и повышать их долговечность.
Влияние разбавленной серной кислоты на металлические вещества
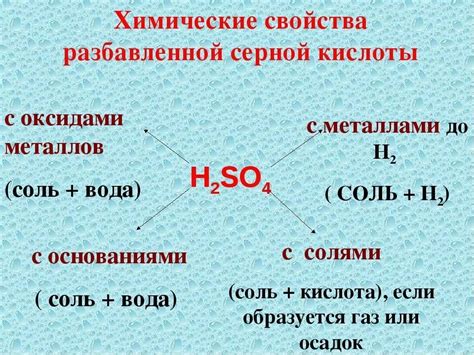
Серная кислота, в химической формуле H2SO4, представляет собой сильную кислоту, которая может оказывать разнообразное влияние на металлические вещества. Когда разбавленная серная кислота взаимодействует с металлами, происходят физические и химические изменения, которые могут быть как полезными, так и вредными.
Одно из наиболее распространенных влияний разбавленной серной кислоты на металлы - это их коррозия. Серная кислота может разрушать поверхность металла, образуя оксиды и соли, которые могут быть дальнейшим источником коррозии. Некоторые металлы, такие как железо и алюминий, подвержены особенно интенсивной коррозии при взаимодействии с разбавленной серной кислотой.
Однако существуют и положительные влияния разбавленной серной кислоты на металлы. Например, она может использоваться для очистки металлической поверхности от оксидных пленок и загрязнений. В этом случае серная кислота действует как агент, разрушающий слой оксида и облегчающий удаление загрязнений с поверхности металла.
Также разбавленная серная кислота может использоваться в процессе электролитического осаждения металла. Под воздействием кислоты происходит растворение металлической пластины (анода), а затем металл осаждается на другом электроде (катоде). Этот процесс используется для получения металлических покрытий или очистки металлов от примесей и загрязнений.
Таким образом, влияние разбавленной серной кислоты на металлические вещества может быть как полезным, так и вредным. Важно правильно дозировать кислоту и контролировать процесс взаимодействия, чтобы достичь желаемого результата и избежать нежелательных последствий.
Физические процессы

Взаимодействие разбавленной серной кислоты с металлическими веществами протекает через ряд физических процессов, включающих диффузию, адсорбцию и образование поверхностных слоев.
Диффузия - это процесс перемещения молекул или ионов разбавленной серной кислоты через металлическую структуру. В результате этого процесса происходит постепенное проникновение кислоты внутрь металла и взаимодействие с его атомами.
Адсорбция - это процесс поглощения молекул разбавленной серной кислоты на поверхности металлического материала. Молекулы кислоты образуют слой на поверхности металла, который может блокировать дальнейшее процесс проникновения кислоты внутрь металлической структуры.
Образование поверхностных слоев - это процесс образования новых соединений на поверхности металла в результате реакции между разбавленной серной кислотой и его атомами. Эти слои могут быть как защитными, предотвращающими дальнейшее проникновение кислоты, так и разрушающими, ведущими к коррозии металла.
Физические процессы, происходящие при взаимодействии разбавленной серной кислоты с металлическими веществами, зависят от конкретных условий воздействия, таких как концентрация кислоты, температура, время взаимодействия и свойства металла. Понимание этих процессов позволяет оптимизировать условия работы с кислотой и предотвращать нежелательные последствия, такие как коррозия металла.
Химические процессы
Разбавленная серная кислота обладает высокой реактивностью и способна вступать в химические реакции с различными металлическими веществами.
Оксидационные реакции являются одним из важных химических процессов, происходящих между разбавленной серной кислотой и металлами. В ходе этих реакций происходит передача электронов от металла к кислороду в серной кислоте. Это приводит к образованию соответствующих солей и выделению водорода.
Важно отметить, что степень реактивности металла может существенно влиять на скорость и интенсивность оксидации. Некоторые металлы, такие как железо и цинк, более активно взаимодействуют с разбавленной серной кислотой, в то время как другие, например, золото и платина, менее активны.
В ходе реакции разбавленной серной кислоты с металлами может также происходить выделение характерного газа - сероводорода. Этот газ образуется в результате окислительной реакции серной кислоты с металлом и имеет характерный запах гнилых яиц. Образование сероводорода является одним из показателей химической реакции между разбавленной серной кислотой и металлами.
Эксперименты и результаты

В рамках исследования были проведены серия экспериментов, направленных на изучение влияния разбавленной серной кислоты на различные металлические вещества. Для этого были выбраны образцы алюминия, железа и меди.
Первый этап эксперимента заключался в погружении металлических образцов в разбавленную серную кислоту различной концентрации. Образцы были оставлены в реакционной среде на протяжении определенного времени.
После завершения каждого эксперимента были проанализированы изменения физических и химических свойств металлических образцов. Было обнаружено, что разбавленная серная кислота оказывает различное воздействие на каждый металл.
Алюминий, находящийся в контакте с разбавленной серной кислотой, образует пленку оксида алюминия, которая защищает его от дальнейшего взаимодействия с кислотой. Наблюдается незначительное образование пузырей газа вокруг образца.
Железо при взаимодействии с разбавленной серной кислотой проявляет активность и начинает активно реагировать. Образуется большое количество водорода, сопровождающееся проникновением пузырьков газа в среду. Поверхность железного образца окисляется и сильно коррозирует.
Медь взаимодействует с разбавленной серной кислотой более нейтрально. Наблюдаются лишь незначительные окислительные реакции и образование купрата меди. Медный образец сохраняет свою структуру и не подвергается значительной коррозии.
Советы по безопасности

Работа с разбавленной серной кислотой требует строгого соблюдения безопасности и правил пользования. Вот несколько советов, которые помогут вам минимизировать риски и обезопасить себя и окружающих:
- Пользуйтесь защитным снаряжением. Всегда надевайте защитные очки, резиновые перчатки, халат и фартук. Это поможет предотвратить возможные ожоги, попадание кислоты на кожу и в глаза.
- Проводите работы в хорошо проветриваемом помещении. Разбавленная серная кислота может испаряться, выделяя ядовитые пары. Поэтому не забывайте работать в хорошо проветриваемой зоне или использовать вытяжные вентиляционные системы.
- Будьте внимательны при разбавлении кислоты. При разбавлении серной кислоты всегда добавляйте кислоту в воду, а не наоборот. Это поможет избежать внезапного резкого выделения тепла и брызг кислоты.
- Храните кислоту в безопасном месте. После использования серную кислоту необходимо хранить во взрыво- и пожаробезопасном месте, закрыв тару крышкой с герметичным уплотнением.
- Также необходимо учесть реакцию металлических веществ с серной кислотой. Некоторые металлы, такие как алюминий или цинк, могут реагировать с кислотой, выделяя взрывоопасный водород. Поэтому перед проведением экспериментов с серной кислотой, изучите свойства выбранного металла и примите все необходимые меры предосторожности.
И помните, что безопасность при работе с разбавленной серной кислотой должна быть вашим главным приоритетом. Следуйте указанным советам и соблюдайте все необходимые меры предосторожности, чтобы избежать возможных опасностей и несчастных случаев.
Вопрос-ответ

Какой эффект оказывает разбавленная серная кислота на металлические вещества?
Разбавленная серная кислота, взаимодействуя с металлическими веществами, может вызывать различные эффекты, включая окисление, растворение или образование защитной пленки.
Какие физические процессы происходят при взаимодействии разбавленной серной кислоты с металлами?
Физические процессы, происходящие при взаимодействии разбавленной серной кислоты с металлами, могут включать образование пузырьков, выделение тепла и изменение цвета раствора.
Каковы химические процессы, происходящие при взаимодействии разбавленной серной кислоты с металлами?
Химические процессы, происходящие при взаимодействии разбавленной серной кислоты с металлами, включают образование солей, выделение газов (например, водорода) и реакции окисления металлов.
В каких случаях разбавленная серная кислота вызывает растворение металлических веществ?
Разбавленная серная кислота вызывает растворение металлических веществ в случае, когда они реагируют с кислотой и образуют растворимые соли. Например, цинк растворяется, образуя сульфат цинка и выделяя водородный газ.
Может ли разбавленная серная кислота использоваться для создания защитной пленки на металлических поверхностях?
Да, разбавленная серная кислота может использоваться для создания защитной пленки на металлических поверхностях. При взаимодействии с металлом, кислота может образовывать плотный оксидный слой, который предотвращает окисление металла и защищает его от коррозии.






