Реакция металлов с концентрированной серной кислотой является одной из наиболее распространенных химических реакций. При этом образуются соли серы, которые имеют широкое применение в различных областях: от производства удобрений и пищевой промышленности до производства косметических и фармацевтических продуктов. Кроме того, реакция с серной кислотой может быть использована для получения водорода.
Первичной стадией реакции металла с серной кислотой является образование сульфата металла и выделение газа сероводорода:
Металл + серная кислота → соль серы + сероводород
Реакционная способность металлов с серной кислотой зависит от их активности, которая связана с их электрохимической активностью и расположением в ряду активности. Наиболее активные металлы, такие как натрий и калий, реагируют с серной кислотой даже при комнатной температуре, образуя соли серны и выделяя большое количество сероводорода. Более инертные металлы, такие как железо или медь, требуют нагревания для начала реакции.
Реакция металлов с серной кислотой является экзотермической и сопровождается выделением тепла. Также важно отметить, что при реакции с концентрированной серной кислотой температура может повышаться настолько, что может запросто привести к ожогам или аварийной ситуации. Поэтому необходимо соблюдать осторожность и работать с серной кислотой только в специально оборудованном помещении с соблюдением правил безопасности.
Реакция металлов с серной кислотой

Серная кислота, или H2SO4, является одной из самых распространенных кислот, используемых в химических реакциях. Она сильный окислитель и реагирует с различными веществами, включая металлы.
Реакция металлов с серной кислотой основана на окислении металла и одновременном восстановлении серной кислоты. В результате образуется соль и вода, а также выделяется сернистый газ.
Реакция металлов с серной кислотой может происходить следующим образом:
Металл активнее водорода. В этом случае, металл замещает водород из серной кислоты, образуя соль и выделяя газ. Например, цинк реагирует с серной кислотой по следующему уравнению: Zn + H2SO4 → ZnSO4 + H2.
Металл менее активен водорода. В этом случае, металл не способен замещать водород и реакция не происходит. Например, медь не реагирует с серной кислотой.
Металл, имеющий положительный окислительный потенциал, может реагировать с серной кислотой, но реакция будет протекать очень медленно и требовать нагревания. Например, железо может реагировать с серной кислотой, но для этого необходимо нагревание.
Реакция металлов с серной кислотой является примером реакции некоторых металлов с кислотами. Эта реакция имеет широкое применение в химической промышленности и лабораториях для получения солей и воды, а также в процессах очистки металлов от посторонних примесей и оксидной пленки.
Роль металлов в химии

Металлы играют важную роль в химии и являются одними из основных элементов периодической таблицы. Они обладают большим числом уникальных свойств и широко применяются в различных сферах нашей жизни.
Металлы являются хорошими проводниками электричества и тепла. Это связано с их особенностями строения атомов и способностью свободно перемещаться по кристаллической решетке. Благодаря этому свойству металлы используются в производстве проводов, электрических контактов и теплоотводов.
Кроме того, металлы обладают высокой прочностью и устойчивостью к коррозии. Эти свойства позволяют использовать металлы для создания строительных конструкций, автомобилей, судов и других технических изделий. Один из ярких примеров - сталь, которая широко применяется в инженерном строительстве и машиностроении.
Металлы также способны образовывать различные соединения с другими элементами. Они могут образовывать ионы положительного заряда, которые играют важную роль в химических реакциях. Это свойство позволяет использовать металлы в процессе электролиза, получения различных сплавов и создания катализаторов.
Особое место среди металлов занимают переходные металлы. Они обладают сложной внутренней структурой и способностью образовывать соединения разной степени окисления. Именно благодаря этим свойствам переходные металлы играют важную роль в биохимии и каталитических процессах. Например, металлы, такие как железо, цинк и медь, являются необходимыми микроэлементами для живых организмов.
В заключении, металлы играют важную роль в химии и имеют множество применений благодаря своим уникальным свойствам. Они являются проводниками электричества и тепла, обладают высокой прочностью и устойчивостью к коррозии, и способны образовывать различные соединения. Переходные металлы дополнительно играют важную роль в биохимии и каталитических процессах. Все эти свойства делают металлы незаменимыми материалами в различных отраслях промышленности и науки.
Свойства концентрированной серной кислоты

Концентрированная серная кислота, также известная как азотистая серная кислота или холодная серная кислота, обладает рядом характерных свойств.
Во-первых, концентрированная серная кислота является сильным окислителем. Она способна окислять различные вещества, образуя при этом продукты реакции. Например, металлы, такие как железо и цинк, реагируют с концентрированной серной кислотой, образуя соответствующие сульфаты и выделяя водород. Эта реакция происходит при высокой экзотермической реакции, сопровождаемой выделением тепла и парами серы.
Во-вторых, концентрированная серная кислота характеризуется высокой кислотностью. Она обладает pH значением меньше 1, что свидетельствует о ее сильной кислотности. При контакте с кожей или слизистыми оболочками она может вызвать ожоги и серьезные повреждения. Поэтому при работе с данной кислотой необходимо соблюдать особые меры предосторожности.
В-третьих, концентрированная серная кислота обладает специфическим запахом, который можно ощутить при ее приближении. Она является безцветной жидкостью, но под действием ряда веществ может изменять свой цвет или образовывать характерные цветные соединения.
В-четвертых, концентрированная серная кислота хорошо растворяется в воде, образуя гидратированные ионы сероводорода, которые придают кислотному раствору характерный запах и свойство разъедать многие органические и неорганические вещества.
В общем, концентрированная серная кислота обладает рядом уникальных свойств, которые делают ее важным химическим веществом в промышленности, лабораторных исследованиях и других сферах деятельности.
Взаимодействие металлов с серной кислотой

Серная кислота (H2SO4) является одной из самых сильных неокислительных кислот. Она обладает высокой кислотностью и образует практически полное количество ионов в растворе. Из-за своей агрессивности она реагирует с многими металлами, образуя соответствующие соли и выделяя водород.
Реакция металлов с серной кислотой протекает с образованием солей серной кислоты и выделением водорода. При этом металл ионизируется, образуя положительно заряженные ионы, которые образуют соль с анионами серной кислоты.
Некоторые металлы, такие как цинк (Zn), железо (Fe), алюминий (Al) и магний (Mg), реагируют со сгущенной серной кислотой, причем реакция происходит взрывоопасно. При этом образуется соль соответствующего металла и серная кислота превращается в бесводную серную кислоту (SO3), которая может образовывать пары и осаждаться в виде белого дыма.
Реакция алюминия с серной кислотой выглядит следующим образом:
- 2 Al + 3 H2SO4 = Al2(SO4)3 + 3 H2↑
| Металл | Реакция |
|---|---|
| Цинк (Zn) | Zn + H2SO4 = ZnSO4 + H2↑ |
| Железо (Fe) | Fe + H2SO4 = FeSO4 + H2↑ |
| Магний (Mg) | Mg + H2SO4 = MgSO4 + H2↑ |
При взаимодействии более реактивных металлов, таких как натрий (Na) или калий (K), с серной кислотой происходит еще более интенсивное выделение водорода, образование соли и образование бесводной серной кислоты:
- 2 Na + H2SO4 = Na2SO4 + H2↑
- 2 K + H2SO4 = K2SO4 + H2↑
Таким образом, реакция металлов с серной кислотой протекает с образованием солей и выделением водорода. Выделение водорода может быть сопровождено выбросом небезопасного белого дыма. При проведении таких реакций необходимо соблюдать меры предосторожности.
Продукты реакции металлов с серной кислотой
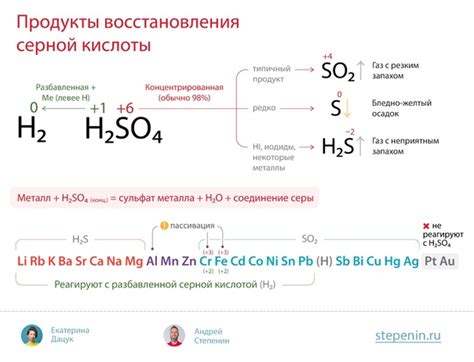
Металлы реагируют с концентрированной серной кислотой и образуют различные продукты.
Железо, например, образует сернокислое железо(II) и выделяется газовый водородH2.
Цинк также реагирует с серной кислотой, образуя сернокислый цинк и выделяющийся газовый водород.
Медь, в свою очередь, не реагирует с концентрированной серной кислотой в холодном состоянии, но при нагревании образует сернокислую медь и выделяет газообразный двуокись серы.
Продукты реакции получаются в виде соединений, растворяющихся в серной кислоте, или в виде отдельных газовых веществ.
Практическое применение реакции металлов с серной кислотой
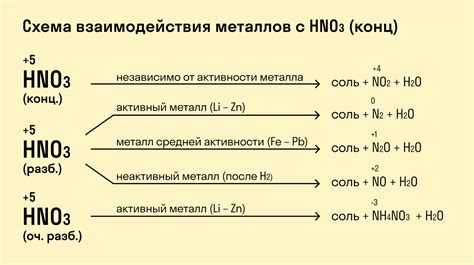
Реакция металлов с концентрированной серной кислотой имеет широкое практическое применение в различных областях. Одним из важных применений этой реакции является получение сульфатов металлов, которые находят применение в промышленности, сельском хозяйстве и медицине.
Сульфаты различных металлов используются в качестве удобрений для повышения урожайности почвы. Калийные сульфаты обеспечивают растения калием, необходимым для их нормального роста и развития. Медные сульфаты используются в сельском хозяйстве в качестве фунгицидов для борьбы с грибковыми заболеваниями растений.
Кроме того, сульфаты металлов находят применение в промышленности. Алюминиевый сульфат используется в производстве бумаги и текстильных материалов, альбуминовый сульфат – в фотографии, железный сульфат – в производстве красок и лаков.
Еще одним практическим применением реакции металлов с серной кислотой является получение водорода. Этот газ широко используется в промышленности, например, в процессе производства аммиака и метанола, а также в качестве топлива для водородных автомобилей и электростанций.
Таким образом, реакция металлов с концентрированной серной кислотой имеет важное практическое значение и находит широкое применение в различных отраслях, начиная от сельского хозяйства и промышленности, и заканчивая медициной и энергетикой.
Вопрос-ответ

Какие металлы реагируют с концентрированной серной кислотой?
С концентрированной серной кислотой реагируют различные металлы, такие как железо, цинк, алюминий, свинец, медь и др. Реакция зависит от химической активности металла и может варьироваться по скорости и степени интенсивности.
Какую реакцию металлы образуют с концентрированной серной кислотой?
Реакция металлов с концентрированной серной кислотой приводит к образованию солей и выделению водорода. Соли, образуемые при этой реакции, называются сульфатами. Водород выделяется в виде газа.
Почему металлы реагируют с концентрированной серной кислотой?
Реакция металлов с концентрированной серной кислотой основана на способности серной кислоты отдавать протоны и образовывать соли. Металлы, в свою очередь, способны принять эти протоны и образовать соли, которые называются сульфатами. Эта реакция также связана с различием в электрохимических потенциалах металлов и их способности образовывать стабильные соединения с серной кислотой.
Какие особенности имеет реакция металлов с концентрированной серной кислотой?
Реакция металлов с концентрированной серной кислотой имеет несколько особенностей. Во-первых, она протекает достаточно быстро и интенсивно, с выделением газа водорода. Во-вторых, различные металлы образуют разные соли, поэтому продукты реакции могут отличаться в зависимости от используемого металла. И в-третьих, реакция со временем может привести к коррозии металла и разрушению его структуры.
