Металлы и кислоты – важные компоненты химического мира, изучаемые в химии. Известно множество различных металлов, таких как железо, алюминий, медь и другие, и каждый из них может реагировать с различными кислотами.
Взаимодействие металлов с кислотами является типичным примером химической реакции. Когда металлы контактируют с кислотами, происходит их окисление, а в результате образуется соль и выделяется водород. Важным фактором в этой реакции является активность металла – чем активнее металл, тем сильнее будет реакция.
Примером такой реакции может служить взаимодействие железа с соляной кислотой. В результате этой реакции образуется соль – хлорид железа и выделяется водородный газ. Что интересно, если взять другой металл, например алюминий, и провести ту же реакцию с соляной кислотой, то произойдет аналогичная реакция, но с образованием другой соли – алюминия хлорида.
Взаимодействие металлов с кислотами служит важным аспектом для понимания принципов химических реакций. Это также может объяснить, почему некоторые металлы коррозируют при контакте с кислотными средами. Благодаря этим знаниям ученики смогут шире взглянуть на мир химии и осознать важность взаимодействия металлов с кислотами.
Металлы и их химические свойства взаимодействия с кислотами

Металлы - это элементы химической таблицы, обладающие определенными химическими и физическими свойствами. Одним из основных химических свойств металлов является их взаимодействие с кислотами.
Взаимодействие металлов с кислотами происходит посредством реакции между ионами металла и ионами водорода, образующимися при диссоциации кислоты. Эта реакция может протекать с выделением газов, тепла и образованием соли.
Металлы можно разделить на активные и неподвижные их взаимодействие с кислотами. Активные металлы, например, натрий (Na), калий (K) и цинк (Zn), обладают способностью активно реагировать с кислотами. Неподвижные металлы, такие как золото (Au) и платина (Pt), не вступают в реакцию с кислотами или реакция происходит слишком медленно.
В результате взаимодействия металлов с кислотами образуются соли, которые могут быть различных типов. Например, при реакции натрия с соляной кислотой образуется хлорид натрия (NaCl), при реакции меди с серной кислотой образуется сульфат меди (CuSO4).
Реакция металлов с кислотами может иметь как практическое, так и теоретическое значение. Практическое значение состоит в использовании этих реакций в различных технологических процессах. Теоретическое значение заключается в исследовании химических свойств металлов и кислот, а также изучении реакций между ними.
Свойства металлов в реакциях с кислотами
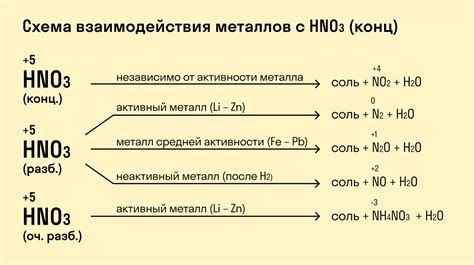
Металлы – это элементы, характеризующиеся своеобразными свойствами во время взаимодействия с кислотами. При контакте с кислотой происходят химические реакции, которые могут стать причиной растворения, разложения или образования новых веществ.
Металлы могут реагировать с различными кислотами, такими как серная, соляная, уксусная и др. Реакции с кислотами позволяют металлам проявить свою активность и химическую реакционность. Каждый металл может проявлять свои особенности при вступлении в реакцию с кислотой.
Большинство металлов способны образовывать соли при реакции с кислотами. Это связано с образованием ионов металла и ионов кислоты. Важно отметить, что разные металлы могут образовывать соли различной степени растворимости в воде. Например, некоторые металлы образуют соли, полностью растворимые в воде, тогда как другие металлы образуют соли, которые могут быть малорастворимыми или вообще нерастворимыми.
Кроме образования солей, в реакциях металлов с кислотами может происходить выделение газов. Например, при реакции цинка с соляной кислотой образуется газ водород. Реакция также сопровождается характерными признаками: шипением, выделением тепла, изменением окраски раствора. Эти признаки связаны с характером реакций и способом поглощения или отдачи энергии в процессе взаимодействия металла с кислотой.
Примеры реакций металлов с кислотами
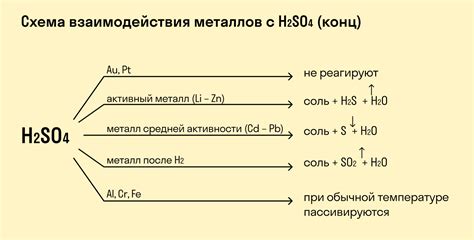
Общая химическая реакция между металлами и кислотами приводит к образованию солей и выделению водорода. Например, следующие металлы активно взаимодействуют с кислотами:
- Цинк (Zn). При взаимодействии с соляной кислотой образуется хлорид цинка (ZnCl2) и выделяется водород.
- Железо (Fe). При реакции с серной кислотой образуется сульфат железа (FeSO4) и выделяется водород.
- Магний (Mg). Реакция металла с соляной кислотой приводит к образованию хлорида магния (MgCl2) и выделению водорода.
- Алюминий (Al). При взаимодействии с соляной кислотой образуется хлорид алюминия (AlCl3) и выделяется водород.
Эти реакции являются примерами химических превращений металлов при взаимодействии с кислотами. Водород, выделяющийся при реакциях, можно обнаружить с помощью горящей спички: он зажигается и издает звук. Образование солей и выделение водорода при реакциях металлов с кислотами широко используется в различных промышленных и лабораторных процессах.
Вопрос-ответ

Какие металлы взаимодействуют с кислотами?
Взаимодействуют с кислотами различные металлы, такие как цинк, железо, алюминий и другие.
Что происходит при взаимодействии металлов с кислотами?
При взаимодействии металлов с кислотами происходят реакции, в результате которых образуется соль и выделяется водород.
Каким образом металлы реагируют с кислотами?
Металлы реагируют с кислотами, отдавая электроны и образуя положительные ионы металла. При этом водородные ионы из кислоты превращаются в молекулы водорода.
Можно ли предсказать, какой металл реагирует с какой кислотой?
Да, взаимодействие металлов с кислотами можно предсказать на основе реакционной активности металла и силы кислоты. Например, активные металлы, такие как натрий или калий, реагируют с более слабыми кислотами, а менее активные металлы, такие как ртуть или серебро, реагируют с более сильными кислотами.
