Одним из важных разделов курса химии в школе является изучение взаимодействия металлов с окисляющими кислотами. Эта тема находится в программе ЕГЭ по химии и требует от учеников хорошего понимания реакций и закономерностей, происходящих при таком взаимодействии.
В ходе обучения ученики узнают, что металлы могут проявлять разную степень активности при взаимодействии с окисляющими кислотами. Некоторые металлы, такие как железо и алюминий, активно реагируют с окислительными средами, а другие металлы, например золото и платина, практически не взаимодействуют с кислотами.
Это взаимодействие металлов с окисляющими кислотами связано с тем, что окислительные среды активно вступают в реакцию с электроотрицательными металлами. При этом происходит окисление металла, а окислительное вещество само восстанавливается. Ученикам необходимо хорошо изучить соответствующие химические уравнения и уметь анализировать процессы, происходящие в ходе взаимодействия металлов с окисляющими кислотами.
Влияние окисляющих кислот на металлы: ключевые аспекты
Взаимодействие металлов с окисляющими кислотами – это важный процесс, в результате которого происходят химические реакции, влияющие на свойства и структуру металлов.
Первым и наиболее значимым аспектом является способность окисляющих кислот образовывать активные ионы, которые возникают в процессе диссоциации кислоты. Данные ионы могут образовывать соединения с металлами, вызывая изменение их состава и свойств.
Вторым аспектом является протекание реакций окисления-восстановления. Окисление – это процесс передачи электронов от металла к кислоте, а восстановление – обратная реакция, при которой электроны переходят от кислоты к металлу. Такие реакции приводят к изменению внешнего вида металлов и образованию новых соединений.
Третий аспект – возможность образования защитных покрытий на поверхности металлов. Некоторые окисляющие кислоты способны создавать пассивные оксидные пленки, которые служат защитой от дальнейшего взаимодействия с кислотой. Такие покрытия улучшают коррозионную стойкость металлов и позволяют им сохранять свою работоспособность на протяжении длительного времени.
Итак, взаимодействие металлов с окисляющими кислотами – это сложный процесс, включающий несколько ключевых аспектов, таких как образование активных ионов, протекание реакций окисления-восстановления и образование защитных пленок. Изучение этих аспектов позволяет понять, как происходят реакции между металлами и кислотами и как это влияет на их свойства и структуру.
Химические реакции металлов с окисляющими кислотами:

Металлы, как химически активные элементы, способны взаимодействовать с различными веществами, в том числе с окисляющими кислотами. Окисляющие кислоты являются сильными окислителями и способны окислять другие вещества, в том числе и металлы.
Реакция металла с окисляющей кислотой протекает с образованием соли и выделением газа. Примером такой реакции может служить взаимодействие железа с серной кислотой. При этом образуется соль - сульфат железа(II) и выделяется водород. Реакция может быть представлена следующим образом:
- Fe + H2SO4 → FeSO4 + H2
Некоторые металлы, такие как цинк и алюминий, проявляют высокую реакционную способность с окисляющими кислотами. Например, при взаимодействии цинка с серной кислотой образуется сульфат цинка и выделяется водород:
- Zn + H2SO4 → ZnSO4 + H2
Однако не все металлы способны реагировать с окисляющими кислотами. Например, такие металлы, как золото и платина, не проявляют реакционной способности при взаимодействии с серной кислотой.
Химические реакции металлов с окисляющими кислотами являются важным объектом изучения в химии и на них основано множество производственных процессов, например, производство сульфата цинка, используемого в процессах гальваностегии.
Применение взаимодействия металлов с окисляющими кислотами в промышленности:

Взаимодействие металлов с окисляющими кислотами находит широкое применение в промышленности. Одним из основных примеров такого применения является гальваническое покрытие. При этом процессе металлический предмет погружается в раствор окисляющей кислоты, что позволяет создать на его поверхности защитный или декоративный слой другого металла. Таким образом, происходит защита от коррозии и повышение эстетических свойств изделий.
Другой пример применения взаимодействия металлов с окисляющими кислотами – это процесс гальванического осаждения. При этом процессе металлы осаждается на поверхность предмета под воздействием электричества, что позволяет достичь определенных свойств поверхности, например, улучшение проводимости, укрепление и повышение износостойкости материала.
Кроме того, взаимодействие металлов с окисляющими кислотами применяется при очистке и обработке поверхностей. Окисляющие кислоты способны растворять окисные пленки и загрязнения с металлической поверхности, что позволяет удалить коррозию и придать изделиям первоначальный блеск и чистоту. Такой процесс широко применяется в промышленности при изготовлении изделий из нержавеющей стали, алюминия и других металлов, которые требуют высокой степени очистки и обработки перед последующей обработкой или эксплуатацией.
Таким образом, взаимодействие металлов с окисляющими кислотами нашло применение в различных сферах промышленности, от гальванического покрытия до очистки и обработки поверхностей. Этот процесс позволяет не только защитить металл от коррозии, но и достичь определенных свойств поверхности, внося важный вклад в производство качественных и долговечных изделий.
Взаимодействие металлов с окисляющими кислотами в природных условиях:

Взаимодействие металлов с окисляющими кислотами играет важную роль в природных условиях. Окисляющие кислоты, такие как азотная кислота и серная кислота, встречаются в природе в виде дождевых осадков или веществ, выделяющихся в атмосферу промышленными предприятиями.
При взаимодействии металлов с окисляющими кислотами происходит окисление металла. Окислительно-восстановительные реакции, происходящие в результате этого процесса, приводят к образованию соединений, которые могут влиять на окружающую среду и биоценоз. Например, в результате взаимодействия цинка с серной кислотой образуется цинковый сульфат, который может быть растворен в воде дождя и попасть в почву или водные объекты.
В процессе взаимодействия металлов с окисляющими кислотами могут образовываться также токсичные газы и вещества, такие как оксиды металлов. Например, при взаимодействии железа с азотной кислотой образуются оксид азота и нитрат железа. Оксид азота является одним из основных источников атмосферного загрязнения и может оказывать вредное влияние на человека и окружающую среду.
Взаимодействие металлов с окисляющими кислотами в природных условиях имеет большое значение для понимания экологической ситуации в регионах, где промышленность активно развита. Изучение данных реакций позволяет предсказать возможные последствия и разработать меры для снижения негативного воздействия на окружающую среду.
Классификация металлов в зависимости от их реакционной способности с окисляющими кислотами:
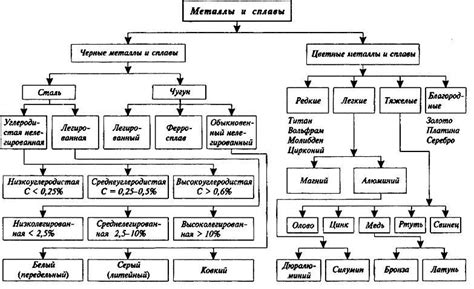
Металлы различаются по своей реакционной способности с окисляющими кислотами. В зависимости от этой способности металлы можно классифицировать на активные, среднеактивные и пассивные.
Активные металлы вступают в реакцию с окисляющими кислотами с выделением водорода. Это, например, металлы первой группы периодической системы и алюминий. Реакция активных металлов с окисляющими кислотами сопровождается образованием солей металла и выделением пузырьков водорода.
Среднеактивные металлы проявляют меньшую реакционную способность по сравнению с активными металлами. К таким металлам относятся, например, цинк, железо и медь. Реакция среднеактивных металлов с окисляющими кислотами протекает медленнее, но все же с выделением водорода.
Пассивные металлы, такие как золото, серебро и платина, практически не проявляют реакцию с окисляющими кислотами. Реакция с пассивными металлами протекает очень медленно или вообще не происходит.
Классификация металлов в зависимости от их реакционной способности с окисляющими кислотами позволяет понять, каким образом взаимодействуют металлы с окисляющими кислотами и предсказать результат такой реакции.
Применение знаний о взаимодействии металлов с окисляющими кислотами в сдаче ЕГЭ по химии:

Успешное сдача ЕГЭ по химии требует хорошего понимания процессов взаимодействия металлов с окисляющими кислотами. Эти знания могут быть применены в разных разделах экзамена, например, при решении задач на расчет реакции между металлом и кислотой, определение степени окисления металла, анализ химических реакций и понимание их механизма.
С помощью знаний о взаимодействии металлов с окисляющими кислотами можно определить, какой металл будет наиболее реакционно активен и как будет протекать процесс окисления. Например, металлы, которые находятся выше в ряду напряжения, будут вытеснять металлы ниже в ряду из их соединений с кислотами, что можно использовать для расчета полезности металла в различных процессах, например, в оценке металлов для использования в качестве анодов.
Важными практическими применениями знаний о взаимодействии металлов с окисляющими кислотами являются различные процессы гальванического осаждения металлов, где окислительные кислоты используются для образования ионов металла, которые затем осаждаются на поверхности других металлов. Эти процессы широко применяются в различных отраслях промышленности, таких как производство электроники, автомобильной промышленности и других.
Вопрос-ответ

Какие металлы могут вступать в реакцию с окисляющими кислотами?
В реакцию с окисляющими кислотами могут вступать активные металлы, такие как натрий, калий, магний, алюминий и цинк.
Что происходит при взаимодействии металлов с окисляющими кислотами?
При взаимодействии металлов с окисляющими кислотами происходит окисление металла и одновременное восстановление кислоты. На выходе получается соль и выделяется водородный газ.
Какие окисляющие кислоты могут взаимодействовать с металлами?
Окисляющие кислоты, такие как соляная кислота (HCl), серная кислота (H2SO4) и азотная кислота (HNO3), могут взаимодействовать с активными металлами.
Что происходит, когда натрий взаимодействует с соляной кислотой?
При взаимодействии натрия с соляной кислотой происходит реакция, в результате которой образуется соль - хлорид натрия (NaCl) и выделяется водородный газ (H2).
Какие газы выделяются при взаимодействии металлов с окисляющими кислотами?
При взаимодействии металлов с окисляющими кислотами выделяется водородный газ (H2).
