Взаимодействие металлов с кислородом является одной из наиболее известных и изученных в химии реакций. Такая реакция обычно называется окислением металла, поскольку кислород переходит отрицательные степени окисления, а металл при этом окисляется.
Кислород – один из самых распространенных элементов на Земле, а металлы тоже являются широко распространенными материалами. Поэтому образование оксидов металлов – важный и всеобъемлющий процесс в природе. Кислород может вступать во взаимодействие со многими металлами, включая алюминий, железо, магний, свинец, цинк и др.
Окисление металла происходит в результате передачи электронов от металла к кислороду, что приводит к образованию оксида металла. Реакция происходит обычно с выделением энергии и может сопровождаться плавлением или горением металла. Некоторые металлы, такие как железо, могут реагировать с кислородом под воздействием нагревания, в то время как другие металлы, например, цинк, требуют наличия катализатора.
Окисление металла с кислородом может привести к образованию различных оксидов, которые обладают различными свойствами и применениями. Так, окись алюминия применяется в производстве керамики, а окись железа – в изготовлении магнитопроводящих материалов. Изучение типов реакций металлов с кислородом имеет важное значение для развития различных отраслей промышленности и науки.
Физические свойства металлов
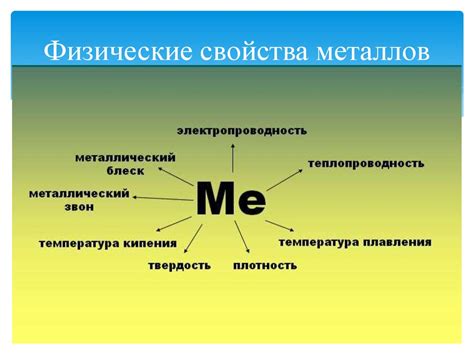
Металлы обладают рядом особых физических свойств, которые отличают их от других веществ. Одним из ключевых свойств металлов является электрическая проводимость. Металлы обладают свободными электронами, которые способны перемещаться внутри материала под внешним электрическим полем. Благодаря этому металлы обладают способностью проводить электрический ток.
Еще одним важным свойством металлов является теплопроводность. Металлы обладают способностью эффективно передавать тепло. Это связано с высокой подвижностью электронов внутри металлической структуры, что позволяет энергии передаваться быстро и без значительных потерь.
Металлы также обладают высокой пластичностью и формовальностью. Они могут быть легко обработаны, изготовлены в различные формы и изделия. Это связано с наличием свободных электронов, которые способствуют перемещению атомов и молекул в материале, позволяя ему принимать новую форму без разрушения.
Помимо этого, металлы обладают высокой плотностью и тяжестью. Они устойчивы к нагрузкам и имеют высокую прочность. Это позволяет использовать металлы в производстве конструкций, автомобилей, самолетов и других технических изделий.
Также характерными свойствами металлов являются блеск и отражательная способность. Металлы имеют хорошую способность отражать свет и создавать блестящую поверхность. Это связано с наличием свободных электронов, которые способствуют рассеиванию и отражению световых волн.
И наконец, металлы имеют высокую точку плавления и кипения. Они обычно превращаются из твердого состояния в жидкое при достаточно высоких температурах. Это связано с особенностями устройства металлической структуры и взаимодействием атомов.
Реакция металлов с кислородом

Металлы – это элементы, характеризующиеся высокой электропроводностью и способностью образовывать положительные ионы (катионы) в процессе химических реакций.
Взаимодействие металлов с кислородом является одним из наиболее распространенных и важных процессов в химии. При этом образуются оксиды металлов. Кислород обычно выступает в роли окислителя, принимая электроны от металла.
Реакция металлов с кислородом может происходить при нагревании металла на воздухе или взаимодействии с кислородом в воде или кислородных соединениях. Например, при горении металлов в кислороде образуются оксиды металлов.
Оксиды металлов имеют различные свойства и могут использоваться в различных областях. Некоторые оксиды металлов обладают кислотными свойствами и могут реагировать с основаниями, образуя соли. Другие оксиды металлов являются основаниями и способны реагировать с кислотами, образуя соли.
Реакция металлов с кислородом является одним из основных способов получения оксидов металлов. Она используется как в лабораторных условиях, так и в промышленности для получения различных оксидов металлов, которые имеют широкий спектр применения.
Окисление металлов

Окисление металлов – это процесс взаимодействия металла с кислородом в результате которого образуется оксид металла. Кислород, присутствующий в воздухе или воде, может вступать в реакцию с различными металлами, приводя к их окислению.
Одним из наиболее известных примеров окисления металлов является ржавчина железа. При взаимодействии железа с влажным воздухом или водой, происходит окисление железа, что приводит к образованию гидроксида железа и оксида железа. Это приводит к изменению свойств и внешнего вида металла – железо покрывается коркой ржавчины.
Взаимодействие металлов с кислородом может происходить также при нагревании. Например, при нагревании алюминия на воздухе образуется тонкая пленка оксида алюминия, которая предотвращает дальнейшее окисление металла.
Окисление металлов может происходить не только с кислородом, но и с другими окислителями, например, с кислотами. В результате этого процесса металл переходит в более высокую окислительную степень и образуется соответствующая соль. К примеру, при взаимодействии цинка с серной кислотой образуется сульфат цинка и выделяется водород.
Коррозия металлов

Коррозия металлов является процессом разрушения металлических поверхностей под воздействием окружающей среды, особенно кислорода. Коррозия может приводить к потере прочности и функциональности металлических изделий и конструкций.
Основной способ защиты от коррозии – нанесение защитных покрытий на металлические поверхности. Наиболее эффективное и популярное из них – покрытие металла слоем неметаллического материала, такого как краска или пластик. Такой слой предотвращает проникновение кислорода и влаги в металл, защищая его от коррозии.
Другим способом защиты является использование специальных сплавов, которые обладают повышенной устойчивостью к коррозии. Например, нержавеющая сталь содержит хром, который образует на поверхности металла защитную пленку, предотвращающую коррозию.
Кроме того, важным фактором в предотвращении коррозии является контроль внешних условий. Это может включать регулярное очищение поверхностей от загрязнений, правильное хранение и транспортировку металлических изделий, контроль влажности и температуры в окружающей среде.
В целом, коррозия металлов – это сложный и многогранный процесс, требующий постоянного внимания и заботы. Защита металлических конструкций от коррозии является не только важной экономической задачей, но и гарантом безопасности и долговечности сооружений.
Защитные меры от коррозии

Коррозия – это процесс разрушения материала, вызванный взаимодействием с окружающей средой, такой как вода, влажность, кислород и другие химические вещества. Коррозия металла может привести к его утрате или функциональным нарушениям, что может иметь серьезные последствия для конструкций или оборудования.
Для предотвращения коррозии и увеличения срока службы металлических изделий используются различные защитные меры. Одним из основных способов защиты от коррозии является нанесение защитных покрытий на металлическую поверхность. Такие покрытия могут быть органическими или неорганическими и предотвращают контакт металла с окружающей средой.
Очень важным этапом при нанесении защитных покрытий является подготовка металлической поверхности. Поверхность должна быть очищена от ржавчины, жира, старых покрытий и других загрязнений. Для этого могут использоваться различные методы, такие как механическая обработка, химическая обработка или их комбинация.
Другой возможностью защиты металлов от коррозии является применение антикоррозионных пигментов. Это специальные вещества, которые добавляются в состав красок и лаков и образуют на поверхности металла защитный слой, предотвращающий коррозию.
Кроме того, для защиты металлов от коррозии могут использоваться специальные покрытия, такие как гальванические покрытия или покрытия методом нанесения порошка. Эти методы защиты позволяют создать на поверхности металла стойкий к коррозии слой, который способен выдерживать агрессивные воздействия.
В конечном итоге, выбор защитной меры зависит от характеристик металла, условий эксплуатации и требований к защите от коррозии. Эффективность и долговечность защиты также важны при выборе определенного метода защиты.
Важные примеры реакций металлов с кислородом
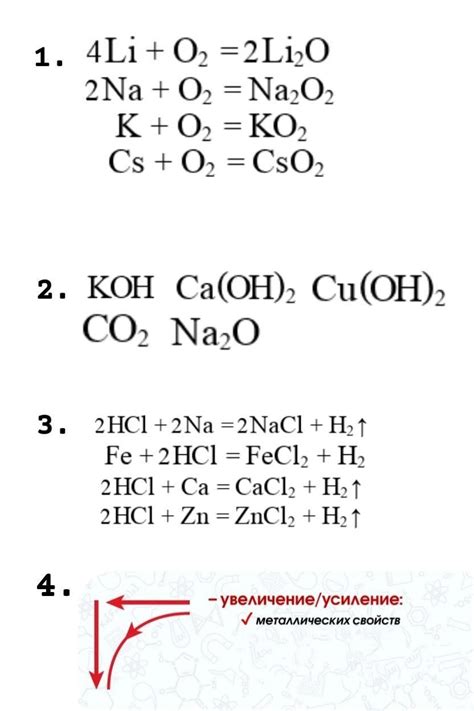
1. Образование оксидов. Многие металлы реагируют с кислородом и образуют оксиды. Например, натрий (Na) реагирует с кислородом (O2) и образует оксид натрия (Na2O).
2. Окисление металлов. Реакция металлов с кислородом приводит к их окислению. Например, железо (Fe) реагирует с кислородом и окисляется до оксида железа (Fe2O3), который является ржавчиной.
3. Образование пероксидов. Некоторые металлы могут образовывать пероксиды при взаимодействии с кислородом. Например, барий (Ba) реагирует с кислородом и образует барийпероксид (BaO2), который используется в качестве кислорода в самолетах и подводных лодках.
4. Образование гидроксидов. Некоторые металлы образуют гидроксиды при реакции с кислородом и водой. Например, натрий реагирует с кислородом и водой, образуя гидроксид натрия (NaOH), который используется в бытовой химии и в производстве стекла.
5. Коррозия металлов. Реакция металлов с кислородом может приводить к их поверхностной коррозии. Например, алюминий (Al) реагирует с кислородом и образует оксид алюминия (Al2O3), который образует защитную пленку на поверхности металла и предотвращает дальнейшую коррозию.
Практическое применение взаимодействия металлов с кислородом
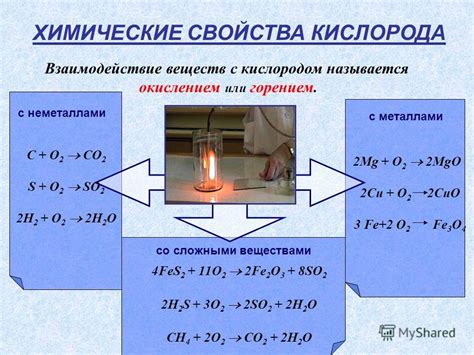
Взаимодействие металлов с кислородом имеет широкое практическое применение в различных областях науки и техники. Одной из основных причин такого интереса к данному процессу является возможность получения различных соединений, которые обладают уникальными свойствами и могут быть использованы в различных сферах деятельности.
Одним из наиболее распространенных применений взаимодействия металлов с кислородом является производство металлоксидов. Металлоксиды широко используются в качестве пигментов, катализаторов и материалов с особыми оптическими свойствами. Например, оксид железа (Fe2O3) используется в производстве красок и стекла, а оксид меди (CuO) - в производстве керамики и электроники.
Взаимодействие металлов с кислородом также находит применение в процессе получения металлических сплавов. Сплавы, состоящие из двух или более металлов, обладают улучшенными механическими и физическими свойствами по сравнению с чистыми металлами. Так, например, сталь - это сплав железа с углеродом, который обеспечивает ей прочность и твердость. Алюминий, взаимодействуя с кислородом, образует оксид алюминия, который затем может быть использован в процессе получения сплавов с другими металлами.
Взаимодействие металлов с кислородом также широко применяется в электрохимических процессах. Например, электроосаждение металла - это процесс, в котором металл, содержащийся в электролите, взаимодействует с кислородом, образуя оксид металла на электроде. Такой процесс широко используется в гальваническом покрытии, при производстве электроники и других отраслях промышленности.
Таким образом, взаимодействие металлов с кислородом имеет огромное практическое значение в различных областях и находит применение в производстве ценных материалов, сплавов и электрохимических процессах.
Вопрос-ответ

Какие металлы реагируют с кислородом?
Реагировать с кислородом могут различные металлы, такие как железо, алюминий, медь, свинец и другие. Однако, скорость реакции и ее характер могут значительно различаться в зависимости от металла и условий, в которых происходит взаимодействие.
Какие продукты образуются при реакции металлов с кислородом?
В результате взаимодействия металлов с кислородом, образуются соответствующие оксиды металлов. Например, железо образует оксид железа (Fe2O3), алюминий - оксид алюминия (Al2O3) и так далее. В некоторых случаях, оксиды могут иметь различные степени окисления металла.
Какие факторы влияют на скорость реакции металлов с кислородом?
Скорость реакции металлов с кислородом может зависеть от нескольких факторов. Один из них - активность металла. Например, щелочные металлы, такие как натрий и калий, сильно реагируют с кислородом, алкалиноземельные металлы, такие как магний и кальций, тоже образуют оксиды, но реакция идет уже не так быстро. Также скорость может зависеть от температуры, концентрации кислорода и площади поверхности металла.
