Металлы считаются одной из основных групп элементов, которые способны проявлять собственные химические свойства и образовывать соединения с другими веществами. Взаимодействие металлов с различными кислотами является одной из важных реакций, которую можно наблюдать при экспериментах в химической лаборатории. Особый интерес вызывает реакция металлов с азотной кислотой.
Азотная кислота, также известная как азотистая кислота, является сильным окислителем и относится к классу неорганических кислот. Она имеет формулу HNO3 и обладает высокой степенью коррозии, что делает ее одним из наиболее агрессивных кислотных соединений. Реакция металлов со стоящими за азотной кислотой может быть различной в зависимости от свойств и активности каждого металла.
Многие металлы, такие как железо, алюминий, цинк, реагируют с азотной кислотой, образуя соединения между атомами металла и атомами азота. При этом происходит образование нитратов металла и выделение газа. Реакция протекает с выделением тепла и может сопровождаться плавлением или образованием пены на поверхности металла.
Другие металлы, такие как серебро, золото, платина, обладают низкой активностью и не реагируют с азотной кислотой. Это связано с их высокой стабильностью и невысокими электрохимическими свойствами. При попытке взаимодействия этих металлов с азотной кислотой наблюдается отсутствие видимых изменений и отсутствие образования новых соединений.
Реакция металлов с азотной кислотой: особенности и примеры

Азотная кислота (HNO3) – один из самых распространенных и активных окислителей, которая реагирует с различными металлами. В результате таких реакций образуются соответствующие нитраты и освобождается водород.
Одной из особенностей реакции металлов с азотной кислотой является образование водорода и его выделение в виде пузырьков. Реакцию можно наблюдать, если поместить металлический листок в азотную кислоту. При этом происходит активное выделение газа и образование нитрата металла.
Например, реакция меди (Cu) с азотной кислотой приводит к образованию нитрата меди (Cu(NO3)2) и выделению водорода:
Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
Аналогичным образом происходит реакция цинка (Zn) с азотной кислотой:
Zn + 4HNO3 → Zn(NO3)2 + 2NO2 + 2H2O
Важно отметить, что реакция металлов с азотной кислотой может протекать более интенсивно при нагревании или использовании более концентрированных растворов кислоты. При этом скорость реакции и интенсивность выделения водорода могут значительно увеличиваться.
Таким образом, реакция металлов с азотной кислотой является активной и заметной, что позволяет использовать ее в различных химических опытах и промышленных процессах.
Химические свойства азотной кислоты и её взаимодействие с металлами
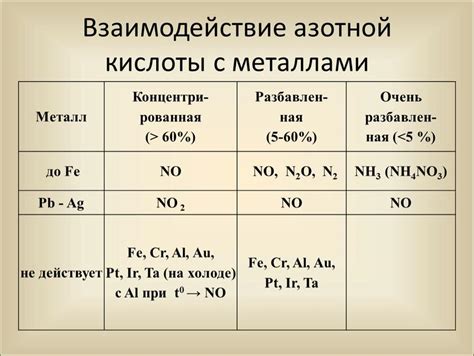
Азотная кислота, также известная как серная кислота, является одним из наиболее известных и распространенных химических соединений. Она обладает сильными окислительными свойствами и широко применяется в промышленности и лабораторных условиях.
Азотная кислота реагирует с большинством металлов, образуя соли и выделяя оксиды азота. В ходе реакции азотная кислота окисляет металл, сама же восстанавливается. В результате этой реакции образуется характерный продукт - нитрат металла.
Взаимодействие азотной кислоты с металлами осуществляется через различные механизмы. Некоторые металлы, такие как медь (Cu), цинк (Zn) и железо (Fe), активно реагируют с азотной кислотой, образуя нитраты металлов и выделяя оксиды азота.
Однако не все металлы так сильно реагируют с азотной кислотой. Например, золото (Au) и платина (Pt) сравнительно инертны к азотной кислоте и реакция с ними проходит в очень медленном темпе.
Реакция металлов с азотной кислотой может быть использована для получения нитратов металлов, которые широко применяются в различных отраслях промышленности, а также в сельском хозяйстве в качестве удобрений.
Вопрос-ответ

Какие металлы реагируют со стоящими за азотной кислотой?
Металлы, которые реагируют со стоющими за азотной кислотой, включают алюминий (Al), цинк (Zn) и железо (Fe).
В чем состоит реакция алюминия с азотной кислотой?
Реакция алюминия с азотной кислотой образует алюминий нитрат (Al(NO3)3) и выделяется окислительный газ диоксид азота (NO2).
